
|
|
Ghi chú bài giảng, phiếu đánh giá
Điều trị tại bệnh viện. Ghi chú bài giảng: ngắn gọn, quan trọng nhất
Cẩm nang / Ghi chú bài giảng, phiếu đánh giá Mục lục
BÀI GIẢNG SỐ 1. Các bệnh về hệ tim mạch. Bệnh thấp khớp Thấp khớp (Bệnh Sokolsky-Buyo) là một bệnh viêm hệ thống của mô liên kết với sự bản địa hóa chủ yếu của quá trình trong hệ thống tim mạch, phát triển ở những người dễ mắc bệnh này (theo quy luật, đây là những người trẻ tuổi) do nhiễm trùng cấp tính với liên cầu tan huyết nhóm A. Định nghĩa về căn bệnh này được đưa ra vào năm 1989 bởi V. A. Nasonov. Nó phản ánh tất cả các tính năng đặc trưng của bệnh: 1) thiệt hại chủ yếu đối với hệ thống tim mạch; 2) vai trò của tính di truyền bệnh lý; 3) tầm quan trọng của nhiễm trùng liên cầu. Bản chất của bệnh nằm ở sự đánh bại tất cả các màng của tim, nhưng chủ yếu là cơ tim và nội tâm mạc với sự xuất hiện của sự biến dạng của bộ máy van tim - bệnh tim và sự phát triển sau đó của suy tim. Sự thất bại của các cơ quan và hệ thống khác trong bệnh thấp khớp có tầm quan trọng thứ yếu và không xác định mức độ nghiêm trọng và tiên lượng sau đó của nó. Nguyên nhân. Liên cầu khuẩn tan máu beta nhóm A gây tổn thương đường hô hấp trên. Đó là lý do tại sao, theo nguyên tắc, sự khởi phát của bệnh thấp khớp thường xảy ra sau cơn đau họng, đợt viêm amidan mãn tính trầm trọng hơn và lượng kháng nguyên liên cầu và kháng thể kháng liên cầu (ASL-O, ASG, ASA, antideoxyribonuclease B (anti-DNase) tăng lên B)) được phát hiện trong máu của người bệnh. Mối liên hệ như vậy với bệnh nhiễm trùng liên cầu trước đó đặc biệt rõ rệt trong đợt cấp tính của bệnh thấp khớp, kèm theo viêm đa khớp. Trong sự phát triển của bệnh thấp khớp, tuổi tác và các yếu tố xã hội đóng một vai trò (điều kiện sống không thuận lợi, suy dinh dưỡng), yếu tố di truyền cũng quan trọng (bệnh thấp khớp là một bệnh di truyền đa gen, sự tồn tại của các gia đình “thấp khớp” được biết đến nhiều), bao gồm đáp ứng cường miễn dịch với các kháng nguyên liên cầu, khuynh hướng của bệnh nhân đối với các quá trình tự miễn dịch và đơn giản hóa miễn dịch. Sinh bệnh học. Với bệnh thấp khớp, một phản ứng miễn dịch phức tạp và đa dạng xảy ra (phản ứng quá mẫn ngay lập tức và chậm) đối với nhiều kháng nguyên liên cầu khuẩn. Khi nhiễm trùng xâm nhập vào cơ thể, các kháng thể chống liên cầu khuẩn được tạo ra và các phức hợp miễn dịch được hình thành (kháng nguyên liên cầu + kháng thể chống lại chúng + bổ sung), lưu thông trong máu và lắng đọng trong giường vi tuần hoàn. Độc tố và enzyme liên cầu khuẩn cũng có tác động gây hại đến cơ tim và mô liên kết. Do một khiếm khuyết được xác định về mặt di truyền trong hệ thống miễn dịch, các kháng nguyên và phức hợp miễn dịch của liên cầu không được đào thải hoàn toàn và nhanh chóng khỏi cơ thể người bệnh. Các mô của những bệnh nhân này có xu hướng gia tăng để cố định các phức hợp miễn dịch này. Các kháng thể phản ứng chéo cũng đóng một vai trò ở đây, được hình thành trên các kháng nguyên của liên cầu, có thể phản ứng với mô, bao gồm cả kháng nguyên tim, của cơ thể. Đáp lại, tình trạng viêm phát triển trên cơ sở miễn dịch (theo kiểu quá mẫn tức thì), trong khi các yếu tố thực hiện quá trình viêm là các enzym lysosome của bạch cầu trung tính thực bào các phức hợp miễn dịch và đồng thời bị tiêu diệt. Quá trình viêm này khu trú trong mô liên kết, chủ yếu là của hệ thống tim mạch, và làm thay đổi các đặc tính kháng nguyên của nó và cơ tim. Kết quả là, quá trình tự miễn dịch phát triển theo kiểu quá mẫn kiểu chậm, và các tế bào lympho phản ứng với mô tim được tìm thấy trong máu của bệnh nhân. Những tế bào này có tầm quan trọng lớn trong nguồn gốc của các tổn thương cơ quan (chủ yếu là tim). Trong mô liên kết với bệnh thấp khớp, các thay đổi giai đoạn xảy ra: sưng mucoid - thay đổi fibrinoid - hoại tử fibrinoid. Biểu hiện hình thái của rối loạn miễn dịch là phản ứng tế bào - sự xâm nhập của tế bào lympho và tế bào bạch cầu, hình thành bệnh thấp khớp, hoặc Ashoff-Talalayevsky, u hạt. Quá trình bệnh lý kết thúc bằng chứng xơ cứng. Một cơ chất hình thái khác của tổn thương tim trong bệnh thấp tim là phản ứng viêm không đặc hiệu tương tự như ở khớp và màng huyết thanh: sưng mô liên kết giữa các cơ, đổ mồ hôi fibrin, thâm nhiễm bởi bạch cầu trung tính và tế bào lympho. Bệnh phát từng đợt, trầm trọng hơn dưới tác động của nhiễm trùng hoặc các yếu tố không đặc hiệu (hạ thân nhiệt, căng thẳng thể chất, căng thẳng, v.v.), có liên quan đến tính chất tự miễn dịch của quá trình bệnh lý. Khi tim bị tổn thương, quá trình viêm có thể lan đến tất cả các màng của tim (viêm tim) hoặc riêng biệt với từng màng. Những thay đổi về hình thái của bệnh thấp khớp được tìm thấy chủ yếu ở cơ tim, vì vậy chính viêm cơ tim ở giai đoạn đầu sẽ quyết định bệnh cảnh lâm sàng. Những thay đổi về viêm ở nội tâm mạc (viêm van tim, viêm màng trong tim), tổn thương các sợi gân và vòng xơ được phát hiện trên lâm sàng 6-8 tuần sau khi bị bệnh thấp khớp tấn công. Van hai lá thường bị ảnh hưởng nhất, sau đó là van động mạch chủ và van ba lá. Van động mạch phổi trong bệnh thấp khớp hầu như không bị ảnh hưởng. Phân loại bệnh thấp khớp. Hiện nay, việc phân loại và danh pháp bệnh thấp khớp, được Hiệp hội Khoa học Thấp khớp Liên minh phê duyệt năm 1990, đã được thông qua, phản ánh giai đoạn của quá trình, đặc điểm lâm sàng và giải phẫu của tổn thương các cơ quan và hệ thống, bản chất của khóa học. và trạng thái chức năng của hệ thống tim mạch (xem Bảng 1). Ảnh lâm sàng. Tất cả các biểu hiện của bệnh có thể được chia thành tim và ngoài tim. Hình ảnh lâm sàng của bệnh có thể được mô tả từ những vị trí này. Giai đoạn I: sự kết nối của bệnh với nhiễm trùng được chuyển được tiết lộ. Trong trường hợp điển hình, 1-2 tuần sau khi bị viêm họng hoặc bệnh hô hấp cấp tính, nhiệt độ cơ thể tăng lên, có khi lên đến 38-40 ° C, dao động trong ngày trong vòng 1-2 ° C và đổ mồ hôi nhiều (thường không có cảm giác ớn lạnh). Với các đợt tấn công lặp đi lặp lại của bệnh thấp khớp, bệnh tái phát thường phát triển dưới ảnh hưởng của các yếu tố không đặc hiệu (như hạ thân nhiệt, quá tải về thể chất, phẫu thuật). Bảng 1 Phân loại bệnh thấp khớp
Biểu hiện thường thấy của bệnh thấp khớp là tổn thương tim - bệnh thấp tim: tổn thương đồng thời cơ tim và nội tâm mạc. Ở người lớn, bệnh thấp tim không nặng. Bệnh nhân phàn nàn về đau nhẹ hoặc khó chịu ở vùng tim, khó thở nhẹ khi vận động, gián đoạn hoặc đánh trống ngực ít phổ biến hơn nhiều. Các triệu chứng này không đặc trưng cho bệnh thấp tim và có thể gặp ở các bệnh tim khác. Bản chất của các khiếu nại như vậy được xác định ở các giai đoạn tiếp theo của quá trình tìm kiếm chẩn đoán. Theo quy luật, bệnh thấp tim ở những bệnh nhân trẻ tuổi rất nghiêm trọng: ngay từ khi bắt đầu bệnh, khó thở dữ dội khi vận động và khi nghỉ ngơi, đau liên tục ở tim và đánh trống ngực. Có thể có các triệu chứng suy tuần hoàn thành một vòng tròn lớn dưới dạng phù nề và nặng hơn ở vùng hạ vị bên phải (do gan tăng tiết). Tất cả những triệu chứng này chỉ ra tình trạng viêm cơ tim lan tỏa nghiêm trọng. Viêm màng ngoài tim, cũng như các biểu hiện ngoài tim của bệnh thấp khớp, rất hiếm. Với sự phát triển của viêm màng ngoài tim khô, bệnh nhân lưu ý chỉ đau liên tục ở vùng của tim. Với viêm màng ngoài tim tiết dịch, được đặc trưng bởi sự tích tụ dịch tiết dạng sợi huyết thanh trong túi tim, cơn đau sẽ biến mất, khi các tấm màng ngoài tim bị viêm được tách ra bởi dịch tiết tích tụ. Khó thở xuất hiện, tăng dần theo tư thế nằm ngang của bệnh nhân. Do máu khó lưu thông về tim phải, xung huyết xuất hiện thành vòng tròn lớn (phù nề, nặng lên vùng hạ vị bên phải do gan tăng tiết). Đặc trưng nhất của bệnh thấp khớp là sự thất bại của hệ thống cơ xương khớp dưới dạng viêm đa khớp dạng thấp. Bệnh nhân ghi nhận cơn đau tăng nhanh ở các khớp lớn (đầu gối, khuỷu tay, vai, cổ chân, cổ tay), không thể vận động chủ động, tăng khối lượng khớp. Có một tác dụng nhanh chóng sau khi sử dụng axit acetylsalicylic và các thuốc chống viêm không steroid khác với sự thuyên giảm trong vài ngày, thường là vài giờ đối với tất cả các biểu hiện khớp. Các tổn thương thận do thấp khớp cũng cực kỳ hiếm, chỉ được phát hiện trong nghiên cứu nước tiểu. Tổn thương hệ thần kinh trong bệnh thấp khớp rất hiếm, chủ yếu ở trẻ em. Các khiếu nại tương tự như các trường hợp viêm não, viêm màng não, viêm mạch máu não do căn nguyên khác. Chỉ có "chứng múa giật nhỏ" mới đáng được quan tâm, xảy ra ở trẻ em (thường là trẻ em gái) và được biểu hiện bằng sự kết hợp của cảm xúc hoang mang và sự tăng vận động dữ dội của thân, tay chân và các cơ bắt chước. Hội chứng bụng (viêm phúc mạc) hầu như chỉ xảy ra ở trẻ em và thanh thiếu niên bị thấp khớp nguyên phát cấp tính. Nó được đặc trưng bởi khởi phát đột ngột, sốt và các dấu hiệu của chứng khó nuốt (đau chuột rút lan tỏa hoặc khu trú, buồn nôn, nôn, đi ngoài phân sống hoặc đi ngoài phân sống). Ở giai đoạn II của việc tìm kiếm chẩn đoán, việc phát hiện các dấu hiệu tổn thương tim là rất ít quan trọng. Trong bệnh thấp tim nguyên phát, tim thường không to. Nghe tim thai cho thấy âm I bị bóp nghẹt, đôi khi xuất hiện âm III, âm thổi tâm thu mềm ở đỉnh. Triệu chứng này là do những thay đổi trong cơ tim. Tuy nhiên, sự gia tăng cường độ, thời gian và sự tồn tại của tiếng ồn có thể cho thấy sự hình thành của bệnh suy van hai lá. Có thể tự tin phán đoán sự hình thành khuyết tật 6 tháng sau khi bắt đầu cơn, trong khi vẫn duy trì hình ảnh nghe tim trên. Trong trường hợp van động mạch chủ bị tổn thương, có thể nghe thấy tiếng thổi cuối tâm trương tại điểm Botkin và độ âm của âm II có thể được duy trì. Chỉ nhiều năm sau, sau khi hình thành thiểu năng van động mạch chủ nặng, sự suy yếu (hoặc vắng mặt) của trương lực II ở khoang liên sườn II bên phải mới tham gia vào dấu hiệu nghe tim này. Ở bệnh nhân viêm đa khớp, biến dạng khớp được ghi nhận do viêm màng hoạt dịch và các mô quanh khớp, đau khi sờ khớp. Trong khu vực của các khớp bị ảnh hưởng, các nốt thấp khớp có thể xuất hiện, nằm trên cẳng tay và ống chân, phía trên phần xương nhô ra. Đây là những hình thành nhỏ, dày đặc, không đau và biến mất dưới ảnh hưởng của điều trị. Erythema annulare (một dấu hiệu gần như bệnh lý đối với bệnh thấp khớp) là các phần tử hình nhẫn màu hồng, không ngứa, nằm trên da của bề mặt bên trong của cánh tay và chân, bụng, cổ và thân. Triệu chứng này cực kỳ hiếm gặp (ở 1-2% bệnh nhân). Viêm phổi thấp khớp và viêm màng phổi có các dấu hiệu thực thể giống như các bệnh tương tự về căn nguyên tầm thường. Nhìn chung, các tổn thương không do tim hiện được quan sát thấy cực kỳ hiếm, ở những người trẻ tuổi có đợt cấp tính của bệnh thấp khớp (khi hoạt động nhiều - độ III). Chúng được biểu hiện một cách rõ ràng, nhanh chóng có thể được điều chỉnh để đảo ngược sự phát triển trong quá trình điều trị chống chấn thương. Ở giai đoạn III của tìm kiếm chẩn đoán, dữ liệu của các nghiên cứu trong phòng thí nghiệm và dụng cụ cho phép chúng ta thiết lập hoạt động của quá trình bệnh lý và làm rõ tổn thương tim và các cơ quan khác. Với một quá trình điều trị thấp khớp tích cực, các xét nghiệm trong phòng thí nghiệm cho thấy giai đoạn cấp tính không đặc hiệu và các thông số miễn dịch bị thay đổi. Các chỉ số giai đoạn cấp tính: bạch cầu trung tính với sự thay đổi công thức máu của bạch cầu sang trái; sự gia tăng nội dung của 2-globulin, tiếp theo là sự gia tăng mức độ của - globulin; tăng hàm lượng fibrinogen; sự xuất hiện của protein phản ứng C; ESR tăng lên. Về các thông số miễn dịch, hiệu giá của các kháng thể chống liên cầu tăng lên (anti-hyaluronidase và antistreptokinase hơn 1: 300, anti-O-streptolysin hơn 1: 250). Điện tâm đồ đôi khi cho thấy rối loạn nhịp và dẫn truyền: phong tỏa nhĩ thất thoáng qua (thường gặp hơn độ I - kéo dài khoảng P-Q, ít thường xuyên hơn - độ II), ngoại tâm thu, nhịp nhĩ thất. Ở một số bệnh nhân, sự giảm biên độ của sóng T được ghi nhận cho đến khi xuất hiện răng âm. Những rối loạn về nhịp và dẫn truyền này không ổn định và nhanh chóng biến mất trong quá trình điều trị bằng thuốc chống suy nhược cơ thể. Nếu những thay đổi trên điện tâm đồ liên tục và vẫn còn sau khi loại bỏ cơn thấp khớp, thì người ta nên nghĩ đến tổn thương hữu cơ đối với cơ tim. Trong quá trình kiểm tra điện tâm đồ, dữ liệu nghe tim được chỉ định: sự suy yếu của âm thứ XNUMX, sự xuất hiện của âm thứ XNUMX, tiếng thổi tâm thu. Trong trường hợp hình thành bệnh tim, những thay đổi xuất hiện trên PCG tương ứng với bản chất của tổn thương van tim. Chụp X-quang ở đợt tấn công đầu tiên của bệnh thấp khớp, không phát hiện ra những thay đổi. Chỉ với bệnh thấp tim nặng ở trẻ em và người trẻ tuổi mới có thể phát hiện được tim tăng do tâm thất trái giãn ra. Với sự phát triển của bệnh thấp tim trên nền của bệnh tim hiện có, hình ảnh X quang sẽ tương ứng với một khiếm khuyết cụ thể. Một nghiên cứu siêu âm tim ở bệnh thấp tim nguyên phát không cho thấy bất kỳ thay đổi đặc trưng nào. Chỉ trong bệnh thấp tim nặng có dấu hiệu suy tim trên siêu âm tim mới có dấu hiệu cho thấy chức năng co bóp của cơ tim giảm và các khoang tim giãn nở. Chẩn đoán. Việc nhận biết bệnh thấp khớp nguyên phát là rất khó khăn vì các biểu hiện phổ biến nhất của bệnh như viêm đa khớp và tổn thương tim đều không đặc hiệu. Hiện nay, các tiêu chuẩn chính và phụ để chẩn đoán bệnh thấp khớp của Hiệp hội Tim mạch Hoa Kỳ được sử dụng rộng rãi nhất. Sự kết hợp của hai tiêu chí chính hoặc một tiêu chí chính và hai tiêu chí phụ cho thấy khả năng mắc bệnh thấp khớp cao hơn chỉ trong những trường hợp nhiễm liên cầu khuẩn trước đó. Với sự khởi phát dần dần của bệnh thấp khớp, chẩn đoán hội chứng được đề xuất bởi A. I. Nesterov vào năm 1973 (xem Bảng 2) là các vấn đề: hội chứng lâm sàng và dịch tễ học (liên quan đến nhiễm trùng liên cầu); hội chứng lâm sàng và miễn dịch (dấu hiệu của việc dưỡng bệnh không hoàn toàn, đau khớp, tăng hiệu giá của kháng thể kháng liên cầu, cũng như phát hiện rối loạn protein máu và các chỉ số giai đoạn cấp tính); hội chứng tim mạch (phát hiện viêm tim, cũng như các tổn thương ngoài tim) (xem Bảng 3). Bảng 2 Tiêu chuẩn cho bệnh thấp khớp
Bảng 3 Mức độ thấp khớp
Chẩn đoán phân biệt. Viêm đa khớp do thấp khớp phải được phân biệt với bệnh không do thấp khớp (xem Bảng 4). Bảng 4 Viêm đa khớp thấp khớp và không thấp khớp
Các bệnh và triệu chứng sau đây được nghi ngờ có liên quan đến bệnh thấp khớp: 1) viêm nội tâm mạc; 2) viêm cơ tim; 3) viêm màng ngoài tim; 4) khuyết tật tim; 5) rối loạn nhịp điệu và dẫn truyền; 6) suy tim cấp tính và mãn tính; 7) tình trạng mụn thịt kéo dài; 8) ban đỏ nốt sần; 9) ban đỏ hình khuyên; 10) nốt sần dưới da; 11) viêm đa khớp dị ứng cấp tính; 12) múa giật. Không có hội chứng lâm sàng nào được liệt kê ở trên là đặc hiệu của bệnh này. Chỉ có sự kết hợp của bệnh lý tim với ít nhất một triệu chứng chính ngoài tim của bệnh thấp khớp mới có lý do để nghi ngờ bệnh thấp khớp. Bản thân việc nhận biết bệnh thấp tim được thực hiện trên cơ sở các triệu chứng như khó thở và hồi hộp, mệt mỏi, đau ở vùng tim và rối loạn nhịp tim, tiếng ồn, đôi khi là nhịp phi nước đại và âm I suy yếu. Điều quan trọng trong chẩn đoán bệnh thấp tim là xác định bệnh lý trên điện tâm đồ. Trong bệnh thấp khớp, nó là do viêm cơ tim, viêm màng ngoài tim và các khuyết tật ở tim. Quan sát động giúp phân biệt những thay đổi không thể đảo ngược đặc trưng của phì đại các bộ phận khác nhau của tim trong trường hợp khuyết tật, với những thay đổi thoáng qua, cho thấy quá trình viêm hiện tại. Điều trị. Hiệu quả tích cực trong điều trị, cũng như ngăn ngừa sự phát triển của bệnh tim, được tạo điều kiện thuận lợi bằng chẩn đoán sớm và điều trị riêng lẻ, dựa trên đánh giá về loại khóa học, hoạt động của quá trình bệnh lý, mức độ nghiêm trọng của bệnh viêm tim, và các biến thể của bệnh van tim. Tình trạng của cơ tim, các mô và cơ quan khác, nghề nghiệp của bệnh nhân, v.v. đều quan trọng. Do đó, toàn bộ phức hợp điều trị bệnh thấp khớp bao gồm liệu pháp kháng khuẩn và chống viêm, các biện pháp nhằm phục hồi cân bằng nội môi miễn dịch. Nên sử dụng một chế độ ăn uống cân bằng hợp lý, tập trung vào việc thích nghi với hoạt động thể chất, chuẩn bị cho công việc, phẫu thuật điều trị kịp thời những bệnh nhân có dị tật tim phức tạp. Tất cả bệnh nhân trong giai đoạn hoạt động của bệnh thấp khớp đều được dùng penicillin (1-200 IU cho 000 liều mỗi ngày, cứ 1 giờ một lần), có tác dụng diệt khuẩn đối với tất cả các loại liên cầu A. Quá trình điều trị là 500 tuần trong giai đoạn hoạt động của bệnh thấp khớp, trong tương lai, cần phải chuyển sang thuốc kéo dài bicillin-000 (6 đơn vị). Không dung nạp với penicillin, có thể kê đơn erythromycin 4 mg 2 lần một ngày. Thuốc có tác dụng chống viêm được sử dụng trong điều trị hiện đại giai đoạn hoạt động của bệnh thấp khớp là glucocorticosteroid, salicylic, dẫn xuất indole, dẫn xuất của axit phenylacetic, v.v. Prednisolone được sử dụng với liều 20-30 mg mỗi ngày (trong 2 tuần, sau đó giảm liều 2,5-5 mg mỗi 5-7 ngày, tổng cộng trong một đợt 1,5-2 tháng) cho bệnh nguyên phát và tái phát với III và II. mức độ hoạt động của quá trình bệnh tim thấp khớp, với viêm đa khớp và múa giật, với sự phát triển của suy tim do viêm tim hoạt động. Trong trường hợp thứ hai, ưu tiên dùng triamcinolone với liều 12-16 mg mỗi ngày, vì nó ít có khả năng làm rối loạn cân bằng điện giải. Các tác nhân Corticoid ảnh hưởng đến chuyển hóa nước-muối, do đó, nên sử dụng kali clorid 3-4 g / ngày, panangin và các thuốc khác trong điều trị có giữ nước - thuốc đối kháng aldosterone (veroshpiron lên đến 6-8 viên mỗi ngày), thuốc lợi tiểu (lasix 40 -80 mg / ngày, furosemide 40-80 mg / ngày, v.v.), với thuốc gây hưng phấn - thuốc an thần, v.v. Thuốc chống viêm không steroid cũng được sử dụng rộng rãi cho bệnh thấp khớp: liều trung bình của axit acetylsalicylic là 3-4 g mỗi ngày, ít hơn thường là 5 g mỗi ngày hoặc hơn. Chỉ định sử dụng salicylat: 1) mức độ hoạt động tối thiểu, mức độ nghiêm trọng nhẹ của viêm tim, chủ yếu là viêm cơ tim; 2) điều trị lâu dài bệnh thấp khớp, nghi ngờ về một khóa học tiềm ẩn; 3) điều trị kéo dài với việc giảm hoạt động của quá trình và ngừng sử dụng corticosteroid, cũng như sau khi hoàn thành điều trị tại bệnh viện; 4) bệnh tim thấp tái phát xảy ra trên cơ sở các khuyết tật tim nặng và suy tuần hoàn, vì salicylat không có khả năng giữ chất lỏng, ngăn ngừa sự hình thành cục máu đông, và là chất kích thích trung tâm hô hấp; 5) giảm khả năng xuất hiện đợt cấp của bệnh thấp khớp vào mùa xuân và mùa thu, cũng như sau khi bị nhiễm trùng đồng thời (cùng với thuốc kháng sinh). Axit acetylsalicylic được sử dụng 1 g 3-4 lần một ngày sau bữa ăn trong 1-3 tháng trở lên với mức dung nạp bình thường và có thể kiểm soát các tác dụng phụ. Việc sử dụng thành công dẫn xuất acid indolacetic - indomethacin trong bệnh thấp khớp hơn 20 năm. Nó có hiệu quả điều trị rõ rệt: các triệu chứng chủ quan của bệnh viêm tim (đau cơ tim, đánh trống ngực, khó thở) biến mất vào ngày điều trị thứ 8-10 và các dấu hiệu khách quan - vào ngày thứ 14-16. Sự biến mất của viêm đa khớp và viêm đa khớp diễn ra nhanh hơn. Trong điều trị bệnh phong thấp cần quan tâm kết hợp XNUMX khâu chính: bệnh viện - phòng khám - nghỉ dưỡng. Trong bệnh viện, điều trị được thực hiện với các loại thuốc được liệt kê ở trên. Sau khi giảm hoạt động của bệnh thấp khớp và bình thường hóa tình trạng của bệnh nhân, họ được chuyển sang giai đoạn II - điều trị tại một viện điều dưỡng thấp khớp. Mục tiêu chính của giai đoạn này là tiếp tục điều trị bằng thuốc chống viêm không steroid, được lựa chọn riêng tại bệnh viện, dẫn xuất aminoquinoline, bicillin-5, phục hồi chức năng. Giai đoạn III bao gồm theo dõi trạm y tế và điều trị dự phòng. Đây là việc thực hiện các biện pháp điều trị nhằm mục đích loại bỏ cuối cùng của quá trình hoạt động của quá trình thấp khớp; tiến hành điều trị triệu chứng rối loạn tuần hoàn ở bệnh nhân bệnh tim; giải quyết các vấn đề về phục hồi chức năng, khả năng lao động và việc làm; thực hiện phòng ngừa ban đầu của bệnh thấp khớp và phòng ngừa thứ phát tái phát của bệnh. BÀI GIẢNG SỐ 2. Các bệnh về hệ tim mạch. Bệnh cơ tim. Bệnh cơ tim giãn nở 1. Bệnh cơ tim Bệnh cơ tim - các tổn thương cơ tim cô lập nguyên phát có tính chất không viêm không rõ nguyên nhân (vô căn), chúng không liên quan đến các khuyết tật van tim hoặc tắc nghẽn trong tim, tăng áp động mạch hoặc phổi, bệnh tim mạch vành hoặc các bệnh hệ thống (như: bệnh collagenose, bệnh amyloidosis, bệnh huyết sắc tố, vv), và trong giai đoạn cuối của bệnh, suy tim sung huyết nặng và rối loạn nhịp tim và nhịp tim phức tạp phát triển. Phân loại bệnh cơ tim như sau: 1) bệnh cơ tim giãn nở: a) vô căn; b) độc hại; c) lây nhiễm; d) với ảnh ghép; 2) phì đại; 3) hạn chế; 4) loạn sản loạn nhịp của tâm thất phải; 5) sự kết hợp của một trong 4 loại bệnh cơ tim với tăng huyết áp động mạch. 2. Bệnh cơ tim giãn nở Bệnh cơ tim giãn nở (DCM) là một bệnh của cơ tim được đặc trưng bởi sự giãn nở lan tỏa của tất cả các buồng tim (chủ yếu là tâm thất trái), trong đó bệnh lý về chức năng bơm máu của tim là ở phía trước và kết quả là , suy tim mãn tính (do đó có tên thứ hai là sung huyết, khi tim không thể bơm máu đầy đủ và nó "ứ đọng" trong các mô và cơ quan của cơ thể). Thành cơ của tim không thay đổi hoặc phì đại ở các mức độ khác nhau. Các bệnh và các yếu tố trước sự phát triển của DCM được mô tả trong bảng dưới đây (xem Bảng 5). Bảng 5 Các bệnh và các yếu tố trước sự phát triển của DCMP
Đây là dạng tổn thương cơ tim phổ biến nhất. Tỷ lệ mắc bệnh là 5-8 trường hợp trên 100 người mỗi năm. Không có tiền sử gia đình rõ ràng cho những bệnh nhân này. Nam giới mắc bệnh nhiều hơn nữ giới gấp 000-2 lần. Sinh bệnh học. Do quá trình viêm trong cơ tim (viêm cơ tim), sự chết của từng tế bào xảy ra ở các bộ phận khác nhau của nó. Trong trường hợp này, tình trạng viêm có bản chất là do virus và các tế bào bị ảnh hưởng bởi virus sẽ trở thành tác nhân lạ cho cơ thể. Theo đó, khi các kháng nguyên xuất hiện trong cơ thể, một phức hợp phản ứng miễn dịch sẽ phát triển nhằm tiêu diệt chúng. Dần dần, các tế bào cơ chết được thay thế bằng mô liên kết, mô liên kết không còn khả năng giãn nở và co bóp vốn có của cơ tim. Do mất các chức năng cơ bản của cơ tim, tim mất khả năng hoạt động như một cái bơm. Để đáp ứng với điều này (như một phản ứng bù trừ), các buồng tim sẽ mở rộng (tức là chúng giãn ra), và ở phần còn lại của cơ tim, sự dày lên và nén lại xảy ra (tức là sự phì đại của nó phát triển). Để tăng cường cung cấp oxy đến các cơ quan và mô của cơ thể, nhịp tim tăng liên tục sẽ xảy ra (nhịp tim nhanh xoang). Đáp ứng bù trừ này chỉ cải thiện tạm thời chức năng bơm máu của tim. Tuy nhiên, khả năng giãn và phì đại cơ tim bị giới hạn bởi số lượng cơ tim còn sống và là từng cá thể đối với từng trường hợp cụ thể của bệnh. Với sự chuyển đổi của quá trình sang giai đoạn mất bù, suy tim mãn tính phát triển. Tuy nhiên, ở giai đoạn này, một cơ chế bù trừ khác phát huy tác dụng: các mô của cơ thể tăng hút oxy từ máu so với cơ thể khỏe mạnh. Nhưng cơ chế này là không đủ, vì giảm chức năng bơm của tim dẫn đến giảm cung cấp oxy cho các cơ quan và mô, vốn cần thiết cho hoạt động bình thường của chúng, trong khi lượng carbon dioxide trong chúng tăng lên. Ở 2/3 số bệnh nhân trong các khoang của tâm thất trong giai đoạn muộn của bệnh, huyết khối thành được hình thành (do giảm chức năng bơm máu của tim, cũng như sự co bóp không đồng đều của cơ tim trong các khoang của tim), tiếp theo là sự phát triển của thuyên tắc trong tuần hoàn phổi hoặc hệ thống. Những thay đổi bệnh lý và hình thái bệnh lý ở tim. Hình dạng của tim trở thành hình cầu, khối lượng của nó tăng từ 500 đến 1000 g, chủ yếu là do tâm thất trái. Cơ tim trở nên nhão, xỉn màu, với các lớp mô liên kết màu trắng đáng chú ý, có sự xen kẽ đặc trưng của các tế bào cơ tim phì đại và teo. Xét nghiệm vi thể, xơ hóa lan tỏa được phát hiện, nó có thể kết hợp với cả teo và phì đại của tế bào cơ tim, trong đó có sự gia tăng đáng kể về thể tích nhân, số lượng ty thể, tăng sản bộ máy Golgi, tăng số lượng myofibrils , tự do và liên kết với các ribosome của lưới nội chất, một lượng dồi dào các hạt glycogen. Ảnh lâm sàng. Không có dấu hiệu cụ thể của bệnh. Hình ảnh lâm sàng đa hình và được xác định bởi: 1) các triệu chứng của suy tim; 2) rối loạn nhịp điệu và dẫn truyền; 3) hội chứng huyết khối tắc mạch. Tất cả các hiện tượng này phát triển trong giai đoạn cuối của bệnh, và do đó việc nhận biết DCM trước khi xuất hiện các triệu chứng này gặp khó khăn đáng kể. Trong hầu hết các trường hợp, tiên lượng của bệnh được xác định bởi sự thất bại của tâm thất trái của tim. Trước khi khởi phát suy tim, DCM tiềm ẩn. Những phàn nàn thường gặp nhất của bệnh suy tim đã khởi phát là những lời phàn nàn về giảm hiệu suất, tăng mệt mỏi, khó thở khi gắng sức và sau đó là khi nghỉ ngơi. Vào ban đêm, anh ta bị ho khan (tương đương với bệnh hen tim), sau đó - những cơn hen suyễn điển hình. Bệnh nhân có biểu hiện đau thắt ngực đặc trưng. Với sự phát triển của tắc nghẽn trong tuần hoàn hệ thống, nặng hơn xuất hiện ở vùng hạ vị bên phải (do gan to), phù chân. Chẩn đoán. Khi chẩn đoán bệnh, một dấu hiệu quan trọng là tim to ra đáng kể (không có dấu hiệu của bệnh van tim hoặc tăng huyết áp động mạch). Bệnh tim to được biểu hiện bằng sự giãn nở của tim theo cả hai hướng, được xác định bằng cách gõ, cũng như sự dịch chuyển của xung đỉnh sang trái và xuống. Trong trường hợp nặng, người ta có thể nghe thấy nhịp phi nước đại, nhịp tim nhanh và âm thanh tương đối suy yếu của van hai lá hoặc van ba lá. Rung tâm nhĩ phát triển trong 20% trường hợp. Huyết áp thường bình thường hoặc tăng nhẹ (do suy tim). Các nghiên cứu sinh hóa về máu và nước tiểu có thể phát hiện ra các chất độc hại khác nhau, cũng như sự thiếu hụt vitamin. Các phương pháp nghiên cứu công cụ giúp bạn có thể phát hiện: 1) dấu hiệu của chứng to tim; 2) thay đổi các chỉ số về huyết động trung tâm; 3) rối loạn nhịp điệu và dẫn truyền. Không có thay đổi đặc trưng nào trên điện tâm đồ hoặc sự thay đổi không đặc hiệu. Đây là những dấu hiệu của sự tăng kích thước của tim, rối loạn dẫn truyền dưới dạng phong tỏa nhánh trước của bó nhĩ thất trái (bó His) hoặc phong tỏa hoàn toàn chân trái (15% trường hợp. ); cũng như nhịp tim nhanh xoang dai dẳng (nhịp tim thường vượt quá 100 nhịp mỗi phút). Điện tâm đồ xác nhận dữ liệu nghe tim dưới dạng nhịp phi nước đại, một phát hiện khá thường xuyên của tiếng thổi tâm thu (do suy van hai lá hoặc van ba lá tương đối). Với sự tắc nghẽn trong tuần hoàn phổi, một trọng âm của giai điệu II được tiết lộ. Chụp X-quang cho thấy tâm thất tăng lên đáng kể (thường kết hợp với tăng trung bình tâm nhĩ trái) và máu ứ trong tuần hoàn phổi (nhỏ). Các vi phạm trong tuần hoàn phổi được biểu hiện bằng sự gia tăng mô hình mạch máu phổi, cũng như sự xuất hiện của dịch chuyển trong các khoang màng phổi, được hình thành do tăng áp lực trong các mạch phổi. Phương pháp siêu âm tim là một trong những phương pháp chính trong chẩn đoán bệnh. Siêu âm tim giúp phát hiện giãn cả hai tâm thất, giảm vận động của thành sau tâm thất trái, chuyển động nghịch thường của vách liên thất trong thời gian tâm thu. Ngoài ra, siêu âm tim cho phép bạn làm rõ sự gia tăng biên độ chuyển động của các lá van hai lá không thay đổi. Các nghiên cứu công cụ bổ sung không bắt buộc để chẩn đoán, nhưng kết quả của chúng cho phép chúng tôi chi tiết mức độ rối loạn huyết động và bản chất của những thay đổi hình thái trong cơ tim. Một nghiên cứu đồng vị phóng xạ của tim (xạ hình cơ tim) được thực hiện để làm rõ tình trạng chức năng bơm của tim, cũng như xác định các khu vực của cơ tim chết. Nghiên cứu các chỉ số về huyết động trung tâm cho thấy thể tích phút và đột quỵ thấp (chỉ số phút và đột quỵ), sự gia tăng áp lực trong động mạch phổi. Về phương diện tim mạch, những thay đổi tương tự được phát hiện như trên siêu âm tim. Sinh thiết cơ tim sống không phải là thông tin để xác định căn nguyên của bệnh cơ tim. Trong một số trường hợp, sinh thiết có thể phát hiện kháng nguyên virus hoặc sự gia tăng hàm lượng LDH, cũng như sự suy giảm sản xuất năng lượng của ty thể. Tuy nhiên, phương pháp phẫu thuật này có thể được sử dụng để làm rõ căn nguyên của bệnh và điều trị thêm. Thao tác được thực hiện như sau: dưới gây tê cục bộ, một động mạch và tĩnh mạch lớn được đâm xuyên (chọc thủng), sau đó một dụng cụ đặc biệt có kéo nhỏ ở cuối được đưa theo đường đi của chúng đến tim. Khi sinh thiết cơ tim kết hợp với chụp mạch vành (tiêm thuốc cản quang vào động mạch vành cung cấp cho tim), có thể loại trừ bệnh động mạch vành ở một bệnh nhân là một trong những bệnh có triệu chứng tương tự như DCM. Hai nghiên cứu này được thực hiện dưới sự kiểm soát của truyền hình tia X. Chẩn đoán phân biệt. Nó được tạo ra chủ yếu với bệnh viêm cơ tim và chứng loạn dưỡng cơ tim, tức là với những tình trạng mà đôi khi được gọi một cách vô lý là bệnh cơ tim thứ phát. Sinh thiết cơ tim hỗ trợ đáng kể trong việc chẩn đoán phân biệt bệnh cơ tim giãn và bệnh tim, xảy ra với sự gia tăng rõ rệt: 1) với viêm cơ tim lan tỏa nghiêm trọng, thâm nhiễm tế bào của mô đệm được tìm thấy kết hợp với các thay đổi loạn dưỡng và hoại tử trong các tế bào cơ tim; 2) với bệnh amyloidosis nguyên phát xảy ra cùng với tổn thương tim (được gọi là biến thể bệnh tim của bệnh amyloidosis nguyên phát), có một sự lắng đọng đáng kể của amyloid trong mô kẽ của cơ tim, kết hợp với sự teo các sợi cơ; 3) với bệnh hemochromatosis (một bệnh do vi phạm chuyển hóa sắt), sự lắng đọng của sắc tố chứa sắt được tìm thấy trong cơ tim, các mức độ loạn dưỡng và teo sợi cơ khác nhau, và sự tăng sinh của mô liên kết được quan sát thấy. Là một dạng biến thể của DCM, bệnh cơ tim do thuốc và nhiễm độc có thể được xem xét. Nhiều tác nhân có thể gây tổn thương cơ tim: ethanol, emetine, lithium, cadmium, coban, asen, isoproterenol và các chất độc khác. Những thay đổi mô bệnh học trong các mô của cơ tim xuất hiện dưới dạng loạn dưỡng khu trú. Trong tương lai, sự phát triển của các vi mạch xảy ra, kèm theo phản ứng viêm ngoại vi. Ví dụ nổi bật nhất của bệnh cơ tim nhiễm độc là bệnh cơ tim, xảy ra ở những người tiêu thụ quá nhiều bia. Đó là do sự hiện diện của coban trong đó, được thêm vào bia để cải thiện bọt. Coban ngăn chặn hoạt động của vitamin B1, và cũng ảnh hưởng trực tiếp đến sự thay đổi các quá trình enzym của tế bào. Trong giai đoạn cấp tính của bệnh cơ tim coban, ghi nhận sự hiện diện của thoái hóa mỡ và nước, phá hủy các cơ quan nội bào và hoại tử khu trú của các tế bào cơ tim. Trong tương lai, xơ hóa mô kẽ lan tỏa hoặc khu trú nhỏ phát triển, kết quả cuối cùng là hình thành các sẹo rộng. Bệnh cơ tim coban nặng hơn bệnh cơ tim do rượu. Nếu chẩn đoán được thực hiện đúng thời gian, thì bệnh nhân sẽ được chữa khỏi lâm sàng. Bệnh cơ tim do rượu. Ethanol có tác dụng gây độc trực tiếp trên tế bào cơ tim. Ngoài ra, với nhiễm độc ethyl mãn tính, thường thiếu dinh dưỡng. Người ta đã chứng minh rằng rượu dẫn đến sự hình thành các axit béo trong tế bào cơ tim, do đó sẽ thiếu năng lượng cần thiết cho hoạt động của chúng. Acetaldehyde, được hình thành trong quá trình chuyển hóa rượu, có thể là một yếu tố gây độc trực tiếp đến quá trình tổng hợp protein. Nghiện rượu cũng đi kèm với việc kích hoạt các virus tiềm ẩn. Nhìn về mặt vĩ mô, cơ tim bị nhão, giống như đất sét, đôi khi quan sát thấy những vết sẹo nhỏ. Các động mạch vành còn nguyên vẹn. Soi kính hiển vi cho thấy sự kết hợp của loạn dưỡng (ưa nước và mỡ), teo và phì đại các tế bào cơ tim, có thể có các ổ ly giải tế bào cơ tim và xơ cứng. Các vùng bị ảnh hưởng của cơ tim tương phản với những vùng không thay đổi. Kiểm tra bằng kính hiển vi điện tử của các mẫu sinh thiết tim cho thấy sự giãn nở dạng nang của lưới cơ chất và hệ thống T của tế bào cơ tim, đây là đặc điểm của bệnh cơ tim do rượu. Các biến chứng của bệnh cơ tim do rượu - đột tử do rung thất hoặc suy tim mãn tính, hội chứng huyết khối tắc mạch. Điều trị. Điều trị bệnh cơ tim là một nhiệm vụ khó khăn vì nguyên nhân cụ thể khiến chúng xuất hiện vẫn chưa được biết. Nguyên tắc chung của điều trị DCM không khác biệt đáng kể so với điều trị suy tim mạn tính. Trong trường hợp DCM thứ phát, bệnh trước đó (bệnh van tim, v.v.) sẽ được điều trị bổ sung và thực hiện mọi biện pháp để loại bỏ nguyên nhân gây ra DCM. Về bản chất, chúng ta có thể nói về việc điều trị bệnh nhân bị bệnh cơ tim chỉ khi các dấu hiệu lâm sàng xuất hiện. Trong suy tim, glycosid trợ tim không hiệu quả. Bệnh nhân nhanh chóng xuất hiện tình trạng không dung nạp thuốc (nhiễm độc glycoside), do đó cần sử dụng các loại glycoside đào thải nhanh ra khỏi cơ thể (strophanthin, isolanide). Thuốc giãn mạch ngoại vi khá hiệu quả, đặc biệt khi dùng đồng thời hội chứng đau thắt ngực (nitrong, duy trì, nitrosorbide). Những loại thuốc này nên được chỉ định cho những trường hợp suy tim nặng, khó điều trị bằng glycosid và thuốc lợi tiểu. Với hội chứng đau thắt ngực, cần phải sử dụng thuốc chống đau thắt ngực, tốt nhất là nitrat kéo dài (duy trì lâu dài, nitrat, nitrosorbide). Adrenoblockers có hiệu quả (chúng được kê đơn trong trường hợp không có dấu hiệu suy tim). Trong số các phương pháp phẫu thuật điều trị DCMP hiện đại, hiệu quả nhất là ghép tim (cấy ghép). Tuy nhiên, khả năng thực hiện hoạt động này bị hạn chế đáng kể. Vì lý do này, để thay thế cho việc ghép tim trong điều trị hiện đại, để tăng tuổi thọ cho bệnh nhân DCMP, phẫu thuật tái tạo đã được phát triển và đang được thực hiện, nhằm loại bỏ tình trạng suy van tim hai lá và van ba lá. Hoạt động loại bỏ sự suy giảm của các van này cho phép một thời gian để "làm chậm" sự khởi phát của giai đoạn cuối cùng của bệnh. Một phương pháp thay thế khác cho việc cấy ghép tim ở bệnh nhân DCM là cắt bỏ một phần tâm thất trái để giảm kích thước của nó (phẫu thuật Baptiste). Cách đây không lâu, để điều trị cho bệnh nhân DCMP, các mô hình máy điều hòa nhịp tim đặc biệt đã được phát triển, chúng cho phép bạn làm cho hoạt động của tâm thất của tim đồng bộ. Điều này dẫn đến sự cải thiện trong việc đổ đầy máu vào tâm thất của tim và tăng chức năng bơm máu của tim. Một vấn đề riêng biệt cần được xem xét là DCM ở trẻ em, đó là 5-10 trường hợp trên 100 trẻ mỗi năm. Đáng lưu ý là bệnh có thể phát triển ở nhiều lứa tuổi khác nhau, kể cả trẻ sơ sinh. Dữ liệu thu được trong nghiên cứu trên một nhóm trẻ em như sau: bệnh nhân nhận được 000 lựa chọn điều trị (đơn trị liệu với prednisolon, đơn trị liệu với digoxin hoặc prednisolon + digoxin). Hiệu quả của điều trị được đánh giá theo các tiêu chí: nhịp tim được xác định trước và sau điều trị, nhịp hô hấp, tình trạng phân suất tống máu và phân suất co bóp. Phân tích các kết quả thu được cho thấy hiệu quả lớn nhất trong điều trị bệnh cơ tim giãn ở trẻ nhỏ khi kết hợp corticosteroid và glycosid (prednisolon và digoxin). Sau khi hoàn thành đợt điều trị chính (prednisolon 3 mg / kg mỗi ngày trong 2 ngày, digoxin), nhịp tim giảm rõ rệt, giảm khó thở. Trong bối cảnh đơn trị liệu với prednisolone, nhịp tim giảm xảy ra. Đơn trị liệu với digoxin làm giảm nhịp tim nhanh và khó thở. Do không thể kê đơn thuốc kìm tế bào ở trẻ nhỏ, do đã quan sát thấy một số biến chứng điều trị đáng kể, nên sử dụng glycosid tim tác dụng kéo dài kết hợp với hormon corticosteroid trong bệnh cơ tim giãn sẽ tối ưu hơn trong khoa nhi. Phòng ngừa. Phòng ngừa DCM bao gồm tránh uống rượu, cocaine và theo dõi cẩn thận các thông số tim trong quá trình hóa trị khối u. Nó rất hữu ích để làm cứng cơ thể ngay từ khi còn nhỏ. Việc kiêng hoàn toàn rượu trong DCM có cồn giúp cải thiện sức co bóp của tim và có thể loại bỏ nhu cầu ghép tim. Thực tế là trong hầu hết các trường hợp, chẩn đoán xảy ra ở giai đoạn suy tim cũng có thể dẫn đến kết quả tiêu cực trong điều trị. Chẩn đoán sớm bệnh cơ tim giãn có thể được thực hiện bằng siêu âm tim ngẫu nhiên (sàng lọc), được thực hiện trong đợt khám sức khỏe hàng năm, cũng như khi kiểm tra những người có gánh nặng di truyền bởi bệnh này. Chính trong trường hợp này, có thể tăng hiệu quả điều trị DCM bằng thuốc. KIẾN TRÚC № 3. Các bệnh về hệ tim mạch. Bệnh cơ tim phì đại Bệnh cơ tim phì đại (HCM) là một bệnh không phải mạch vành của cơ tim thất (chủ yếu là bên trái), được đặc trưng bởi sự phì đại lớn của các bức tường của chúng với sự nhô ra của vách ngăn liên thất (IVS) vào khoang của tâm thất phải, có thể dày lên đáng kể. , giảm thể tích bên trong tâm thất, bình thường hoặc tăng sức co bóp của cơ tâm thất và suy giảm khả năng thư giãn (rối loạn chức năng tâm trương). Phổ biến nhất là phì đại vách ngăn liên thất cô lập (hẹp eo động mạch chủ phì đại cô lập - IHSS) hoặc phần đỉnh của tâm thất. Phân loại. Phân loại HCM theo vị trí phì đại (E. D. Wigle và cộng sự, 1985 có bổ sung). I. Phì đại LV. 1) Phì đại không đối xứng, trong đó xảy ra phì đại cơ tim của từng thành hoặc từng đoạn của tâm thất (bao gồm phì đại IVS - 90% có hoặc không có tắc nghẽn đường ra của tâm thất trái, giữa thất - 1%, phì đại đỉnh của thất trái - 3%, phì đại thành tự do thất trái và phần sau của IVS - 1%). 2) Phì đại đối xứng (đồng tâm) của tâm thất trái, khi phì đại cơ tim kéo dài đến tất cả các thành của tâm thất, xảy ra trong 5% trường hợp. II. Sự phì đại của tuyến tụy. Trong trường hợp phì đại cơ tim ngăn cản dòng chảy bình thường của máu từ tâm thất của tim, chúng nói lên một dạng tắc nghẽn HCM. Trong các trường hợp khác, HCM là không cản trở. Nguyên nhân. Bệnh có thể là bẩm sinh hoặc mắc phải. HCM bẩm sinh được di truyền theo kiểu gen trội. Trong cùng một họ, có thể quan sát thấy nhiều dạng và biến thể khác nhau của HCM. Thông thường, phì đại không đối xứng của vách liên thất là do di truyền. Dạng HCM mắc phải xảy ra ở bệnh nhân cao tuổi có tiền sử tăng huyết áp động mạch. Tỷ lệ hiện mắc là 0,02-0,05%. Các lý do cho sự phát triển của HCM bị mua lại không được hiểu đầy đủ. Theo một trong những giả thuyết được đề xuất, những người mắc phải HCM trong giai đoạn trước khi sinh phát triển một khiếm khuyết trong các thụ thể adrenergic của tim liên quan đến điều hòa hoạt động của tim, đặc biệt là nhịp tim. Kết quả là, sự nhạy cảm với norepinephrine và các hormone tương tự, làm tăng nhịp tim, tăng lên đáng kể, ảnh hưởng đến sự phát triển phì đại cơ tim ở họ, và cuối cùng là HCM. Hình ảnh bệnh lý. Sự sắp xếp mất phương hướng, không chính xác, hỗn loạn của các tế bào cơ tim và sợi cơ trong tế bào cơ tim, xơ hóa cơ tim là vi phạm cấu trúc cơ tim. Sinh bệnh học. Rối loạn huyết động phát sinh do chức năng tâm trương của tim bị suy giảm. Trong thời kỳ tâm trương, lượng máu chảy vào tâm thất không đủ (đặc biệt là bên trái) do mật độ và độ cứng của chúng, dẫn đến áp lực cuối tâm trương tăng nhanh. Cả độ cứng cơ tim tăng và áp lực trong tâm thất tăng đều làm cho lượng máu tống ra khỏi tâm thất ít hơn trong thời kỳ tâm thu. Để cung cấp đầy đủ oxy đến các cơ quan và mô của cơ thể (với hoạt động bình thường của hệ thống tim mạch), để thực hiện bất kỳ tải trọng nào, việc giải phóng máu từ tim phải tăng lên. Theo đó, để đáp ứng với tải trọng, nhịp tim tăng lên. Với sự phát triển của HCM, việc bơm đầy máu vào tim cũng bị ảnh hưởng khi nghỉ ngơi, và nhịp tim tăng lên trong thời gian vận động lại càng bị ảnh hưởng tiêu cực hơn. Kết quả của điều này là không có sự gia tăng đầy đủ chức năng bơm máu của tim khi tập thể dục ở HCM. Hoạt động thể chất ở HCM ảnh hưởng đến sự gia tăng áp lực trong não thất, dẫn đến tăng áp lực trong tâm nhĩ trái nằm ở phía trên, cũng như trong các mạch của tuần hoàn nhỏ (phổi). Trong những điều kiện này, chức năng và phì đại tâm nhĩ trái phát triển, và sau đó - tăng áp động mạch phổi ("thụ động"). Kết quả là, khó thở xảy ra, tỷ lệ thuận với mức độ tải. Vì trong quá trình tập thể dục, lượng máu từ tâm thất trái không tương ứng với sự gia tăng tải trọng, lưu lượng máu trong động mạch vành nuôi cơ tim bắt đầu bị ảnh hưởng. Đóng một vai trò quan trọng và thực tế là ở HCM có sự khác biệt giữa khối lượng cơ tim phì đại đáng kể và khả năng cung cấp máu mạch vành, vẫn giống như ở người khỏe mạnh. Lưu lượng máu qua động mạch vành giảm dẫn đến xuất hiện những cơn đau thắt ngực ở giữa và nửa ngực trái, tỏa xuống cánh tay trái, dưới xương bả vai trái. Giống như khó thở, cơn đau thắt ngực xảy ra do gắng sức. Trong một số trường hợp HCM khi vận động, lượng máu cung cấp cho não cũng bị suy giảm dẫn đến tình trạng ngất xỉu. Cần lưu ý rằng để giảm sự gia tăng áp lực trong não thất khi tập thể dục, có một cơ chế bù trừ, hoạt động dựa trên thực tế là khoang của tâm nhĩ trái mở rộng và độ dày của các bức tường của nó tăng lên. Kết quả là, có một lượng máu bổ sung vào tâm thất trái khi tập thể dục. Tuy nhiên, đây chỉ là sự bù đắp tạm thời do dự trữ của tâm nhĩ trái như một "máy bơm" là không đáng kể, và sự mở rộng đáng kể của khoang của tâm nhĩ trái dẫn đến sự phát triển của rung nhĩ. Ảnh lâm sàng. HCM được đặc trưng bởi rất nhiều triệu chứng, gây ra chẩn đoán sai. Sự hiện diện và thời điểm khiếu nại ở HCM chủ yếu được xác định bởi 2 yếu tố: hình thức HCM và vị trí tổn thương. Buồng tim mạnh nhất là tâm thất trái, do đó, khi thành cơ tim phì đại, những phàn nàn có thể không xuất hiện trong một thời gian dài. Tổn thương đơn độc ở tâm thất phải của tim là cực kỳ hiếm. Ở dạng HCM không tắc nghẽn, khi không có gì cản trở dòng chảy của máu từ tâm thất, bệnh nhân có thể không có bất kỳ phàn nàn nào. Đôi khi có thể có khó thở (khi gắng sức đáng kể), gián đoạn hoạt động của tim, cũng như nhịp tim không đều. Trong dạng tắc nghẽn HCM, sự tống máu từ tim khi vận động giảm đáng kể do sự hiện diện của vật cản đường ra của máu từ tâm thất. Trong trường hợp này, khó thở khi gắng sức, đau thắt ngực và ngất xỉu là những phàn nàn điển hình. Căn bệnh này được đặc trưng bởi sự tiến triển chậm của các khiếu nại kể từ thời điểm khởi phát. Do sự giống nhau của các phàn nàn (đau ở vùng tim và sau xương ức) và dữ liệu nghiên cứu (tiếng thổi tâm thu dữ dội), bệnh tim thấp và bệnh tim mạch vành thường bị chẩn đoán sai. Hình ảnh lâm sàng của HCM là: 1) dấu hiệu phì đại cơ tim thất (chủ yếu là bên trái); 2) dấu hiệu của chức năng tâm thất tâm trương không đủ; 3) các dấu hiệu thay đổi của tắc nghẽn đường ra thất trái. Chẩn đoán. Trong quá trình tìm kiếm chẩn đoán, quan trọng nhất là phát hiện tiếng thổi tâm thu, mạch thay đổi và xung đỉnh lệch. Hình ảnh nghe tim ở bệnh nhân HCM tắc nghẽn có một số đặc điểm: âm cực lớn của tiếng thổi tâm thu (tiếng thổi tống máu) được xác định ở điểm Botkin và ở đỉnh tim, mức độ nặng của tiếng thổi tỷ lệ thuận với mức độ tắc nghẽn, sự tăng cường của nó xảy ra khi bệnh nhân đứng lên đột ngột, cũng như trong quá trình kiểm tra Valsalva; Âm điệu II luôn được giữ nguyên; tiếng ồn không được thực hiện trên các mạch cổ. Mạch thường cao và nhanh. Điều này là do không có sự thu hẹp trong các đường đi ra từ tâm thất trái khi bắt đầu thì tâm thu, nhưng sau đó, với sự co thắt mạnh mẽ của các cơ, sự thu hẹp "chức năng" của các đường ra xuất hiện, do đó mạch sóng giảm sớm. Nhịp đỉnh trong khoảng 1/3 số trường hợp có tính chất “kép”: lúc đầu khi sờ, người ta cảm thấy tiếng thổi do tâm nhĩ trái co lại, sau đó do tâm thất trái co lại. Để thuận tiện cho việc xác định tính chất này của nhịp đỉnh, tốt nhất nên tiến hành sờ nắn khi bệnh nhân nằm nghiêng về bên trái. Đối với chẩn đoán HCM, dữ liệu siêu âm tim có tầm quan trọng lớn nhất, cho phép làm rõ các đặc điểm giải phẫu của bệnh, mức độ nặng của phì đại cơ tim, tắc nghẽn đường ra của thất trái. Các dấu hiệu sau được tiết lộ: phì đại không đối xứng của IVS, rõ ràng hơn ở XNUMX/XNUMX trên, giảm vận động của nó; tâm thu chuyển động của lá trước của van hai lá theo hướng ra trước; sự tiếp xúc của lá trước của van hai lá với IVS trong tâm trương. Các dấu hiệu không đặc hiệu là: phì đại tâm nhĩ trái, phì đại thành sau tâm thất trái, giảm tốc độ trung bình của vỏ tâm trương của lá trước van hai lá. Trên điện tâm đồ, bất kỳ thay đổi cụ thể nào chỉ được tìm thấy khi phì đại thất trái phát triển đầy đủ. Bằng cách ghi lại điện tâm đồ trong 24 giờ (theo dõi Holter), các rối loạn nhịp tim hiện có sẽ được phát hiện. Kiểm tra điện tâm đồ với một hoạt động thể chất theo liều lượng sử dụng máy đo tốc độ xe đạp hoặc máy chạy bộ cho phép bạn đánh giá mức độ nghiêm trọng của các triệu chứng của bệnh, tiên lượng của bệnh và phát triển phương pháp điều trị thích hợp. Sự phì đại biệt lập của IVS gây ra sự gia tăng biên độ của sóng Q trong chuyển đạo ngực trái (V5-6), làm phức tạp chẩn đoán phân biệt với thay đổi khu trú do nhồi máu cơ tim. Tuy nhiên, độ rộng nhỏ của sóng Q cho phép loại trừ nhồi máu cơ tim. Trong quá trình phát triển quá tải huyết động của tâm nhĩ trái, điện tâm đồ có thể cho thấy dấu hiệu phì đại tâm nhĩ trái: sóng P mở rộng hơn 0,10 s, tăng trong biên độ của nó, sự xuất hiện của sóng P hai pha trong đạo trình V1 với giai đoạn thứ hai tăng về biên độ và thời gian. Chẩn đoán bằng tia X chỉ quan trọng trong giai đoạn tiến triển của bệnh, khi sự gia tăng của tâm thất trái và tâm nhĩ trái, sự mở rộng của phần đi xuống của động mạch chủ có thể được xác định. Trên điện tâm đồ, biên độ của âm I và II được bảo toàn, đây là một dấu hiệu phân biệt của HCM với hẹp lỗ động mạch chủ và cũng phát hiện được tiếng thổi tâm thu với mức độ nặng nhẹ khác nhau. Phương pháp nghiên cứu xâm lấn (thăm dò các phần bên trái của tim, chụp mạch cản quang) hiện không bắt buộc, vì siêu âm tim cung cấp thông tin khá đáng tin cậy để chẩn đoán. Tuy nhiên, đôi khi các phương pháp này được sử dụng trong các trường hợp gây tranh cãi để làm rõ chẩn đoán hoặc trong việc chuẩn bị cho bệnh nhân phẫu thuật. Thăm dò tim được sử dụng dưới sự kiểm soát của truyền hình X-quang. Kỹ thuật thực hiện phương pháp: bằng cách chọc thủng một động mạch lớn dưới gây tê cục bộ cùng với việc đưa thêm một ống thông đặc biệt vào trong khoang tim, người ta đo gradient áp lực (chênh lệch) giữa tâm thất trái và động mạch chủ xuất phát từ nó. Thông thường, độ dốc này không nên. Tuy nhiên, với HCM, có sự chênh lệch áp suất giữa tâm thất trái và động mạch chủ từ 50 đến 150 mm Hg. Art., Sự gia tăng áp suất cuối tâm trương trong khoang của tâm thất trái lên đến 18 mm Hg. Mỹ thuật. Gradient áp suất giảm sau khi sử dụng thuốc chẹn β. Ngoài ra, trong quá trình nghe tim, một chất cản quang được tiêm vào khoang của tâm thất (chụp não thất) để nghiên cứu các đặc điểm giải phẫu của nó. Ở một số bệnh nhân (theo quy định, đây là những người trên 40 tuổi), chụp động mạch vành (chụp động mạch vành) được sử dụng đồng thời trước khi phẫu thuật tim để làm rõ căn nguyên của cơn đau thắt ngực và loại trừ bệnh mạch vành đồng thời. Điều trị. Cơ sở điều trị bằng thuốc cho HCM là thuốc cải thiện lưu lượng máu đến tâm thất trong tâm trương. Những loại thuốc này là nhóm thuốc chẹn beta (anaprilin, atenolol, metoprolol và propranolol, 160-320 mg/ngày, v.v.) và nhóm thuốc đối kháng ion canxi (verapamil, nhưng phải thận trọng). Novokinamid và disopyramide cũng làm giảm nhịp tim và có tác dụng chống loạn nhịp. Khi bắt đầu điều trị, liều lượng nhỏ của các loại thuốc này được sử dụng, sau đó liều lượng tăng dần đến mức tối đa mà bệnh nhân có thể dung nạp được. Thuốc chẹn β được sử dụng thận trọng trong bệnh đái tháo đường, hen phế quản và một số bệnh khác. Khi điều trị bằng các loại thuốc này, cần theo dõi liên tục huyết áp và nhịp mạch. Nguy hiểm là áp suất giảm xuống dưới 90/60 mm Hg. Mỹ thuật. và nhịp tim dưới 55 mỗi phút. Nếu một bệnh nhân bị rối loạn nhịp tim nguy hiểm mà không thể điều trị bằng thuốc chẹn β hoặc thuốc đối kháng ion canxi, thì các loại thuốc chống loạn nhịp tim khác sẽ được sử dụng bổ sung để điều trị cho những bệnh nhân đó. Việc chỉ định thuốc chống đông máu được khuyến cáo đối với rối loạn nhịp tim kịch phát và rung nhĩ, cũng như khi có cục máu đông trong buồng tim (warfarin, v.v.). Trong thời gian điều trị bằng các thuốc này, cần theo dõi thường xuyên một số chỉ số của hệ thống đông máu. Với quá liều đáng kể của thuốc chống đông máu, có thể xuất huyết bên ngoài (mũi, tử cung, v.v.) và bên trong (tụ máu, v.v.). Điều trị phẫu thuật được thực hiện ở bệnh nhân HCM tắc nghẽn khi điều trị nội khoa không hiệu quả hoặc khi gradient giữa tâm thất trái và động mạch chủ trên 30 mm Hg. Mỹ thuật. (phẫu thuật cắt bỏ cơ hoặc cắt bỏ cơ được thực hiện - cắt bỏ hoặc cắt bỏ một phần cơ tim phì đại của tâm thất trái). Thay van hai lá và cắt bỏ IVS không phẫu thuật cũng được thực hiện. Phòng ngừa. Tất cả bệnh nhân HCM, đặc biệt là những người có dạng tắc nghẽn, đều bị chống chỉ định tham gia các môn thể thao có thể làm tăng đáng kể hoạt động thể chất trong một thời gian ngắn (điền kinh, bóng đá, khúc côn cầu). Phòng ngừa bệnh nằm ở chẩn đoán sớm, giúp bắt đầu điều trị bệnh sớm và ngăn ngừa sự phát triển của bệnh phì đại cơ tim nghiêm trọng. Bắt buộc phải thực hiện siêu âm tim ở người thân di truyền của bệnh nhân. Sàng lọc ECG và EchoCG, được thực hiện trong quá trình khám sức khỏe hàng năm, cũng rất quan trọng để chẩn đoán. Ở những bệnh nhân HCM tắc nghẽn, cần ngăn ngừa viêm nội tâm mạc nhiễm trùng (dự phòng bằng kháng sinh, v.v.), vì sự hiện diện của tắc nghẽn sẽ tạo điều kiện cho tình trạng đe dọa tính mạng này phát triển. KIẾN TRÚC № 4. Các bệnh về hệ tim mạch. Bệnh cơ tim hạn chế Bệnh cơ tim hạn chế (RCMP) - (từ từ tiếng Latinh limittio - "hạn chế") - một nhóm các bệnh về cơ tim và nội tâm mạc, trong đó, do xơ hóa rõ rệt và mất tính đàn hồi, do nhiều lý do, có một hạn chế cố định trong việc trám răng của tâm thất trong thì tâm trương. Việc làm đầy não thất được thực hiện trong giai đoạn làm đầy sớm, sau đó là ổn định áp lực não thất. Căn bệnh này kèm theo lượng máu cung cấp cho tim không đủ, càng dẫn đến suy tim mãn tính. Bệnh cơ tim hạn chế là bệnh ít được nghiên cứu nhất và ít phổ biến nhất trong tất cả các bệnh cơ tim. RCMP bao gồm: Viêm nội tâm mạc xơ hóa thành Lefler (gặp ở các nước có khí hậu ôn hòa, được mô tả bởi W. Loffler và cộng sự, 1936) và xơ hóa nội tâm mạc (gặp ở các nước nhiệt đới châu Phi, được mô tả bởi D. Bedford và E. Konstman). Trước đây, chúng được coi là hai quá trình bệnh lý độc lập. Tuy nhiên, hình ảnh bệnh lý ở các bệnh này khác nhau rất ít. Nguyên nhân của RCM. RCM nguyên phát rất hiếm và nguyên nhân duy nhất được chứng minh về sự xuất hiện của nó là hội chứng tăng bạch cầu ái toan (bệnh Leffler, viêm nội tâm mạc xơ hóa vùng đỉnh của Leffler). Bệnh xảy ra chủ yếu ở nam giới trong độ tuổi 30-40. Với hội chứng tăng bạch cầu ái toan, tình trạng viêm nội tâm mạc xảy ra, theo thời gian lên đến đỉnh điểm là nội tâm mạc bị nén đáng kể và sự bám dính thô của nó với cơ tim lân cận, dẫn đến khả năng giãn nở của cơ tim giảm mạnh. Hội chứng Lefler còn được đặc trưng bởi tình trạng tăng bạch cầu ái toan kéo dài từ 6 tháng trở lên (1500 bạch cầu ái toan trên 1 mm).3), tổn thương các cơ quan nội tạng (gan, thận, phổi, tủy xương). Trong phần lớn các trường hợp, nguồn gốc của RCMP là thứ phát, do các lý do khác, trong đó phổ biến nhất là: 1) bệnh amyloidosis - một căn bệnh liên quan đến sự vi phạm chuyển hóa protein trong cơ thể; Đồng thời, trong các mô của các cơ quan khác nhau, một protein bất thường (amyloid) được hình thành và lắng đọng với số lượng lớn; khi tim bị tổn thương, amyloid làm giảm khả năng co bóp và kéo dài của tim; 2) hemochromatosis - vi phạm chuyển hóa sắt trong cơ thể, kèm theo hàm lượng sắt trong máu tăng lên, lượng sắt dư thừa được lắng đọng trong nhiều cơ quan và mô, bao gồm cả cơ tim, do đó gây giảm khả năng mở rộng của nó; 3) bệnh sarcoidosis - một bệnh chưa rõ nguyên nhân, đặc trưng bởi sự hình thành các cụm tế bào (u hạt) trong các cơ quan và mô; phổi, gan, hạch bạch huyết và lá lách thường bị ảnh hưởng nhất; và phát triển u hạt trong cơ tim dẫn đến giảm khả năng mở rộng của nó; 4) các bệnh nội tâm mạc (xơ hóa màng trong tim, xơ hóa màng trong tim, v.v.), khi có sự dày lên và chèn ép đáng kể của nội tâm mạc, điều này cũng dẫn đến hạn chế rõ rệt về khả năng mở rộng của cơ tim. Đặc biệt, bệnh xơ hóa màng trong tim chỉ có thể xảy ra ở trẻ sơ sinh; bệnh này không tương thích với cuộc sống do sự phát triển sớm của bệnh suy tim nặng. Sinh bệnh học. Với RCM, độ giãn nở của cơ tim bị ảnh hưởng vì nhiều lý do. Kết quả là lượng máu đổ vào tâm thất giảm và áp lực trong não thất tăng lên đáng kể. Tuy nhiên, không giống như HCM, khả năng phát triển phì đại cơ tim bù trong bệnh cơ tim hạn chế là rất nhỏ. Do đó, sau một thời gian, tuần hoàn phổi bị ứ đọng và chức năng bơm của tim giảm, dẫn đến tình trạng ứ nước dần dần trong cơ thể, phát triển tình trạng sưng tấy dai dẳng ở chân, gan to và cổ trướng. Nếu sự chèn ép của nội tâm mạc kéo dài đến các van nhĩ thất (hai lá và ba lá), điều này sẽ trở nên trầm trọng hơn do sự phát triển của tình trạng thiểu năng của chúng, và cũng dẫn đến huyết khối trong các khoang tim do giảm sức co bóp và khả năng mở rộng của chúng. Sự lây lan của các mảnh vỡ của các cục máu đông này theo dòng máu có thể gây ra huyết khối và tắc nghẽn các mạch lớn, nhồi máu cơ tim của các cơ quan nội tạng. Với sự lây lan của các tạp chất bệnh lý của cơ tim đến khu vực của hệ thống dẫn truyền của tim, các vi phạm khác nhau về dẫn truyền xung động của tim có thể xuất hiện, kèm theo sự phát triển của các phong tỏa. Với RCMP, các dạng rối loạn nhịp tim khác nhau cũng thường được quan sát thấy. Dựa vào những điều trên, chúng ta có thể kết luận rằng bệnh theo quan điểm di truyền bệnh tiến triển theo 3 giai đoạn. Giai đoạn I - hoại tử - thâm nhiễm bạch cầu ái toan của cơ tim và các cơ quan khác. Giai đoạn II - huyết khối - sự hình thành các cục máu đông trong các khoang của tâm thất trái và phải, sự phát triển của các biến chứng huyết khối và dày dần nội tâm mạc chủ yếu ở vùng đỉnh và gần van nhĩ thất. Giai đoạn III - xơ, được đặc trưng bởi sự dày lên của nội tâm mạc lên đến vài mm, xơ hóa cơ tim được biểu hiện - chủ yếu là các khu vực dưới nội tâm mạc. Khoang bị xóa một phần do huyết khối có tổ chức, xơ hóa của van hai lá, trào ngược van hai lá được ghi nhận. Giãn tâm nhĩ rõ rệt. Rối loạn chức năng tâm trương hạn chế được quan sát thấy. Ảnh lâm sàng. Biểu hiện của bệnh rất đa dạng và được xác định bằng triệu chứng rối loạn tuần hoàn theo vòng tròn nhỏ hay lớn (tùy theo tổn thương chủ yếu ở tâm thất phải hay trái). Sự phàn nàn có thể không có hoặc có thể do tắc nghẽn tuần hoàn phổi hoặc toàn thân. Bệnh nhân thường phàn nàn về khó thở, xuất hiện đầu tiên khi vận động và khi bệnh tiến triển, khó thở xuất hiện khi nghỉ ngơi. Do giảm chức năng bơm máu của tim, bệnh nhân kêu mệt mỏi và kém khả năng chịu tải. Theo thời gian, chân phù nề, gan to và cổ chướng ở bụng cùng với nhau. Theo chu kỳ, nhịp tim không đều xuất hiện và với sự phát triển của các cơn phong tỏa dai dẳng, có thể bị ngất xỉu. Giai đoạn đầu của sự phát triển của bệnh (hoại tử) được đặc trưng bởi sự xuất hiện của sốt, sụt cân, ho, phát ban trên da và nhịp tim nhanh. Chẩn đoán. Nhận biết RCM là vô cùng khó khăn. Người ta chỉ có thể tự tin nói về bệnh lý này sau khi loại trừ một số bệnh tương tự (chẳng hạn như viêm cơ tim vô căn thuộc loại Abramov-Fiedler, viêm màng ngoài tim tiết dịch, dị tật van tim). Khi kiểm tra bệnh nhân bị RCMP, người ta tìm thấy các triệu chứng đặc trưng của suy tim sung huyết (phù, gan to và cổ trướng), cũng như nhịp đập rõ rệt của các tĩnh mạch cổ. Sau đó là do khó cung cấp máu cho tim do khả năng co giãn của cơ tim kém. Trong quá trình nghe tim thai, việc phát hiện tim to, tiếng thổi cuối tâm thu mềm và âm III lớn sớm (do tâm thất đổ đầy nhanh trong thời kỳ tâm trương) là rất quan trọng. Tiếng thổi ở tim cũng được phát hiện ở bệnh nhân suy van nhĩ thất. Một nghiên cứu điện tâm đồ cho thấy sự phì đại vừa phải của cơ tâm thất, cũng như các rối loạn nhịp và dẫn truyền khác nhau của xung tim, những thay đổi không đặc hiệu của sóng T trên điện tâm đồ. Siêu âm tim là một trong những phương pháp thông tin nhất để chẩn đoán bệnh, với sự trợ giúp của nó, nội tâm mạc dày lên, thay đổi tính chất của việc đổ đầy tâm thất của tim, giảm chức năng bơm máu của tim, cử động nhanh. của lá trước của van hai lá trong thời kỳ tâm trương và một chuyển động sớm nhanh chóng của thành sau của tâm thất trái ra ngoài được phát hiện. Chụp cộng hưởng từ cho phép bạn thu được thông tin về giải phẫu của tim, xác định các ổ bệnh lý trong cơ tim và đo độ dày của nội tâm mạc. Khi kiểm tra các thông số về huyết động học trung tâm, áp suất làm đầy tăng lên ở cả hai tâm thất được xác định và áp suất cuối cùng ở bên trái vượt quá áp suất ở tâm thất phải. Chụp não thất cho thấy tâm thất trái tăng co, các đường viền nhẵn của thành, đôi khi có khuyết lõm ở đỉnh (bằng chứng của sự tắt nghẽn). Trong một số trường hợp, chỗ lõm ở vùng cơ nhú được xác định. Có dấu hiệu của suy van tim, cụ thể là van hai lá hoặc van ba lá. Chẩn đoán phân biệt. Trong chẩn đoán phân biệt RCM, điều rất quan trọng là phải tính đến sự giống nhau của bệnh với các biểu hiện bên ngoài với viêm màng ngoài tim co thắt, nhưng phương pháp điều trị các bệnh này lại hoàn toàn trái ngược nhau. Sinh thiết cơ tim và nội tâm mạc trong tử cung thường được sử dụng đồng thời với thăm dò tim, cho phép có nhiều thông tin hơn để làm rõ bản chất của bệnh và điều trị thêm. Trong những trường hợp cực kỳ hiếm gặp, khi các phương pháp chẩn đoán trên không cho phép phân biệt RCM với viêm màng ngoài tim co thắt, việc kiểm tra trực tiếp màng ngoài tim được thực hiện trên bàn mổ. Tất cả bệnh nhân RCMP cần được khám toàn diện về lâm sàng, sinh hóa và kiểm tra bổ sung để xác định nguyên nhân không do tim của bệnh. Điều trị. Việc điều trị bệnh gặp nhiều khó khăn đáng kể. Hầu hết các loại thuốc dùng để điều trị suy tim có thể không mang lại kết quả như mong muốn do đặc điểm của bệnh là không thể cải thiện đáng kể độ giãn nở của cơ tim (trong một số trường hợp, thuốc đối kháng ion canxi được kê đơn). cho những mục đích này). Thuốc lợi tiểu (aldactone) được sử dụng để loại bỏ chất lỏng dư thừa trong cơ thể. Để loại bỏ các rối loạn dẫn truyền dai dẳng, có thể cần phải lắp đặt (cấy ghép) máy điều hòa nhịp tim vĩnh viễn. Điều này là do các bệnh như sarcoidosis và hemochromatosis, dẫn đến sự phát triển của RCMP thứ cấp, họ phải tự điều trị. Trong điều trị bệnh sarcoidosis, các loại thuốc nội tiết tố (prednisolone, v.v.) được sử dụng, và trong bệnh huyết sắc tố, thường xuyên đi ngoài ra máu (để giảm nồng độ sắt trong cơ thể). Điều trị bệnh amyloidosis cơ tim phụ thuộc trực tiếp vào nguyên nhân gây ra nó. Nên sử dụng các thuốc chống đông máu cho các trường hợp huyết khối trong các buồng tim. Điều trị phẫu thuật được áp dụng trong các trường hợp RCMP do tổn thương nội tâm mạc. Trong quá trình phẫu thuật, nếu có thể, phần nội tâm mạc đã trải qua những thay đổi sẽ được cắt bỏ. Trong một số trường hợp, nếu không có van nhĩ thất, việc phục hình của chúng sẽ được thực hiện. Một số dạng tổn thương cơ tim do amyloid được điều trị bằng ghép tim. Phòng ngừa RCMP. Thật không may, các biện pháp phòng ngừa căn bệnh này còn hạn chế. Chủ yếu, việc xác định sớm các nguyên nhân có thể phòng ngừa được của bệnh amyloidosis, sarcoidosis, hemochromatosis, v.v. là cần thiết. Để đạt được những mục tiêu này, việc khám sức khỏe hàng năm cho người dân là rất quan trọng. BÀI GIẢNG SỐ 5. Các bệnh về hệ tim mạch. Viêm nội tâm mạc nhiễm trùng Viêm nội tâm mạc nhiễm trùng (IE) - một bệnh bao gồm tổn thương loét do polyposis của bộ máy van tim (thường xảy ra với sự phát triển của suy van tim) hoặc nội tâm mạc thành (ít thường xuyên hơn, nội mạc của động mạch chủ hoặc động mạch lớn gần nhất bị ảnh hưởng). Bệnh do các vi sinh vật gây bệnh khác nhau gây ra và kèm theo tổn thương toàn thân của các cơ quan nội tạng (thận, gan, lá lách) trên nền phản ứng bị thay đổi của cơ thể. Cho đến nay, trong các ấn phẩm in khác nhau, các thuật ngữ được sử dụng trước đây "viêm nội tâm mạc nhiễm khuẩn", "viêm nội tâm mạc nhiễm khuẩn kéo dài" có thể được tìm thấy để chỉ quá trình bệnh lý này. Tuy nhiên, thuật ngữ "viêm nội tâm mạc nhiễm trùng" đã thay thế chúng để phản ánh rõ hơn nguyên nhân của bệnh do nhiều loại vi sinh vật gây ra - tác nhân vi khuẩn, rickettsiae, vi rút và nấm. Số bệnh nhân mắc IE ngày càng tăng trên toàn thế giới. Điều này là do sự hiện diện của cái gọi là nhóm nguy cơ (bệnh nhân bị xơ vữa động mạch, thấp khớp, chấn thương van, dị tật tim hoặc van, thông liên thất, hẹp eo động mạch chủ) như một hậu quả của thực tế là nhiễm trùng xảy ra dễ dàng hơn khi bị thay đổi bệnh lý van hoặc màng trong tim. Nguyên nhân. Tác nhân gây bệnh của bệnh thường là nhóm vi sinh vật cầu khuẩn - streptococci (viridans streptococcus trước đây đã được phân lập trong 90% trường hợp), staphylococci (vàng, trắng), enterococcus, phế cầu khuẩn. Trong những năm gần đây, do việc sử dụng rộng rãi kháng sinh, phạm vi vi khuẩn gây bệnh đã thay đổi. Bệnh có thể do vi khuẩn gram âm (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella); bằng chứng đã xuất hiện về vai trò quan trọng của nấm gây bệnh, Sarcinus, Brucella và virus. Bệnh do các mầm bệnh này gây ra nặng hơn, đặc biệt là viêm nội tâm mạc do nhiễm nấm (thường xảy ra do sử dụng kháng sinh không hợp lý). Tuy nhiên, ở một số bệnh nhân, tác nhân gây bệnh thực sự không được phát hiện (tỷ lệ cấy máu âm tính 20-50%). Thông thường, nhiễm trùng xảy ra tại vị trí van giả - cái gọi là IE giả, phát triển chủ yếu trong vòng 2 tháng sau khi phẫu thuật thay van tim. Trong trường hợp này, tác nhân gây bệnh thường có bản chất liên cầu. Do đó, các nguồn lây nhiễm và nhiễm khuẩn huyết trong IE rất khác nhau (phẫu thuật trong khoang miệng, phẫu thuật và quy trình chẩn đoán ở vùng tiết niệu sinh dục, can thiệp phẫu thuật trên hệ thống tim mạch (bao gồm cả thay van), thời gian đặt ống thông trong tĩnh mạch kéo dài, truyền tĩnh mạch thường xuyên và các phương pháp nghiên cứu nội soi, chạy thận nhân tạo mãn tính (shunt động mạch), tiêm thuốc qua đường tĩnh mạch). Có cái gọi là IE nguyên phát, phát triển trên các van còn nguyên vẹn, cũng như IE dựa trên nền tảng của những thay đổi bẩm sinh và mắc phải ở tim và bộ máy van của nó - viêm nội tâm mạc thứ phát. Những thay đổi này giúp phân biệt bệnh nhân thành các nhóm nguy cơ riêng biệt: dị tật tim (bẩm sinh và mắc phải), sa van hai lá, phình động mạch, phình động mạch sau nhồi máu, bệnh lý shunts, tình trạng sau phẫu thuật tim và mạch lớn. Sinh bệnh học. Cơ chế phát triển của IE rất phức tạp và chưa được nghiên cứu đầy đủ, tuy nhiên, có thể xác định được những điểm chính trong sự phát triển của bệnh. Nếu có một trọng điểm nhiễm trùng trong cơ thể dưới ảnh hưởng của miễn dịch dịch thể và tại chỗ (tế bào) bị thay đổi với sự biến đổi của các phản ứng miễn dịch, các yếu tố nội sinh và ngoại sinh khác nhau, nhiễm khuẩn huyết sẽ phát triển. Từ máu, vi sinh vật xâm nhập vào van tim, tạo ra một ổ nhiễm trùng thứ cấp ở đó. Sự cố định và sinh sản của vi sinh vật trên nội tâm mạc được tạo điều kiện thuận lợi bởi một số yếu tố: sự thay đổi trước đó của mô và bề mặt của van, sự hiện diện của các khối huyết khối trên đó, phát sinh dưới ảnh hưởng của tác động gây hại trực tiếp của dòng máu. khi tuần hoàn trong tim của nó thay đổi trong điều kiện của bệnh tim hiện có. Đồng thời, các tế bào máu khác nhau (tiểu cầu, v.v.) “kết dính” với vị trí chấn thương, hình thành các tế bào phát triển giống như các cục băng treo trên van. Những thảm thực vật này trở nên sẵn sàng cho sự lây nhiễm đã xâm nhập vào lớp mạch máu. Sự biến dạng của các van do sự xuất hiện của một gradient áp suất lớn, sự hẹp của lỗ và thay đổi vận tốc dòng máu cũng góp phần đưa các tác nhân lây nhiễm vào nội tâm mạc với sự hình thành tiêu điểm lây nhiễm. Khi một van nguyên vẹn trước đó bị hư hỏng, những thay đổi xảy ra làm phá vỡ các đặc tính bình thường của các phần riêng lẻ của van này (sưng tấy xuất hiện), các quá trình tiết dịch hoặc tăng sinh ("viêm van kẽ" - giai đoạn tiền lâm sàng). Trong sự phát triển của bệnh, giai đoạn III có thể được phân biệt. Giai đoạn I (nhiễm độc - nhiễm độc) diễn ra với các mức độ nhiễm độc nặng nhẹ khác nhau. Có sự phát triển của vi khuẩn, phá hủy các van, dẫn đến sự phát triển của bệnh tim; ở cùng một giai đoạn, một quá trình tổng quát thường xảy ra do sự lây lan theo đường máu - các mảnh vụn hoặc khuẩn lạc của vi sinh vật có thể tách ra khỏi van, đầu mút có thể vỡ ra. Sự tách rời của các mảnh thảm thực vật vi sinh vật có van góp phần đưa các emboli bị nhiễm bệnh vào các bộ phận khác nhau của giường mạch và làm trầm trọng thêm các biểu hiện nhiễm trùng. Các mảnh van hoặc các vi sinh vật lưu thông trong cơ thể theo dòng máu, khi xâm nhập vào não sẽ gây nhồi máu não, kèm theo liệt, liệt và nhiều rối loạn thần kinh khác. Van, đã trải qua quá trình phá hủy, không thể thực hiện chức năng của nó, và sớm bị suy tim phát triển nhanh như chớp. Giai đoạn II - viêm miễn dịch, trong đó các vi sinh vật cố định trên van gây ra hiện tượng tự mẫn cảm kéo dài và tổn thương cơ ức chế đối với các cơ quan và mô của cơ thể (quá trình tổng quát hóa miễn dịch). Trong thời kỳ này, các phức hợp miễn dịch lưu thông trong máu và cố định trong các mô (tim, thận, gan, mạch máu). Các rối loạn miễn dịch và tự miễn dịch gây ra sự phát triển của viêm mạch và viêm nội tạng (viêm thận đơn giản miễn dịch, viêm cơ tim, viêm gan, viêm mao mạch, v.v.). Giai đoạn III - loạn dưỡng - xảy ra với sự tiến triển của quá trình bệnh lý: chức năng của một số cơ quan bị rối loạn, suy tim và thận xảy ra, làm trầm trọng thêm diễn biến của bệnh. Phân loại. Hiện nay, việc phân loại và danh pháp IE được sử dụng, phản ánh dạng lâm sàng, biến thể diễn biến, mức độ hoạt động, giai đoạn bệnh sinh cũng như dạng lâm sàng và hình thái của bệnh (xem Bảng 6). Bảng 6 Phân loại IE
Một sự khác biệt cũng được thực hiện giữa IE hoạt động và không hoạt động (được chữa lành). Ngoài ra còn có một phân loại phẫu thuật, trong đó có: 1) tổn thương giới hạn ở các lá van; 2) tổn thương kéo dài ra ngoài van. IE cấp tính (tiến triển nhanh, phát triển trong vòng 8 - 10 tuần) hiếm gặp, thường xảy ra ở những người trước đó chưa bị bệnh tim và biểu hiện lâm sàng bằng hình ảnh nhiễm trùng huyết nói chung. Với các phương pháp điều trị hiện đại, có thể chuyển sang thể bán cấp. IE bán cấp (thường gặp nhất) kéo dài 3-4 tháng, nếu điều trị bằng thuốc đầy đủ, bệnh có thể thuyên giảm. Tuy nhiên, bệnh có thể tái phát. IE kéo dài kéo dài trong nhiều tháng với các giai đoạn kịch phát và thuyên giảm, nó được đặc trưng bởi các biểu hiện lâm sàng nhẹ, các thông số xét nghiệm nhỏ và rối loạn chung. Bệnh thường đáp ứng tốt với điều trị. Với một diễn tiến không thuận lợi, các biến chứng nặng nề xảy ra, và bệnh nhân tử vong do suy tim tiến triển, nhiễm độc nhiễm trùng ngày càng tăng. Ảnh lâm sàng. Tùy thuộc vào tác nhân gây nhiễm trùng, IE có thể xảy ra đột ngột và phát triển nhanh chóng (Staphylococcus aureus, enterococci) hoặc khởi phát tiềm ẩn (viridans streptococcus). Các biểu hiện của IE được thể hiện dưới dạng hội chứng. 1) Hội chứng thay đổi viêm nhiễm và nhiễm trùng huyết (sốt, ớn lạnh, phát ban xuất huyết, thay đổi các chỉ số máu trong giai đoạn cấp tính: tăng bạch cầu với sự dịch chuyển sang trái, tăng ESR, xuất hiện protein phản ứng C, tăng fibrinogen, α2-globulin. 2) Các hội chứng nhiễm độc nói chung của cơ thể (suy nhược, đổ mồ hôi, nhức đầu, đau cơ và đau khớp, chán ăn, xanh xao trên da có màu tím tái). 3) Hội chứng tổn thương van (hình thành bệnh tim). 4) Hội chứng rối loạn miễn dịch “phòng thí nghiệm” (sự hiện diện của các phức hợp miễn dịch lưu hành trong máu hoặc cố định ở thận, cơ tim, mạch máu; tăng glucaglobulin máu; xuất hiện yếu tố dạng thấp; phát hiện kháng thể kháng mô). 5) Hội chứng biến chứng huyết khối tắc mạch (viêm thận khu trú, nhồi máu cơ tim, lách, ruột, huyết khối tắc mạch ở não, mạch chi dưới, v.v.). 6) Hội chứng tổng quát các tổn thương (viêm cầu thận lan tỏa, viêm cơ tim, viêm gan, viêm mạch,…). Mức độ nghiêm trọng của các hội chứng này là khác nhau. Nó phụ thuộc vào bản chất của quá trình IE, giai đoạn, loại mầm bệnh. Ví dụ, IE do tụ cầu được đặc trưng bởi quá trình hoạt động cao, các triệu chứng nhiễm độc nặng nói chung và sự phát triển của các biến chứng có mủ. Viêm nội tâm mạc do nấm thường đi kèm với tắc các động mạch lớn, đặc biệt là chi dưới. Hình ảnh điển hình của bệnh là đặc trưng của bệnh IE do liên cầu viridans gây ra. Sự khởi phát của bệnh thường liên quan đến nhiễm trùng cấp tính hoặc đợt cấp của nhiễm trùng mãn tính, cũng như với một số thao tác y tế. Đặc biệt đặc trưng là sự kết hợp của sự gia tăng nhiệt độ cơ thể ở nhiều mức độ khác nhau (từ sốt kéo dài đến tình trạng ốm yếu hoặc nhiệt độ bình thường) với ớn lạnh và đổ mồ hôi. Bệnh nhân trình bày các khiếu nại đồng thời do sự hiện diện của quá trình nhiễm trùng và nhiễm độc, cũng như các biến chứng huyết khối tắc mạch của tổn thương tim. Bệnh nhân có thể có tiền sử từng đợt điều trị kháng sinh dài hạn (điều này xảy ra khi IE tái phát ở những bệnh nhân đã điều trị trước đó). Chẩn đoán. Tầm quan trọng lớn nhất để đưa ra chẩn đoán chính xác là việc phát hiện tổn thương van tim bằng những thay đổi trong mô hình nghe tim của các khuyết tật tim đã có từ trước; sự xuất hiện của tiếng ồn "bổ sung". Các tổn thương đặc trưng của da và màng nhầy được bộc lộ: màu da café au lait, xuất huyết, các triệu chứng Hecht's (pinch) và Konchalovsky-Rumpel-Leede (tourniquet) dương tính, cũng như các nút Osler - các nốt dày đặc tăng huyết áp đau đớn trên bề mặt lòng bàn tay và đầu ngón tay , dấu hiệu Lukin-Libman (đốm Lukin) - xuất huyết ở nếp chuyển tiếp của kết mạc. Lách to thường được quan sát thấy trong IE. Giảm cân đáng kể (đôi khi 15-20 kg) là rất điển hình. Trong một số ít trường hợp, viêm màng ngoài tim phát triển (tiếng ồn ma sát màng phổi yếu do lắng đọng fibrin trên màng ngoài tim). Khám thực thể có thể cho thấy huyết áp tăng, cho thấy sự phát triển của viêm cầu thận lan tỏa. Đôi khi xác định được các dấu hiệu rối loạn chức năng của hệ thần kinh trung ương (liệt, tăng vận động, phản xạ bệnh lý, v.v.) do tắc mạch não. Trong trường hợp này, lỗi chẩn đoán phổ biến nhất là đánh giá một hội chứng cụ thể như một biểu hiện của một bệnh độc lập (ví dụ, với các dấu hiệu rõ ràng của tổn thương gan, chẩn đoán viêm gan, v.v.). Tuy nhiên, chẩn đoán IE chủ yếu dựa vào việc phát hiện sớm tác nhân gây bệnh. Đối với điều này, các nghiên cứu trong phòng thí nghiệm và công cụ sau đây được sử dụng. 1) Lấy máu cấy dương tính là dấu hiệu chẩn đoán quan trọng nhất của IE. Phân tích cũng là cần thiết để lựa chọn kháng sinh hiệu quả nhất trong trường hợp này. Ít nhất 2-3 trong số họ được yêu cầu để xác nhận chẩn đoán. Điều quan trọng là kỹ thuật lấy mẫu máu và nuôi cấy, thời điểm cấy (tốt nhất là khi sốt cao), việc sử dụng môi trường đã được làm giàu. 2) Thực hiện NBT (xét nghiệm nitrobluttetrazolium) - chẩn đoán nhiễm trùng do vi khuẩn toàn thân, cho phép phân biệt nhiễm trùng do vi khuẩn với các bệnh viêm nhiễm khác. Phương pháp này dựa trên sự khử thuốc nhuộm NBT hòa tan bởi bạch cầu trung tính thành kết tủa formazan không hòa tan. Nếu số lượng tế bào dương tính với NBT trên 10%, xét nghiệm được coi là dương tính. 3) Xét nghiệm máu lâm sàng để phát hiện các chỉ số giai đoạn cấp tính: tăng ESR đến 50 mm / h hoặc hơn, tăng bạch cầu với sự chuyển dịch công thức bạch cầu sang trái hoặc (ở giai đoạn II) giảm bạch cầu và thiếu máu giảm sắc tố. Giá trị chẩn đoán gắn liền với việc phát hiện mô bào trong máu lấy từ dái tai. Nội dung của họ hơn 6 trong lĩnh vực xem có thể cho thấy có lợi cho IE. Xét nghiệm máu sinh hóa cho thấy sự gia tăng hàm lượng fibrinogen, α2-globulin và α-globulin - lên đến 30 - 40%. 4) Xác định các thay đổi miễn dịch: tăng bạch cầu huyết, phức hợp miễn dịch tuần hoàn, giảm hiệu giá bổ thể, xuất hiện yếu tố thấp khớp (antiglobulin), tăng phản ứng biến đổi nghiêm trọng của tế bào lympho với PHA (phytohemagglutinin) và kháng nguyên vi khuẩn, phát hiện kháng thể kháng mô. 5) Phân tích nước tiểu được thực hiện để làm rõ các tổn thương của các cơ quan và hệ thống khác nhau, khi viêm cầu thận được phát hiện, biểu hiện bằng protein niệu, tiểu cầu và tiểu máu. Sự gia tăng hàm lượng bilirubin, transaminase cho thấy gan bị tổn thương. 6) Dấu hiệu chẩn đoán trực tiếp của IE - sự hiện diện của thảm thực vật trên van tim - được phát hiện bằng siêu âm tim. Do đó, từ toàn bộ các triệu chứng, những triệu chứng chính và bổ sung cần được phân biệt. Các tiêu chí chính để chẩn đoán IE: 1) sốt với nhiệt độ trên 38 ° C kèm theo ớn lạnh; 2) Lukin đốm; 3) Các nốt của Osler; 4) viêm nội tâm mạc trên các van không thay đổi (nguyên phát) hoặc do dị tật tim bẩm sinh và thấp khớp. viêm cơ tim nhiễm trùng; 5) thuyên tắc nhiều huyết khối động mạch, vỡ các túi phình động mạch có xuất huyết; 6) lách to; 7) cấy máu dương tính; 8) tác động tích cực rõ rệt từ việc sử dụng kháng sinh. Tiêu chí bổ sung để chẩn đoán IE: 1) nhiệt độ cơ thể tăng lên đến 38 ° C, lạnh run; 2) xuất huyết trên da; 3) giảm cân nhanh chóng; 4) viêm khớp không đối xứng của các khớp nhỏ của bàn tay, bàn chân; 5) nung chảy; 6) ESR trên 40 mm / h; 7) SRV dương tính mạnh; 8) sự hiện diện của yếu tố dạng thấp; 9) α-globulin trên 25%; 10) tăng hàm lượng các globulin miễn dịch M, E và A. Chẩn đoán phân biệt. Mặc dù thuyên tắc huyết khối thường được quan sát thấy nhiều nhất trong IE, nhưng không nên loại trừ các nguyên nhân khác gây tắc mạch trong động mạch của hệ thống tuần hoàn: nhồi máu cơ tim xuyên thành và phình động mạch tim, viêm cơ tim Abramov-Fiedler vô căn và rung nhĩ có nhiều nguồn gốc khác nhau, nhưng chủ yếu được quan sát thấy với chứng hẹp van tim do thấp khớp. của lỗ nhĩ thất trái. Viêm nội tâm mạc nhiễm trùng và thấp khớp có tầm quan trọng lớn nhất để chẩn đoán phân biệt (Bảng 7). Bảng 7 Tiêu chuẩn chẩn đoán phân biệt đối với viêm nội tâm mạc do thấp khớp và IE kéo dài
Các triệu chứng đặc trưng của IE bao gồm lá lách to. Tuy nhiên, một lá lách to, chắc, không đau được thấy trong bệnh amyloidosis; mềm, không đau cho thấy nó tăng sản nhiễm trùng. Đau được ghi nhận với nhồi máu lá lách, nằm dưới bao. Lá lách có thể là một trong những biểu hiện của tăng áp lực tĩnh mạch cửa trong suy tim phải. Trong trường hợp này, nó được kết hợp với cổ trướng và gan to. Sự gia tăng kích thước gan với IE kéo dài được quan sát thấy khá thường xuyên. Tăng sản nhiễm trùng được đặc trưng bởi sự mở rộng tương đối nhỏ và độ đặc mềm của gan. Có thoái hóa mỡ và cực kỳ hiếm - nhồi máu gan. Thông thường, sự gia tăng của gan có liên quan đến tắc nghẽn tĩnh mạch với suy tim phải. Trong trường hợp không có cổ trướng, tắc nghẽn được ghi nhận hồi cứu bằng sự giảm kích thước gan sau khi điều trị bằng glycosid trợ tim và thuốc lợi tiểu. Điều trị. Điều trị IE nên càng sớm và càng điều trị càng tốt, có tính đến dữ liệu vi khuẩn học. Trước khi thuốc kháng khuẩn được sử dụng rộng rãi trong thực hành y tế, hầu hết bệnh nhân mắc IE đều chết vì nhiễm trùng và các biến chứng của nó. Hơn 80% hiện đã được chữa khỏi thành công. Nhưng gần 20%, việc điều trị bằng thuốc không thành công và họ sớm phát triển bệnh suy tim, gần như không thể điều trị được. Về vấn đề này, nên kết hợp điều trị bảo tồn và phẫu thuật. Để điều trị IE ở mọi lứa tuổi, kháng sinh chủ yếu được sử dụng có tác dụng diệt khuẩn đối với vi sinh vật, tốt nhất là với liều lượng riêng tùy thuộc vào nồng độ của kháng sinh trong máu và mức độ nhạy cảm của mầm bệnh với nó. Thuốc được lựa chọn đầu tiên vẫn là penicillin. Nó có độc tính thấp, cho phép sử dụng lâu dài với liều lượng tương đối cao. Liều hàng ngày - lên đến 20 IU được tiêm tĩnh mạch và tiêm bắp. Tuy nhiên, không thể loại trừ một thực tế là ở những bệnh nhân cao tuổi và cao tuổi, khi điều trị bằng penicillin và các kháng sinh khác với liều lượng cao, tác dụng gây độc cho tim thường được quan sát thấy: xuất hiện hoặc tăng cường suy tim, đau ở tim, nhịp tim nhanh. Khi giảm liều hoặc thay đổi thuốc, các hiện tượng này chấm dứt. Với căn nguyên chưa rõ, điều trị bắt đầu bằng liều cao benzylpenicillin tiêm bắp hoặc tiêm tĩnh mạch lên đến 18-000 đơn vị hoặc hơn, kết hợp với streptomycin đến 000 g / m mỗi ngày hoặc aminoglycoside (gentamicin, tobramycin với tỷ lệ 20-000 mg / ngày) được sử dụng. kg mỗi ngày). Trong trường hợp không có tác dụng hoặc sau khi xác định tác nhân gây bệnh, người ta sử dụng các penicilin bán tổng hợp (oxacillin, methicillin hoặc ampicilin tiêm bắp tới 000 g / ngày). Cephalosporin cũng là thuốc cơ bản được sử dụng để điều trị IE: được sử dụng phổ biến nhất là claforan, cefamisin (1-4 g / ngày, tiêm bắp và tiêm tĩnh mạch), cũng như zeporin (6-12 g / ngày) và kefzol (tối đa 4-10 g tiêm tĩnh mạch). Và vv). Fusidin có tác dụng chống tụ cầu tốt, trong một số trường hợp, nó có hiệu quả trong việc đề kháng của vi sinh vật với các kháng sinh khác (10-16 g / ngày). Điều trị kháng sinh được chỉ định trong một thời gian dài trong một đợt từ 1,5-2 tháng, cho đến khi loại bỏ hoàn toàn tình trạng nhiễm trùng. Sau khi loại bỏ nhiễm trùng, tình trạng chung của bệnh nhân được cải thiện, thảm thực vật biến mất theo siêu âm tim và xác nhận vi sinh. Khi giảm hoạt tính miễn dịch của sinh vật, các tác nhân kháng khuẩn được kết hợp với liệu pháp miễn dịch thụ động (ví dụ, với viêm nội tâm mạc do tụ cầu - với huyết tương kháng tụ cầu hoặc α-globulin chống tụ cầu), sử dụng các chất điều hòa miễn dịch (thymalin, T-activin, v.v.). Để ngăn ngừa huyết khối, ví dụ, với bệnh viêm nội tâm mạc phát triển trên nền nhiễm trùng huyết, giảm đông máu có kiểm soát được tạo ra bằng cách sử dụng heparin (20-000 IU tiêm tĩnh mạch hoặc tiêm dưới da). Để ức chế các enzym phân giải protein, sử dụng theo phương (lên đến 25-000 IU tiêm tĩnh mạch). Khi IE van tim góp phần hình thành bệnh van tim hoặc các biểu hiện của bệnh không biến mất mặc dù điều trị bằng kháng sinh ồ ạt, thì nên thực hiện điều trị phẫu thuật. Một lập luận bổ sung ủng hộ can thiệp phẫu thuật là thuyên tắc lặp lại từ các lá van tim bị phá hủy do nhiễm trùng. Đôi khi nhiễm trùng vượt ra ngoài ranh giới của vòng van, đồng thời hình thành các ổ áp xe, đây cũng là một chỉ định điều trị ngoại khoa. Mục tiêu chính của ca mổ là bảo tồn van của chính bệnh nhân. Đôi khi chúng được giới hạn trong việc loại bỏ thực vật, khâu lại các vết rách của van, vv Nếu van gần như bị phá hủy hoàn toàn dưới tác động của nhiễm trùng, nó được thay thế bằng một bộ phận nhân tạo (bộ phận giả) sử dụng bộ phận giả cơ học và sinh học. Phòng ngừa. Phòng ngừa IE bao gồm vệ sinh kịp thời các ổ nhiễm trùng mãn tính ở khoang miệng, amidan, vòm họng, xoang cạnh mũi và sử dụng liệu pháp kháng khuẩn tích cực đối với các bệnh liên cầu khuẩn và tụ cầu cấp tính (đau thắt ngực, v.v.). Nên làm cứng cơ thể. Tất cả bệnh nhân bị bệnh van tim, cũng như với van giả, nên dùng kháng sinh dự phòng một ngày trước và ngay sau bất kỳ can thiệp nào, sau đó nhiễm trùng có thể xâm nhập vào máu. Cần theo dõi bệnh nhân ở những người đã bị nhiễm trùng cấp tính do liên cầu, tụ cầu. BÀI GIẢNG SỐ 6. Các bệnh về hệ hô hấp. Hen phế quản Cho đến nay vẫn chưa có một định nghĩa đầy đủ về bệnh hen suyễn, tuy nhiên, định nghĩa đầy đủ nhất về bệnh này được G. B. Fedoseev đưa ra vào năm 1982. Bệnh hen phế quản (BA) là một bệnh độc lập, mạn tính, tái phát với tổn thương chủ yếu ở đường hô hấp, cơ chế sinh bệnh chính và bắt buộc trong đó là phản ứng phế quản bị thay đổi do các cơ chế đặc hiệu (miễn dịch) và (hoặc) không đặc hiệu, bẩm sinh hoặc mắc phải, và dấu hiệu lâm sàng chính (bắt buộc) là cơn hen và (hoặc) bệnh hen. tình trạng (tình trạng hen) do co thắt cơ trơn phế quản, tăng tiết, rối loạn phân hủy và phù nề niêm mạc phế quản. Nguyên nhân. Sự kết hợp của một số yếu tố đóng vai trò quan trọng trong sự xuất hiện của bệnh hen suyễn. Về vấn đề này, có 2 dạng hen suyễn - dị ứng (từ athopia trong tiếng Latin - “khuynh hướng di truyền”) và dị ứng truyền nhiễm. Khuynh hướng di truyền là do sự liên quan của một số kháng nguyên tương hợp mô (HLA) với mức độ nghiêm trọng của bệnh hen suyễn, và sự gia tăng mức độ nghiêm trọng của bệnh đặc biệt thường thấy ở những người mang kháng nguyên B.35 và B40. Các yếu tố bên trong sự phát triển của bệnh là các khiếm khuyết sinh học trong hệ thống miễn dịch, nội tiết, hệ thống thần kinh tự chủ, độ nhạy và phản ứng của phế quản, sự thanh thải niêm mạc, nội mô mạch máu phổi, hệ thống phản ứng nhanh (tế bào mast, v.v.), chuyển hóa axit arachidonic, vân vân. Các yếu tố bên ngoài bao gồm: 1) các chất gây dị ứng truyền nhiễm (vi rút, vi khuẩn, nấm, nấm men, v.v.); 2) chất gây dị ứng không lây nhiễm (phấn hoa, bụi, công nghiệp, thuốc, thực phẩm; chất gây dị ứng của bọ ve, côn trùng và động vật); 3) chất kích ứng cơ học và hóa học (kim loại, gỗ, silicat, bụi bông; hơi axit, kiềm; khói, v.v.); 4) các yếu tố khí tượng và lý hóa (thay đổi nhiệt độ và độ ẩm không khí, dao động khí áp, từ trường Trái đất, nỗ lực vật lý, v.v.); 5) căng thẳng, tác động thần kinh và hoạt động thể chất. Tác nhân truyền nhiễm không những có thể có tác dụng gây dị ứng, mà còn làm giảm ngưỡng nhạy cảm của cơ thể đối với dị nguyên không lây nhiễm (dị ứng), tăng tính thấm của niêm mạc đường hô hấp đối với chúng; để tạo ra sự thay đổi trong khả năng phản ứng của các tế bào đích (tế bào mast, basophils, bạch cầu đơn nhân, v.v.) và hệ thống tác động. Sinh bệnh học. Phản ứng phế quản bị thay đổi là mối liên hệ trung tâm trong cơ chế bệnh sinh của bệnh và có thể là nguyên phát hoặc thứ phát. Trong trường hợp đầu tiên, những thay đổi về khả năng phản ứng có thể là bẩm sinh hoặc mắc phải do tiếp xúc trực tiếp với các yếu tố hóa học, cơ học, vật lý và nhiễm trùng. Những thay đổi thứ cấp trong khả năng phản ứng của phế quản là biểu hiện của những thay đổi trong khả năng phản ứng của hệ thống miễn dịch, nội tiết và thần kinh của cơ thể. Như vậy, nói về cơ chế bệnh sinh của AD, chúng ta có thể phân biệt 2 nhóm cơ chế: miễn dịch và không miễn dịch. Cơ chế miễn dịch trong đại đa số các trường hợp chiếm ưu thế trong quá trình bệnh. Vi phạm hệ thống miễn dịch trong màng nhầy của đường hô hấp, xảy ra theo loại I, III và IV của phản ứng quá mẫn, tức là với sự thay đổi miễn dịch dịch thể và tế bào, dẫn đến thay đổi phản ứng của phế quản. Đồng thời, giảm IgA tiết, hệ thống thực bào bị rối loạn, chức năng ức chế T của tế bào lympho giảm, sản xuất interferon giảm, cuối cùng dẫn đến giảm khả năng phòng thủ chống virus của cơ thể. Loại I (dị ứng, tái âm hoặc phản vệ). Để phản ứng với việc tiêu thụ các kháng nguyên exoallergen (phấn hoa, protein động thực vật, vi khuẩn và thuốc) vào cơ thể, có sự gia tăng sản xuất IgE (thuốc thử), được cố định và tích tụ trên các tế bào mast (tế bào tác động chính). Đây là giai đoạn miễn dịch của AD. Sau đó, giai đoạn bệnh lý của quá trình phát triển - làm suy giảm tế bào mast với việc giải phóng các chất hoạt tính, co giãn phế quản và hóa học (histamine, serotonin, các yếu tố hóa học khác nhau, v.v.). Đây là những chất trung gian chính hoạt động trên mạch máu và tế bào đích (tế bào tác động thứ cấp) - bạch cầu ái toan, bạch cầu trung tính, tiểu cầu, bạch cầu đơn nhân đại thực bào. Sau đó, khi tiếp xúc với chất trung gian chính, tiết ra chất trung gian thứ cấp (leukotrienes, prostaglandin, thromboxan, yếu tố hoạt hóa tiểu cầu và các chất khác thuộc nhóm eicosanoid). Dưới ảnh hưởng của các hoạt chất sinh học, giai đoạn sinh lý bệnh của bệnh sinh bắt đầu: tính thấm của lớp vi tuần hoàn tăng lên, dẫn đến sự phát triển của phù nề, viêm huyết thanh và co thắt phế quản. Về mặt lâm sàng, điều này được biểu hiện bằng sự vi phạm cấp tính của sự thông thoáng của phế quản và sự phát triển của một cơn hen suyễn. Phản ứng loại III (loại immunocomplex, hoặc hiện tượng Arthus) phát triển dưới ảnh hưởng của ngoại dị nguyên và nội dị nguyên (tự dị nguyên, được hình thành do sự biến tính của các protein của tiểu phế quản và phế nang do viêm nhiễm hoặc dị ứng và tác động của các chất kích thích khác nhau). Phản ứng xảy ra trong vùng dư thừa kháng nguyên với sự tham gia của các kháng thể kết tủa thuộc các globulin miễn dịch của lớp O và M. Tác động gây hại của phức hợp kháng nguyên-kháng thể được hình thành được thực hiện thông qua hoạt hóa bổ thể, giải phóng các enzym lysosome. Có tổn thương màng đáy, co thắt cơ trơn phế quản, giãn mạch và tăng tính thấm của vi mạch. Loại IV (tế bào, quá mẫn kiểu chậm) được đặc trưng bởi thực tế là các tế bào lympho nhạy cảm có tác động gây tổn thương. Trong trường hợp này, các chất trung gian của phản ứng dị ứng là các lymphokines (hoạt động trên các đại thực bào, các tế bào biểu mô), các enzym lysosome và một hệ thống kinin hoạt hóa. Dưới ảnh hưởng của các chất này, phù nề phát triển, sưng màng nhầy, co thắt phế quản, tăng sản xuất chất tiết nhớt phế quản. Hậu quả là sự vi phạm cấp tính của sự bảo vệ của phế quản, được biểu hiện bằng một cuộc tấn công nghẹt thở. Cơ chế phi miễn dịch là sự thay đổi cơ bản trong phản ứng của phế quản do kết quả của các khuyết tật sinh học bẩm sinh và mắc phải. Cơ chế phi miễn dịch tác động lên các tế bào tác động chính hoặc phụ hoặc trên các thụ thể của cơ trơn phế quản, mạch máu, tế bào của tuyến phế quản. Điều này làm thay đổi khả năng phản ứng của các tế bào đích và hơn hết là các tế bào mast, đi kèm với việc sản xuất quá nhiều các chất có hoạt tính sinh học (histamine, leukotrienes, v.v.). Để phản ứng với sự phóng thích của chúng, co thắt phế quản, sưng màng nhầy, tăng và phân biệt các tuyến phế quản phát triển. Tất cả những điều này làm thay đổi đáng kể sự lưu thông của phế quản và gây ra cơn hen suyễn. Sức cản phế quản có thể thay đổi có điều kiện và vô điều kiện như một phản xạ. Ví dụ, tắc nghẽn phát sinh do tiếp xúc với không khí lạnh, hít phải khí và bụi khó chịu và hoạt động thể chất là do co thắt phế quản thông qua phản xạ phế vị. Nguyên nhân gây co thắt phế quản cũng có thể là do tổn thương vùng tác động của phản xạ co thắt phế quản phế vị hoặc do sự phong tỏa các thụ thể β-adrenergic. Gần đây, họ nói về một vai trò đặc biệt trong cơ chế bệnh sinh của vi phạm sự bảo quản phế quản của suy glucocorticoid và rối loạn disovarian. Sự thiếu hiệu quả của glucocorticosteroid dẫn đến sự phát triển tăng hoạt tính của tế bào mast, giảm tổng hợp catecholamine và hoạt hóa các prostaglandin F2a, cũng như vi phạm hệ thống năng lực miễn dịch (ở đây chúng ta nói về sự tham gia phức tạp vào cơ chế bệnh sinh của AD và các cơ chế miễn dịch và không miễn dịch). Giảm kích thích sinh dục và giảm bạch cầu ái toan hoạt động trên các thụ thể α- và β-adrenergic, làm tăng hoạt tính của thụ thể trước và giảm hoạt tính của thụ thể sau. Phân loại. Sự chiếm ưu thế của cơ chế này hoặc cơ chế khác trong sinh bệnh học của bệnh hen suyễn cho phép chúng ta xác định các đặc điểm sinh bệnh học khác nhau của nó. Hiện nay, cách phân loại do G. B. Fedoseev (1982) đề xuất được sử dụng. Các giai đoạn phát triển của AD. I - tiền hen (các tình trạng đe dọa phát triển: viêm phế quản cấp và mãn tính, viêm phổi cấp và mãn tính có yếu tố co thắt phế quản phối hợp với viêm mũi vận mạch, mày đay). II - BA hình thành trên lâm sàng (được coi là như vậy sau đợt tấn công đầu tiên hoặc ngay lập tức bắt đầu trạng thái asthmaticus). BA dạng: 1) miễn dịch học; 2) không miễn dịch. Cơ chế di truyền bệnh (các biến thể lâm sàng và di truyền bệnh) của AD: 1) dị ứng; 2) phụ thuộc vào nhiễm trùng; 3) tự miễn dịch; 4) bất bình thường; 5) mất cân bằng vi mạch thần kinh; 6) mất cân bằng hệ adrenergic; 7) mất cân bằng cholinergic; 8) phản ứng phế quản bị thay đổi chính. Ở một bệnh nhân, có thể kết hợp một số biến thể lâm sàng và di truyền bệnh. Trong tình huống như vậy, tại thời điểm kiểm tra, cần phải nêu rõ biến thể chính của bệnh nhân này, điều quan trọng là phải có liệu pháp thích hợp. Trong quá trình BA kéo dài, có thể thay đổi cơ chế phát sinh bệnh. Mức độ nghiêm trọng của BA: 1) đợt cấp nhẹ (hiếm gặp, 2-3 lần một năm, cắt cơn hen ngắn hạn bằng cách uống các loại thuốc giãn phế quản khác nhau bên trong); 2) mức độ nghiêm trọng trung bình (các đợt cấp thường xuyên hơn 3-4 lần một năm, các cơn hen suyễn nặng hơn và ngừng tiêm thuốc); 3) diễn tiến nặng (đặc trưng bởi các đợt cấp thường xuyên và kéo dài, các cơn nặng, thường chuyển sang trạng thái hen). Việc phân chia BA theo mức độ nghiêm trọng của khóa học là có điều kiện. Vì vậy, với một diễn biến nhẹ của BA, bệnh nhân có thể tử vong do bệnh hen suyễn phát triển đột ngột. Các giai đoạn của khóa học cử nhân: 1) đợt cấp (sự hiện diện của các cơn hen suyễn hoặc hen suyễn tái phát); 2) đợt cấp giảm dần (các cuộc tấn công trở nên hiếm hơn và nhẹ hơn, các dấu hiệu thực thể và chức năng của bệnh ít rõ ràng hơn so với trong đợt cấp); 3) thuyên giảm (các biểu hiện điển hình của BA biến mất: cơn hen không xảy ra; sự thông thoáng của phế quản được phục hồi hoàn toàn hoặc một phần). Các biến chứng: 1) phổi: khí phế thũng, suy phổi, xẹp phổi, tràn khí màng phổi, tình trạng hen suyễn, v.v ...; 2) ngoài phổi: cor pulmonale (còn bù và mất bù với sự phát triển của suy tim phải), loạn dưỡng cơ tim, v.v. Ảnh lâm sàng. Dấu hiệu đặc trưng nhất của bệnh hen suyễn là phàn nàn về các cơn nghẹt thở (khó thở chủ yếu khi thở ra), khó thở và ho các loại (khô, kịch phát hoặc tiết ra đờm nhớt). Sự phát triển của nhiễm trùng phế quản phổi gây ra sự gia tăng nhiệt độ cơ thể. Khó thở bằng mũi là biểu hiện của bệnh viêm mũi dị ứng (viêm mũi vận mạch, polyp), thường xảy ra trong giai đoạn tiền hen suyễn. Dữ liệu lịch sử giúp thiết lập mối liên hệ giữa sự phát triển của các cơn co giật và việc tiếp xúc với một số chất gây dị ứng và các yếu tố khác. Thông thường đó là nhiễm trùng đường hô hấp, đặc biệt là trong đợt cấp của bệnh. Từ tiền sử bệnh, họ tìm hiểu về ảnh hưởng của nỗ lực thể chất (như đi bộ nhanh, cười, v.v.), sự thay đổi của các yếu tố khí tượng (như lạnh, độ ẩm cao, v.v.), rối loạn lưỡng sắc, các yếu tố chuyên môn đến sự xuất hiện của bệnh hen suyễn các cuộc tấn công. Nghiên cứu về tiền sử dị ứng góp phần chẩn đoán một biến thể dị ứng của BA. Trong những trường hợp như vậy, các đợt cấp của bệnh là theo mùa (thường xuyên hơn vào mùa xuân và mùa hè), kèm theo viêm mũi, viêm kết mạc. Những bệnh nhân như vậy có mày đay, phù Quincke; không dung nạp thực phẩm, một số dược chất được phát hiện; có khuynh hướng di truyền đối với các bệnh dị ứng. Dữ liệu từ tiền sử bệnh thường cho phép xác định sự hiện diện của cái gọi là hen suyễn do aspirin. Trong trường hợp này, không có hình thức di truyền của các bệnh dị ứng. Những bệnh nhân như vậy lo ngại về việc khó thở bằng mũi (các khối đa nhân), và triệu chứng đặc trưng nhất là không dung nạp thuốc chống viêm không steroid (axit acetylsalicylic, indomethacin, v.v.), gây ra các cơn hen. Trong trường hợp này, người ta đã có thể giả định cơ chế gây AD của prostaglandin. Dữ liệu về sự phát triển của tình trạng hen trong quá khứ cho biết mức độ nghiêm trọng của bệnh và cho biết sự cần thiết của liệu pháp corticosteroid. Chẩn đoán. Điều quan trọng nhất là việc xác định các biểu hiện ngoài phổi của dị ứng, dấu hiệu tắc nghẽn phế quản, biến chứng của bệnh hen suyễn và các bệnh khác kèm theo cơn co thắt phế quản. Khi kiểm tra da, có thể phát hiện các biểu hiện dị ứng: mày đay, ban đỏ sẩn, cho thấy đây là một biến thể miễn dịch của BA. Sự kết hợp của bệnh hen suyễn với bệnh chàm, viêm da thần kinh, bệnh vẩy nến dẫn đến bệnh hen suyễn nặng. Thường có thể xác định được sự vi phạm của hơi thở bằng mũi. Viêm mũi và polyp được coi là tiền hen suyễn. Viêm xoang và các bệnh viêm xoang khác có thể gây nghẹt thở. Kiểm tra thực thể phổi, thường là do viêm phế quản mãn tính tiềm ẩn, có thể phát hiện các dấu hiệu của khí phế thũng dẫn đến sự phát triển của suy hô hấp mãn tính và rối loạn nhịp tim. Các dấu hiệu nghe tim của tắc nghẽn phế quản được phát hiện: thay đổi nhịp thở (thở ra dài, khô, hầu hết là khò khè, thở khò khè), thở ra ép buộc, bộc lộ co thắt phế quản tiềm ẩn (xuất hiện hoặc tăng thở khò khè khô). Nghe tim phổi phải được thực hiện ở tư thế bệnh nhân nằm: số lượng ran khô tăng lên theo cơ chế "phế vị" của chúng. Thường xuyên lắng nghe ở một khu vực nhất định, tiếng lục khục sủi bọt mịn có âm thanh ẩm ("rắc") có thể là dấu hiệu của chứng xơ vữa động mạch đã phát triển. Khám khách quan cho thấy bệnh nhân có triệu chứng của các bệnh khác (nổi “bướm” trên da mặt, nổi hạch kết hợp với gan và lách to, huyết áp tăng liên tục, sốt dai dẳng, v.v.), trong đó xuất hiện các cơn co thắt phế quản, biểu hiện bằng ngạt thở (lupus ban đỏ hệ thống, viêm quanh túi lệ nốt). Sau đó, chẩn đoán được cho là AD trở nên khó xảy ra. Chụp cắt lớp cho thấy các dấu hiệu đặc trưng của tắc nghẽn phế quản: giảm thể tích thở ra cưỡng bức trong giây đầu tiên (FEV1), giảm hệ số Tiffno (FEV1 sang VC dưới dạng phần trăm) và phần trăm FEV1 đến FZhEL. Trong đợt cấp của BA, thể tích phổi còn lại (RLVT) và khả năng tồn dư chức năng (FOC) vượt quá mức ban đầu từ 100% trở lên. Khi phân tích xoắn khuẩn, các dấu hiệu của rối loạn vận động khí quản được tìm thấy, góp phần vào việc vi phạm tính thông thoáng của phế quản, bởi sự hiện diện của một vết khía ở phần trên của màu giảm dần của xoắn khuẩn (triệu chứng Kolbet-Wyss). Đo lường khí nén cho thấy sức mạnh thở ra chiếm ưu thế so với sức mạnh thở ra, đây là đặc điểm của tắc nghẽn phế quản. Theo phương pháp chụp phổi với việc xây dựng đường cong "dòng chảy - thể tích", sự vi phạm sự thông thương của phế quản được chẩn đoán riêng biệt ở cấp độ phế quản lớn, trung bình và nhỏ. Sự xuất hiện của tăng sức đề kháng của phế quản, được đăng ký bằng cách sử dụng xoắn ốc, đo khí và chụp cắt lớp màng phổi, để phản ứng với hoạt động thể chất, hít phải không khí lạnh, khí khó chịu và acetylcholine cho thấy phản ứng phế quản bị thay đổi. Thử nghiệm dị ứng được thực hiện bằng cách sử dụng một tập hợp các chất gây dị ứng không lây nhiễm và truyền nhiễm khác nhau, nó chỉ được thực hiện bên ngoài đợt cấp của bệnh. Để đánh giá tác động kích thích của chất gây dị ứng, các xét nghiệm dị ứng da được thực hiện (phương pháp bôi, soi và bôi chất gây dị ứng trong da), chất gây dị ứng có thể được bôi lên kết mạc mắt, niêm mạc mũi. Đáng tin cậy nhất là chẩn đoán cụ thể bệnh hen suyễn - xác định tình trạng tăng tiết khí phế quản cụ thể với sự trợ giúp của các xét nghiệm kích thích hít thở. Tuy nhiên, không nên quên thực tế rằng đường dùng này có thể gây ra cơn hen suyễn nặng hoặc phát triển tình trạng hen suyễn. Ví dụ, để chẩn đoán cụ thể AD, khi không thể tiến hành xét nghiệm dị ứng, xét nghiệm hấp thụ phóng xạ cũng được sử dụng, giúp định lượng kháng thể IgE. Các nghiên cứu trong phòng thí nghiệm giúp xác nhận chẩn đoán được đề xuất, đánh giá diễn biến của bệnh và hiệu quả của phương pháp điều trị. Tiêu chuẩn chẩn đoán chính của AD là sự xuất hiện của bạch cầu ái toan trong đờm, nhưng đây là một dấu hiệu không đặc hiệu, nó có thể là biểu hiện của một phản ứng dị ứng chung của cơ thể. Cũng có tầm quan trọng trong chẩn đoán là phát hiện xoắn ốc Kurshman và tinh thể Charcot-Leiden trong đờm. Các nghiên cứu trong phòng thí nghiệm chứng minh sự hiện diện của một quá trình viêm đang hoạt động và mức độ nghiêm trọng của nó về sự gia tăng các chỉ số giai đoạn cấp tính. Với sự gia tăng suy hô hấp trong trường hợp cơn hen kịch phát và tình trạng hen suyễn, điều quan trọng là phải nghiên cứu trạng thái axit-bazơ và thành phần khí máu. Kiểm tra X-quang chẩn đoán các ổ nhiễm trùng (trong xoang cạnh mũi, răng, túi mật) và sự hiện diện của bệnh cấp tính (viêm phổi) hoặc đợt cấp của quá trình viêm mãn tính ở phổi, khí phế thũng và xơ phổi. Dữ liệu điện tâm đồ chứng minh các dấu hiệu của sự phát triển của pulmonale bù trừ - phì đại của tim phải. Chẩn đoán phân biệt. BA được phân biệt với hen tim (xem Bảng 8). Bảng 8 Chẩn đoán phân biệt AD
Cũng cần phân biệt bệnh hen suyễn do nhiễm trùng-dị ứng và dị ứng (xem Bảng 9). Bảng 9 Hen suyễn do dị ứng và dị ứng truyền nhiễm
Điều trị. Trong điều trị hen suyễn, nên sử dụng phương pháp từng bước, điều này được giải thích bởi mức độ nghiêm trọng khác nhau của diễn biến bệnh ở những người khác nhau và trên cùng một bệnh nhân. Giai đoạn 1 là cơn hen nhẹ nhất, giai đoạn 4 là nặng nhất. Giai đoạn 1: Một đợt nhẹ không liên tục trong đó các triệu chứng hen suyễn xuất hiện khi tiếp xúc với chất kích hoạt (ví dụ: phấn hoa hoặc lông động vật) hoặc do tập thể dục. Việc sử dụng thuốc chống viêm lâu dài trong điều trị cho những bệnh nhân này không được chỉ định. Điều trị bằng thuốc dự phòng nếu cần thiết (β hít2chất chủ vận, cromoglycate, nedocromil, hoặc thuốc kháng cholinergic). Đôi khi, các đợt cấp nặng hơn và kéo dài hơn cần dùng một đợt corticosteroid đường uống ngắn hạn. Nếu bệnh hen suyễn biểu hiện với các triệu chứng thường xuyên hơn, tăng nhu cầu sử dụng thuốc giãn phế quản thì cần chuyển sang giai đoạn tiếp theo. Giai đoạn 2. Liệu trình bền bỉ nhẹ. Liệu pháp chính bao gồm thuốc chống viêm, corticosteroid dạng hít, natri cromoglycate hoặc nedocromil natri. Liều lượng corticosteroid là 200-500 microgam beclomethasone dipropionate hoặc budesonide mỗi ngày. Để điều trị triệu chứng, hít β2- thuốc, nhưng không quá 3-4 lần một ngày. Đối với các đợt cấp nặng hơn và kéo dài, có thể dùng một đợt corticosteroid đường uống ngắn hạn. Nếu các triệu chứng vẫn tồn tại mặc dù đã dùng liều corticosteroid dạng hít ban đầu, nên tăng liều beclomethasone dipropionat lên 750-800 microgam mỗi ngày. Tuy nhiên, một giải pháp thay thế để tăng liều hormone hít, đặc biệt để kiểm soát cơn hen về đêm, là bổ sung thuốc giãn phế quản tác dụng kéo dài uống vào ban đêm (với liều corticosteroid dạng hít ít nhất 500 mcg). Giai đoạn 3 được đặc trưng bởi mức độ nghiêm trọng trung bình của BA. Những bệnh nhân này cần uống thuốc chống viêm dự phòng hàng ngày. Liều corticosteroid dạng hít là 800-2000 mcg kết hợp với thuốc giãn phế quản tác dụng kéo dài. Bạn có thể sử dụng theophylin tác dụng kéo dài (với việc theo dõi liên tục nồng độ của chúng không quá 5-15 µg / ml), uống và hít.2thuốc chủ vận tác dụng kéo dài. Chỉ định một cách có triệu chứng β2- Thuốc chủ vận tác dụng ngắn hạn hoặc thuốc thay thế (giai đoạn 2). Giai đoạn 4. Hen suyễn nặng, khi nó không được kiểm soát hoàn toàn. Trong trường hợp này, mục tiêu điều trị là đạt được kết quả tốt nhất có thể. Điều trị chủ yếu là dùng corticosteroid dạng hít liều cao (từ 800 đến 2000 microgam beclomethasone dipropionat mỗi ngày) kết hợp với thuốc giãn phế quản tác dụng kéo dài. Nếu cần thiết, β hít được chỉ định để làm giảm các triệu chứng.2- Thuốc chủ vận tác dụng ngắn (không quá 3-4 lần một ngày). Đợt cấp nặng hơn có thể cần một đợt điều trị bằng corticosteroid đường uống, được kê đơn với liều lượng tối thiểu hoặc cách ngày. Để ngăn ngừa sự phát triển của các tác dụng phụ, liều cao corticosteroid dạng hít được sử dụng thông qua một ống đệm. Bước 5 liên quan đến việc giảm bớt thuốc hỗ trợ. Điều này có thể thực hiện được nếu bệnh hen suyễn vẫn được kiểm soát trong ít nhất 3 tháng, điều này giúp giảm nguy cơ tác dụng phụ và tăng tính nhạy cảm của bệnh nhân với phương pháp điều trị theo kế hoạch. "Giảm" điều trị được thực hiện dưới sự kiểm soát liên tục các triệu chứng, biểu hiện lâm sàng và các chỉ số của chức năng hô hấp bằng cách giảm dần (hủy bỏ) liều cuối cùng hoặc các loại thuốc bổ sung. Dừng các cuộc tấn công. Cơn nhẹ có thể được điều trị tại nhà bằng thuốc giãn phế quản tác dụng ngắn. Điều trị được thực hiện cho đến khi các triệu chứng biến mất hoàn toàn. Các cơn vừa và nặng không chỉ cần dùng đủ liều thuốc giãn phế quản tác dụng ngắn (thuốc hít β2- thuốc chủ vận tác dụng ngắn hạn), mà còn chỉ định corticosteroid toàn thân. Nếu bệnh nhân bị giảm oxy máu, nên cho thở oxy. Để điều trị các cơn hen suyễn tại trung tâm y tế hoặc bệnh viện, liều cao dạng hít β2chất chủ vận thông qua máy phun sương. Việc sử dụng ống hít khí dung theo liều đo thông qua một ống đệm là rất hiệu quả. Tốt hơn, corticosteroid được dùng bằng đường uống, không tiêm tĩnh mạch. Khi sử dụng theophylline hoặc aminophylline kết hợp với liều cao của β2- thuốc đối kháng không có tác dụng giãn phế quản bổ sung, nhưng nguy cơ tác dụng phụ sẽ tăng lên. Theophyllines chỉ có thể được sử dụng khi không có β2- chất đối kháng, tuy nhiên, chúng có thể được tiêm tĩnh mạch với tốc độ 6 mg / kg aminophylline (hoặc 5 mg / kg theophylline) với liều không đổi 0,5-1,0 mg / kg mỗi giờ trong 24 giờ. Ngoài ra, β2Thuốc chủ vận tác dụng ngắn cũng có thể sử dụng epinephrine, nhưng có thể có những tác dụng phụ đáng kể khi sử dụng. Thuốc tiêu nhầy dạng hít, thuốc an thần và thuốc kháng histamine, magnesium sulfate, vật lý trị liệu lồng ngực, ngậm nước với thể tích lớn dịch cho người lớn và trẻ lớn hơn không được khuyến cáo để điều trị cơn hen suyễn để tránh làm tăng cơn ho. Phòng ngừa. Phòng ngừa hen suyễn ban đầu bao gồm điều trị bệnh nhân ở trạng thái tiền hen suyễn, xác định các khiếm khuyết sinh học ở những người khỏe mạnh thực tế có tiền sử gia đình gây ra mối đe dọa cho sự xuất hiện của bệnh hen suyễn, loại bỏ các chất gây dị ứng, chất kích thích nguy hiểm tiềm ẩn và các yếu tố khác khỏi cơ thể. Môi trường của bệnh nhân có thể dẫn đến sự phát triển của bệnh. Khi điều trị bệnh nhân trong tình trạng tiền hen suyễn, cần vệ sinh ổ nhiễm trùng, điều trị bệnh tê giác do dị ứng, áp dụng nhiều phương pháp điều trị không dùng thuốc, bao gồm châm cứu và tâm lý trị liệu, tập thể dục, liệu pháp barot và điều trị spa. Thực hiện giảm mẫn cảm cụ thể và không đặc hiệu được hiển thị. BÀI GIẢNG SỐ 7. Các bệnh về hệ hô hấp. Viêm phế quản hình nón Viêm phế quản tắc nghẽn mãn tính là một tổn thương viêm lan tỏa không dị ứng của cây phế quản, gây ra bởi các tác động kích thích kéo dài lên phế quản của các tác nhân khác nhau, có diễn tiến tiến triển và được đặc trưng bởi tắc nghẽn thông khí phổi, tạo chất nhầy và chức năng thoát nước của phế quản. cây, được biểu hiện bằng ho, có đờm và khó thở. Theo định nghĩa của WHO, nếu bệnh nhân ho ra đờm hầu hết các ngày trong ít nhất 3 tháng liên tục trong hơn 2 năm liên tục thì bệnh được coi là viêm phế quản mãn tính (CB). Viêm phế quản mãn tính được chia thành nguyên phát và thứ phát. Viêm phế quản mãn tính nguyên phát là một bệnh độc lập không liên quan đến các quá trình phế quản phổi khác hoặc tổn thương các cơ quan và hệ thống khác, trong đó có tổn thương lan tỏa của cây phế quản. CB thứ phát phát triển dựa trên nền tảng của các bệnh khác - cả phổi (lao, giãn phế quản, v.v.) và ngoài phổi (nhiễm độc niệu, suy tim sung huyết, v.v.). Thông thường nó có tính chất cục bộ (phân đoạn). Xem xét HB sơ cấp. Nguyên nhân. Cả yếu tố ngoại sinh (khói thuốc lá, ô nhiễm không khí, điều kiện nghề nghiệp không thuận lợi, yếu tố khí hậu và nhiễm trùng) và yếu tố nội sinh (bệnh lý vòm họng, suy hô hấp qua mũi, bệnh hô hấp cấp tính tái phát, viêm phế quản cấp và nhiễm trùng khu trú đường hô hấp trên) đóng một vai trò trong sự phát triển của con đường CB., khuynh hướng di truyền, rối loạn chuyển hóa (béo phì)). Sinh bệnh học. Dưới ảnh hưởng của các yếu tố ngoại sinh và với sự tham gia của các yếu tố nội sinh trong cây khí quản, các đặc tính cấu trúc và chức năng của màng nhầy và lớp dưới niêm mạc thay đổi, tình trạng viêm màng nhầy phát triển, chức năng thông thoáng và thoát nước của phế quản bị gián đoạn. Những thay đổi về cấu trúc và chức năng ở màng nhầy và lớp dưới niêm mạc được biểu hiện bằng sự tăng sản và tăng chức năng của các tế bào hình cốc, tuyến phế quản, tăng tiết chất nhầy đặc và nhớt, dẫn đến sự gián đoạn trong hệ thống vận chuyển đường mật. Lượng IgA-lysozyme và lactoferrin bài tiết được tạo ra bị giảm. Phù nề của màng nhầy phát triển, và sau đó - teo và chuyển sản của biểu mô. Viêm màng nhầy là do các chất kích thích khác nhau kết hợp với nhiễm trùng (virus và vi khuẩn). Các chất hóa học (chất ô nhiễm) chứa trong không khí có tác động làm tổn thương đường hô hấp, làm sưng màng nhầy và ức chế hoạt động của biểu mô có lông mao. Điều này dẫn đến vi phạm quá trình di tản và giảm chức năng rào cản của niêm mạc phế quản. Nội dung catarrhal được thay thế bằng catarrhal-mủ, và sau đó có mủ. Quá trình viêm lan rộng đến các phần xa của cây phế quản làm gián đoạn việc sản xuất chất hoạt động bề mặt và làm giảm hoạt động của các đại thực bào phế nang thực bào các phần tử lạ. Nếu sự co thắt phế quản xảy ra trong trường hợp viêm được rõ rệt, thì một thành phần co thắt phế quản (không dị ứng) sẽ phát triển. Nhiễm trùng liên quan trong đợt cấp của chứng viêm góp phần vào sự phát triển của một thành phần hen (dị ứng), điều này có thể làm cho CB như vậy là tiền hen suyễn. Hội chứng tắc nghẽn phát triển do sự kết hợp của một số yếu tố: 1) co thắt các cơ trơn của phế quản do tác động kích thích của các yếu tố ngoại sinh và những thay đổi viêm ở màng nhầy; 2) tăng tiết chất nhầy, thay đổi tính chất lưu biến của nó, dẫn đến gián đoạn sự vận chuyển của chất nhầy và tắc nghẽn phế quản với chất tiết nhớt; 3) chuyển sản biểu mô từ hình trụ sang vảy phân tầng và sự tăng sản của nó; 4) vi phạm sản xuất chất hoạt động bề mặt; 5) viêm phù nề và thâm nhiễm niêm mạc; 6) xẹp các phế quản nhỏ và làm tắc nghẽn các tiểu phế quản; 7) thay đổi dị ứng trên màng nhầy. Nếu các phế quản cỡ lớn có liên quan đến quá trình này (viêm phế quản gần), tắc nghẽn phế quản không được biểu hiện. Nhưng trong trường hợp tổn thương phế quản vừa và nhỏ, một sự vi phạm rõ rệt về tính bảo vệ của phế quản xảy ra. Tuy nhiên, với một tổn thương biệt lập của phế quản nhỏ (viêm phế quản xa), không có thụ thể ho, khó thở có thể là bằng chứng duy nhất của viêm phế quản phát triển và ho xuất hiện khi các phế quản lớn hơn tham gia vào quá trình này. Các tỷ lệ thay đổi khác nhau trong màng nhầy gây ra sự hình thành một dạng lâm sàng nhất định: 1) với viêm phế quản không tắc nghẽn catarrhal, những thay đổi bề ngoài trong các đặc tính cấu trúc và chức năng của màng nhầy chiếm ưu thế; 2) với viêm phế quản có mủ (mủ), các quá trình viêm nhiễm chiếm ưu thế. Tuy nhiên, một tình huống cũng có thể xảy ra khi viêm phế quản catarrhal kéo dài do thêm nhiễm trùng có thể trở nên chảy mủ, vv Trong biến thể không tắc nghẽn của tất cả các dạng lâm sàng của viêm phế quản mãn tính, rối loạn thông khí hơi rõ rệt; 3) rối loạn tắc nghẽn ban đầu chỉ xuất hiện trên nền của đợt cấp của bệnh và gây ra bởi những thay đổi viêm trong phế quản, tăng và rối loạn kiềm, co thắt phế quản (các thành phần có thể đảo ngược của tắc nghẽn), nhưng sau đó chúng kéo dài liên tục, trong khi hội chứng tắc nghẽn phát triển chậm rãi. Trong viêm phế quản mãn tính tắc nghẽn, màng nhầy và lớp dưới niêm mạc dày lên, phù và tăng tiết chiếm ưu thế, và rối loạn thông khí dai dẳng cũng là đặc điểm. Sự tắc nghẽn phát triển của các phế quản nhỏ dẫn đến khí phế thũng. Trong quá trình của nó, HB trải qua một quá trình phát triển nhất định. Kết quả của sự phát triển của khí phế thũng và xơ phổi, sự thông khí không đồng đều của phổi được ghi nhận, các vùng tăng và giảm thông khí được hình thành. Kết hợp với những thay đổi viêm tại chỗ, điều này dẫn đến suy giảm trao đổi khí, suy hô hấp, giảm oxy máu động mạch và tăng áp phổi, tiếp theo là sự phát triển của tình trạng đe dọa tính mạng chính - suy thất phải. Phân loại. Hiện tại không có phân loại CB được chấp nhận rộng rãi. Điều quan trọng là phải chia CB thành các biến thể tắc nghẽn và không tắc nghẽn, trong đó mỗi biến thể có thể phát triển quá trình viêm catarrhal (chất nhầy), catarrhal-mủ hoặc mủ. Phân loại cũng bao gồm các dạng hiếm - CB xuất huyết và xơ. Theo mức độ tổn thương của phế quản, người ta phân biệt: tổn thương chủ yếu là phế quản lớn (viêm phế quản gần) và với tổn thương chủ yếu là phế quản nhỏ (phế quản xa) (N. R. Paleev, 1985). Ảnh lâm sàng. Các triệu chứng chính của CB là ho, khạc đờm và khó thở. Trong thời gian bệnh trầm trọng hơn hoặc do thiếu oxy dẫn đến suy phổi và các biến chứng khác, các triệu chứng chung được xác định (đổ mồ hôi, suy nhược, tăng nhiệt độ cơ thể, mệt mỏi, v.v.). Ho là biểu hiện điển hình nhất của bệnh. Dựa trên tính chất và tính nhất quán của đờm, người ta có thể giả định một biến thể của diễn biến bệnh. Trong phiên bản không tắc nghẽn của viêm phế quản catarrhal, ho đi kèm với việc tiết ra một lượng nhỏ đờm nhầy, nước (thường vào buổi sáng, sau khi tập thể dục hoặc do thở nhiều). Khi bắt đầu bệnh, cơn ho không làm người bệnh khó chịu; sự xuất hiện của cơn ho kịch phát cho thấy sự phát triển của tắc nghẽn phế quản. Cơn ho có âm sắc sủa và có tính chất kịch phát với sự xẹp rõ rệt khi thở ra của khí quản và phế quản lớn. Với bệnh viêm phế quản có mủ và nhầy, người bệnh càng lo lắng về tình trạng ho khạc ra đờm. Trong trường hợp đợt cấp của bệnh, đờm có đặc tính giống như mủ, số lượng tăng lên, đôi khi đờm được bài tiết khó khăn (do tắc nghẽn phế quản trong đợt cấp). Trong biến thể tắc nghẽn của viêm phế quản, ho không có kết quả và thành tiếng, kèm theo khó thở và có một ít đờm. Khó thở xảy ra ở tất cả bệnh nhân viêm phế quản mãn tính vào nhiều thời điểm khác nhau. Sự xuất hiện của khó thở ở những bệnh nhân "ho kéo dài" ban đầu khi gắng sức đáng kể cho thấy có thêm tắc nghẽn phế quản. Khi bệnh tiến triển, khó thở trở nên rõ rệt hơn và liên tục, tức là suy hô hấp (phổi) phát triển. Ở biến thể không tắc nghẽn, CB tiến triển chậm, khó thở thường xuất hiện sau 20 - 30 năm kể từ khi bệnh khởi phát. Những bệnh nhân như vậy hầu như không bao giờ khắc phục được sự khởi phát của bệnh, mà chỉ cho biết sự xuất hiện của các biến chứng hoặc đợt cấp thường xuyên. Có tiền sử quá mẫn với lạnh và hầu hết các bệnh nhân cho biết họ đã hút thuốc trong thời gian dài. Ở một số bệnh nhân, bệnh có liên quan đến các nguy cơ nghề nghiệp tại nơi làm việc. Khi phân tích tiền sử ho, cần chắc chắn rằng bệnh nhân không có bệnh lý nào khác của bộ máy phế quản phổi (lao, khối u, giãn phế quản, bệnh bụi phổi, các bệnh hệ thống của mô liên kết, v.v.), kèm theo các triệu chứng tương tự. Đôi khi bệnh sử cho thấy ho ra máu do niêm mạc phế quản bị tổn thương nhẹ. Ho ra máu tái phát cho thấy một dạng viêm phế quản xuất huyết. Ngoài ra, ho ra máu trong viêm phế quản mãn tính, lâu ngày có thể là triệu chứng đầu tiên của bệnh ung thư phổi hoặc giãn phế quản. Chẩn đoán. Nghe thấy khó thở (với sự phát triển của khí thũng, nó có thể trở nên yếu đi) và thở khò khè khô có tính chất rải rác, âm sắc của chúng phụ thuộc vào kích thước của phế quản bị ảnh hưởng (thở khò khè, có thể nghe rõ khi thở ra, là đặc điểm của tổn thương phế quản nhỏ). ). Những thay đổi trong dữ liệu nghe tim sẽ giảm thiểu ở bệnh viêm phế quản mãn tính không do tắc nghẽn thuyên giảm và rõ ràng nhất trong đợt cấp của quá trình (các vết ướt có nhiều cỡ nòng khác nhau có thể biến mất sau khi ho nhiều và tiết nhiều đờm). Với đợt cấp của viêm phế quản tắc nghẽn, khó thở tăng lên, các hiện tượng suy hô hấp tăng lên. Tiết dịch nhớt có mủ càng làm phức tạp thêm sự thông thoáng của phế quản. Thành phần tắc nghẽn đã tham gia vào cả hai dạng viêm phế quản có mủ và viêm phế quản, và trong giai đoạn đợt cấp hoặc trong quá trình tiến triển của chúng, làm trầm trọng thêm quá trình viêm phế quản. Các dấu hiệu của tắc nghẽn phế quản: kéo dài giai đoạn thở ra với nhịp thở bình tĩnh và đặc biệt là cưỡng bức; thở khò khè khi thở ra (nghe tim tốt hơn khi thở cưỡng bức và ở tư thế nằm ngửa); các triệu chứng của bệnh khí thũng phổi tắc nghẽn. Trong các trường hợp viêm phế quản mãn tính tiến triển và kèm theo các biến chứng, các dấu hiệu của khí phế thũng phổi, suy hô hấp và tim (tâm thất phải) - tim phổi mất bù xuất hiện: acrocyanosis, nhão hoặc sưng phù chân và bàn chân, thay đổi ở móng dạng kính đồng hồ, và các phalang tận cùng của bàn tay và bàn chân - ở dạng que trống, sưng các tĩnh mạch cổ, đập ở vùng thượng vị do tâm thất phải, giọng của âm II ở liên sườn II. khoang bên trái xương ức, gan to. Ảnh hưởng đến hình ảnh của bệnh và thêm thành phần hen (dị ứng), khi có sự tương đồng với bệnh hen phế quản. Các chỉ số trong phòng thí nghiệm và dụng cụ có mức độ ý nghĩa khác nhau tùy thuộc vào giai đoạn của quá trình. Trong thời kỳ đầu của bệnh hoặc trong giai đoạn thuyên giảm, có thể không có thay đổi. Tuy nhiên, các chỉ số này có tầm quan trọng lớn đối với việc xác định hoạt động của quá trình viêm; làm rõ các hình thức lâm sàng của bệnh; xác định các biến chứng; chẩn đoán phân biệt với các bệnh có triệu chứng lâm sàng tương tự. Chụp X-quang các cơ quan trong lồng ngực được thực hiện ở tất cả các bệnh nhân bị viêm phế quản mãn tính, tuy nhiên, theo quy luật, không có thay đổi nào ở phổi trên phim chụp X quang đơn giản. Có thể có một biến dạng lưới của mô hình phổi, do sự phát triển của chứng xơ phổi. Với một quá trình dài của quá trình, các dấu hiệu của khí phế thũng được bộc lộ. Với sự phát triển của tim phổi, thân động mạch phổi phồng lên xuất hiện trên đường viền bên trái của bóng tim, mở rộng các động mạch nền, tiếp theo là sự thu hẹp hình nón của chúng và giảm đường kính của ngoại vi. cành cây. Chụp Xquang đóng vai trò quan trọng trong chẩn đoán các biến chứng (viêm phổi cấp, giãn phế quản) và chẩn đoán phân biệt với các bệnh có triệu chứng tương tự. Chụp phế quản chỉ được sử dụng để chẩn đoán giãn phế quản. Nội soi phế quản có tầm quan trọng lớn trong chẩn đoán viêm phế quản mãn tính và phân biệt với các bệnh có biểu hiện lâm sàng tương tự. Nó xác nhận sự hiện diện của một quá trình viêm; làm rõ bản chất của viêm (chẩn đoán viêm phế quản xuất huyết hoặc xơ chỉ được thực hiện sau nghiên cứu này); bộc lộ các rối loạn chức năng của cây khí quản (đặc biệt quan trọng là xác định tình trạng xẹp thở - rối loạn vận động của khí quản và phế quản lớn); giúp xác định các tổn thương hữu cơ của cây phế quản. Ngoài ra, nội soi phế quản cho phép bạn lấy các chất trong phế quản hoặc nước rửa để nghiên cứu vi sinh, ký sinh trùng và tế bào học. Nghiên cứu chức năng của hô hấp ngoài được thực hiện để xác định các rối loạn hạn chế và tắc nghẽn của thông khí phổi. Theo biểu đồ xoắn khuẩn, chỉ số Tiffno được tính toán (tỷ lệ giữa thể tích thở ra cưỡng bức trong 1 s - FEV1 dung tích sống của phổi - VC tính theo phần trăm) và chỉ số vận tốc khí - PSV (tỷ số giữa thông khí tối đa của phổi - MVL trên VC). Với sự phát triển của hội chứng tắc nghẽn, có sự giảm các chỉ số tốc độ tuyệt đối của hô hấp ngoài (MVL và FEV1), vượt quá mức độ giảm VC; chỉ số Tiffno giảm và sức đề kháng của phế quản khi hết hạn tăng lên. Theo phương pháp đo lượng khí, sức mạnh thở ra chiếm ưu thế so với sức mạnh thở ra được phát hiện là một dấu hiệu sớm của tắc nghẽn phế quản. Có thể xác định các vi phạm về tính bảo quản của phế quản ở các cấp độ khác nhau của cây phế quản với sự trợ giúp của các máy chụp khí quản đặc biệt, giúp có được đường cong "lưu lượng - thể tích". Tắc nghẽn ngoại vi được đặc trưng bởi sự giảm đáng kể của đường cong lưu lượng-thể tích ở khu vực có thể tích thấp. Đánh giá chung về sức cản của phế quản và thể tích phổi cũng giúp xác định mức độ tắc nghẽn. Trong trường hợp tắc nghẽn ở mức độ của các phế quản lớn, có sự gia tăng thể tích tồn dư của phổi (RLVT), và tổng dung tích phổi (TLC) không tăng. Với tắc nghẽn ngoại vi, sự gia tăng TRL đáng kể hơn và sự gia tăng TRL được quan sát thấy. Để xác định tỷ lệ co thắt phế quản trong tổng tỷ lệ tắc nghẽn phế quản, thông khí và cơ học hô hấp được nghiên cứu sau một loạt các thử nghiệm dược lý. Sau khi hít khí dung giãn phế quản, hiệu suất thông khí được cải thiện khi có thành phần co cứng của tắc nghẽn đường thở. Chụp X quang bằng đồng vị phóng xạ 133Xe được thực hiện để phát hiện tình trạng thông khí không đều liên quan đến tắc nghẽn các phế quản nhỏ. Đây là dấu hiệu chẩn đoán sớm nhất của loại tắc nghẽn phế quản này. Điện tâm đồ là cần thiết để phát hiện phì đại tâm thất phải và tâm nhĩ phải phát triển với tăng áp động mạch phổi. Phát hiện độ lệch rõ rệt của trục QRS sang phải, sự dịch chuyển của vùng chuyển tiếp sang trái (R / S <1 ở V4-V6), ECG kiểu S được phát hiện; sóng P sắc nét cao trong các đạo trình VF, III, II. Xét nghiệm máu lâm sàng cho thấy tăng hồng cầu thứ phát do thiếu oxy mãn tính với sự phát triển của suy phổi nặng. Các chỉ số "giai đoạn cấp tính" được thể hiện ở mức độ vừa phải: ESR bình thường hoặc tăng vừa phải, tăng bạch cầu ít, cũng như sự chuyển dịch công thức bạch cầu sang trái. Như bằng chứng về các biểu hiện dị ứng, tăng bạch cầu ái toan là có thể xảy ra. Việc nghiên cứu các chất trong đờm và phế quản giúp xác định mức độ nghiêm trọng của tình trạng viêm. Với tình trạng viêm nặng, các chất bên trong là mủ hoặc mủ nhầy, chứa nhiều bạch cầu trung tính và đại thực bào đơn lẻ, các tế bào bị biến đổi loạn dưỡng của biểu mô có lông và vảy được biểu thị kém. Đối với tình trạng viêm vừa phải, các nội dung gần với chất nhầy; số lượng bạch cầu trung tính giảm, số lượng đại thực bào, chất nhầy và tế bào biểu mô phế quản tăng lên. Với tình trạng viêm nhẹ, thành phần trong phế quản là chất nhầy, các tế bào bong vảy của biểu mô và phế quản chiếm ưu thế; đại thực bào và bạch cầu trung tính rất ít. Kiểm tra vi sinh đối với đờm và các chất trong phế quản là rất quan trọng để xác định căn nguyên của các đợt cấp của viêm phế quản mãn tính và lựa chọn liệu pháp kháng sinh. Chẩn đoán phân biệt. Bảng 10 Tiêu chuẩn chẩn đoán phân biệt cho CB
Điều trị. Bao gồm một tập hợp các biện pháp khác nhau trong giai đoạn trầm trọng và thuyên giảm của bệnh. Trong giai đoạn trầm trọng của bệnh mãn tính, hai hướng điều trị được phân biệt: etiotropic và pathogen. Điều trị căn nguyên nhằm mục đích loại bỏ quá trình viêm trong phế quản: điều trị bằng thuốc kháng sinh, thuốc sulfanilamide, thuốc sát trùng, phytoncide, ... Điều trị bắt đầu bằng kháng sinh thuộc dòng penicillin (penicillin, ampicillin) hoặc nhóm cephalosporin (cefamesin) , tseporin), và trong trường hợp không có tác dụng, kháng sinh của nhóm được sử dụng dự trữ (gentamicin, v.v.). Đường dùng được ưu tiên nhất là đặt trong khí quản (khí dung hoặc bơm đầy ống thanh quản qua ống nội soi phế quản). Điều trị di truyền bệnh là nhằm cải thiện thông khí phổi; phục hồi sự thông thương của phế quản; kiểm soát tăng áp động mạch phổi và suy thất phải. Việc phục hồi thông khí phổi, ngoài việc loại bỏ quá trình viêm trong phế quản, được tạo điều kiện thuận lợi bằng liệu pháp oxy và liệu pháp tập thể dục. Điều chính trong điều trị viêm phế quản mãn tính - phục hồi sự thông thoáng của phế quản - đạt được bằng cách cải thiện hệ thống thoát nước và loại bỏ co thắt phế quản. Để cải thiện sự thoát nước của phế quản, thuốc long đờm được kê đơn (uống kiềm nóng, nước sắc của thảo mộc, mukaltin, v.v.), thuốc tiêu nhầy (acetylcysteine, bromhexine; với bài tiết nhớt có mủ - khí dung của các enzym phân giải protein - chymopsin, trypsin); nội soi phế quản trị liệu được sử dụng. Để loại bỏ co thắt phế quản, eufillin được sử dụng (tiêm tĩnh mạch, trong thuốc đạn, viên nén), ephedrin, atropine; có thể chỉ định đơn lẻ trong một bình xịt thuốc cường giao cảm: fenoterol, orciprenaline sulfat (asthmopenta) và một loại thuốc nội địa mới "Soventol", thuốc kháng cholinergic: atrovent, troventol. Các chế phẩm hiệu quả của aminophylline kéo dài (teopec, teodur, theobelong, v.v.) - 2 lần một ngày. Trong trường hợp không có tác dụng của liệu pháp như vậy, liều lượng nhỏ corticosteroid được dùng bằng đường uống (10-15 mg prednisolon mỗi ngày) hoặc tiêm trong khí quản (hỗn dịch hydrocortisone - 50 mg). Như một liệu pháp bổ sung, chỉ định: 1) thuốc chống ho: với ho không hiệu quả - libexin, tusuprex, bromhexine, với ho khan - codeine, dionin, stoptussin; 2) Thuốc tăng sức đề kháng của cơ thể: vitamin A, C, nhóm B, thuốc kích thích sinh học. Hiện nay, trong điều trị viêm phế quản mãn tính, ngày càng sử dụng nhiều thuốc kích hoạt miễn dịch: T-activin hoặc thymalin (100 mg tiêm dưới da trong 3 ngày); bên trong - catergen, natri nucleinate hoặc pentoxyl (trong vòng 2 tuần), levamisole (decaris). Điều trị vật lý trị liệu: kê thuốc xông hơi, điện di canxi clorua, thạch anh lên vùng ngực, xoa bóp lồng ngực và tập thở. Với tình trạng viêm phế quản vừa và nặng, cùng với điều trị chống tái phát và điều dưỡng, nhiều bệnh nhân buộc phải liên tục dùng thuốc hỗ trợ. Điều trị duy trì nhằm cải thiện sự thông thoáng của phế quản, giảm tăng áp động mạch phổi và chống suy thất phải. Các loại thuốc tương tự được kê đơn như trong giai đoạn đợt cấp, chỉ với liều lượng nhỏ hơn, trong các khóa học. Dự báo. Tiên lượng cho sự phục hồi hoàn toàn là không thuận lợi. Tiên lượng kém thuận lợi nhất là CB tắc nghẽn và CB với tổn thương chủ yếu ở phế quản xa, nhanh chóng dẫn đến suy phổi phát triển và hình thành bệnh tâm phế. Tiên lượng thuận lợi nhất là CB nông (catarrhal) không bị tắc nghẽn. BÀI GIẢNG SỐ 8. Các bệnh về hệ hô hấp. Viêm phổi Viêm phổi là một bệnh truyền nhiễm và viêm cấp tính có tính chất khu trú, trong đó các bộ phận hô hấp và mô liên kết kẽ của phổi tham gia vào quá trình bệnh lý. Phân loại của E. V. Gembitsky (1983). Theo căn nguyên: 1) vi khuẩn (chỉ ra mầm bệnh); 2) virus (chỉ ra mầm bệnh); 3) ăn mòn; 4) rickettsial; 5) mycoplasma; 6) nấm; 7) hỗn hợp; 8) nhiễm trùng-dị ứng; 9) căn nguyên không rõ. Theo cơ chế bệnh sinh: 1) nguyên phát (quá trình viêm cấp tính độc lập); 2) thứ phát (biến chứng của các bệnh của hệ thống tim mạch với rối loạn tuần hoàn trong tuần hoàn phổi, các bệnh mãn tính về thận, hệ thống máu, chuyển hóa, các bệnh truyền nhiễm hoặc phát triển trên nền các bệnh mãn tính đường hô hấp). Đặc điểm lâm sàng và hình thái: 1) nhu mô (đối với viêm phổi do phế cầu khuẩn): thể nang; đầu mối; 2) kẽ. Theo nội địa hóa và mức độ: đơn phương; song phương. Theo mức độ nghiêm trọng: cực kỳ nghiêm trọng; nặng; vừa phải; nhẹ và phá thai. Hạ lưu: sắc bén; kéo dài (X quang và phân giải lâm sàng của viêm phổi). Nguyên nhân. Hầu hết viêm phổi đều có nguồn gốc lây nhiễm. Viêm phổi dị ứng và những bệnh do yếu tố vật lý hoặc hóa học gây ra rất hiếm. Viêm phổi do vi khuẩn được chẩn đoán thường xuyên hơn ở người trung niên và người cao tuổi; viêm phổi do virus - ở người trẻ. Trong nguyên nhân gây viêm phổi do vi khuẩn nguyên phát, vai trò hàng đầu thuộc về phế cầu khuẩn. Trong dịch cúm, vai trò của các hiệp hội vi rút-vi khuẩn (thường là tụ cầu khuẩn), cũng như các vi sinh vật cơ hội, tăng lên. Trong viêm phổi thứ phát, nguyên nhân hàng đầu do vi khuẩn gram âm (klebsiella pneumoniae và trực khuẩn cúm) đảm nhiệm; trong trường hợp viêm phổi hít phải, tầm quan trọng của nhiễm trùng kỵ khí là rất lớn. Sinh bệnh học. Mầm bệnh truyền nhiễm từ bên ngoài xâm nhập vào các bộ phận hô hấp của phổi qua phế quản: hít phải và hít vào (từ vòm họng hoặc hầu họng). Bằng đường máu, mầm bệnh xâm nhập vào phổi chủ yếu trong viêm phổi thứ phát hoặc trong quá trình hình thành huyết khối của viêm phổi. Sự lây lan của nhiễm trùng bạch huyết với sự xuất hiện của viêm phổi chỉ được quan sát thấy ở những vết thương ở ngực. Ngoài ra còn có một cơ chế nội sinh cho sự phát triển của tình trạng viêm trong mô phổi, do sự kích hoạt của hệ vi sinh trong phổi. Vai trò của nó rất lớn trong bệnh viêm phổi thứ phát. Sự phát triển của bệnh viêm phổi được tạo điều kiện thuận lợi bởi các yếu tố bất lợi của môi trường bên ngoài và bên trong, dưới ảnh hưởng của nó là sự suy giảm sức đề kháng không đặc hiệu chung của cơ thể (ức chế thực bào, sản xuất vi khuẩn, v.v.) và ức chế cục bộ cơ chế bảo vệ (suy giảm thanh thải niêm mạc, giảm hoạt động thực bào của đại thực bào phế nang và bạch cầu trung tính, v.v.). Tầm quan trọng đáng kể trong cơ chế bệnh sinh của viêm phổi cũng gắn liền với các phản ứng dị ứng và tự dị ứng. Các chất hoại sinh và vi sinh vật gây bệnh, trở thành kháng nguyên, góp phần sản xuất các kháng thể cố định trên các tế bào của màng nhầy của đường hô hấp, nơi xảy ra phản ứng kháng nguyên-kháng thể, dẫn đến tổn thương mô và phát triển quá trình viêm. Khi có sự hiện diện của các yếu tố quyết định kháng nguyên thông thường của vi sinh vật và mô phổi, hoặc khi mô phổi bị tổn thương bởi vi rút, vi sinh vật, chất độc và các chất độc hại, dẫn đến biểu hiện các đặc tính kháng nguyên của nó, các quá trình tự dị ứng phát triển. Các quá trình này góp phần vào sự tồn tại lâu hơn của những thay đổi bệnh lý và quá trình kéo dài của bệnh. Ảnh lâm sàng. Các hội chứng chính: 1) nhiễm độc (suy nhược chung, mệt mỏi, đau đầu và đau cơ, khó thở, đánh trống ngực, xanh xao, chán ăn); 2) hội chứng thay đổi viêm nói chung (cảm giác nóng, ớn lạnh, sốt, thay đổi công thức máu trong giai đoạn cấp tính: tăng bạch cầu với sự thay đổi công thức bạch cầu sang trái, tăng ESR, mức fibrinogen, α2-globulin, sự xuất hiện của protein phản ứng C); 3) hội chứng thay đổi viêm trong nhu mô phổi (xuất hiện ho và khạc đờm, rút ngắn âm thanh bộ gõ), tăng giọng nói run và giãn phế quản, thay đổi tần số và tính chất của nhịp thở, xuất hiện ran ẩm, thay đổi X quang; 4) hội chứng liên quan đến các cơ quan và hệ thống khác. Mức độ nghiêm trọng của các biểu hiện này đặc trưng cho mức độ nghiêm trọng của quá trình viêm phổi (xem Bảng 11). Bảng 11 Các triệu chứng và diễn tiến của bệnh viêm phổi
Ở các giai đoạn khác nhau của quá trình viêm phổi, bệnh cảnh lâm sàng có thể thay đổi khi có thêm một số biến chứng: phổi và ngoài phổi. Phổi: hình thành áp xe; viêm màng phổi (para- và siêu âm), ít thường xuyên hơn - tràn khí màng phổi; sự gia nhập của một thành phần hen suyễn, sự hình thành của phù phổi và sự phát triển của suy hô hấp cấp tính là có thể. Biến chứng ngoài phổi: sốc nhiễm độc (với các triệu chứng mạch máu cấp, thất trái cấp và suy thận, loét màng nhầy của đường tiêu hóa và chảy máu, phát triển đông máu nội mạch lan tỏa; viêm cơ tim do nhiễm trùng-dị ứng; viêm nội tâm mạc nhiễm trùng; viêm màng ngoài tim; viêm màng não hoặc viêm não màng não; viêm thận; viêm gan Trong viêm phổi thể nặng, rối loạn tâm thần do nhiễm độc có thể phát triển và trong viêm phổi toàn bộ hợp lưu - tim phổi cấp tính. Những phàn nàn chính của bệnh nhân bị viêm phổi: ho, tạo đờm, đau ngực, trầm trọng hơn khi thở và ho, khó thở, suy giảm sức khỏe tổng quát, sốt. Ho có thể khô hoặc có đờm (nhầy, nhầy, mủ, nhầy, máu). Đờm "rỉ" là đặc trưng của viêm phổi thùy, có máu - đối với viêm phổi do Klebsiella (trực khuẩn Fridlander) và viêm phổi do virus; đờm có máu mủ cho thấy viêm phổi có nguồn gốc liên cầu. Ho dai dẳng kèm theo một ít đờm nhầy có thể quan sát được khi bị viêm phổi do nấm, cũng được đặc trưng bởi cảm giác đau họng. Đau ở một bên, trầm trọng hơn khi thở sâu và ho, là đặc điểm của viêm phổi do phế cầu khuẩn thùy, cũng như sự tham gia của màng phổi vào quá trình bệnh lý. Với sự bản địa hóa của viêm phổi ở các phần dưới của phổi và sự tham gia của màng phổi hoành trong quá trình này, cơn đau có thể lan đến khoang bụng, mô phỏng hình ảnh của một cơn đau bụng cấp tính. Nếu phân đoạn trên hoặc dưới của cây sậy bên trái có liên quan đến quá trình này, các cơn đau sẽ khu trú ở vùng tim. Ở 25% bệnh nhân, phàn nàn về khó thở là một trong những nguyên nhân chính, đặc biệt là với bệnh viêm phổi phát triển trên nền các bệnh hô hấp mãn tính và suy tim. Mức độ nghiêm trọng của khó thở tăng lên song song với việc vi phạm sức khỏe chung. Các triệu chứng nhiễm độc nặng là đặc trưng nhất của viêm phổi cornitic và mycoplasmal, và cũng được quan sát thấy trong viêm phổi do tụ cầu, cúm và phế cầu (croupous). Bệnh nhân có thể bị rối loạn do ớn lạnh và nhiệt độ cơ thể tăng lên đến sốt. Trong bối cảnh chung của tình trạng say và nhiệt độ sốt, các triệu chứng cục bộ xuất hiện. Chẩn đoán. Để chẩn đoán nguyên nhân, việc đánh giá chính xác các triệu chứng của bệnh ngay từ đầu là rất quan trọng. Khàn giọng hoặc không nói được là đặc điểm của bệnh viêm phổi do virus á cúm gây ra. Lạch cạch, đau mắt, đau họng khi nuốt, chảy nhiều dịch từ mũi mà không thay đổi các bộ phận khác của đường hô hấp xảy ra với viêm phổi do adenovirus. Ý nghĩa nhất đối với chẩn đoán là sự hiện diện của hội chứng thay đổi viêm trong mô phổi. Hội chứng này bao gồm các triệu chứng sau: 1) thở chậm của bên ngực bị ảnh hưởng; 2) rút ngắn âm thanh bộ gõ trong khu vực hình chiếu của tổn thương ở mức độ lớn hơn hoặc nhỏ hơn; 3) tăng giọng nói run và giãn phế quản trong cùng một khu vực; 4) thay đổi bản chất của hơi thở (khó thở, phế quản, suy yếu, v.v.); 5) sự xuất hiện của tiếng ồn bệnh lý đường hô hấp (ẩm ướt, nổi bọt mịn và crepitus). Bản chất của hơi thở có thể thay đổi theo nhiều cách khác nhau. Trong giai đoạn đầu của bệnh viêm phổi thể phổi, nhịp thở có thể yếu đi, thở ra kéo dài; trong giai đoạn gan hóa, cùng với sự gia tăng độ chói của âm thanh gõ, người ta nghe thấy tiếng thở của phế quản; với sự phân giải của tiêu điểm khí nén với sự giảm độ âm ỉ của bộ gõ, hơi thở trở nên khó khăn. Với bệnh viêm phổi khu trú, các triệu chứng thường xuyên nhất là thở khó và ẩm ướt, phát ra những tiếng ran có bọt mịn. Tuy nhiên, với bệnh viêm phổi trung ương, dữ liệu thực thể được trình bày rất kém và chỉ có thể nhận biết được bệnh viêm phổi sau khi kiểm tra bằng tia X. Bệnh bụi phổi Mycoplasma được phân biệt bởi sự khan hiếm của dữ liệu vật lý. Nhiễm độc nặng, kết hợp với một số rất nhỏ thở khò khè, được quan sát thấy trong viêm phổi do Klebsiella pneumonia. Trong một số trường hợp, trong quá trình nghe tim mạch, có thể xuất hiện một số lượng lớn các âm trầm và âm bổng khô khan, không đặc trưng của hội chứng thâm nhiễm viêm, có thể xuất hiện trước. Điều này xảy ra với bệnh viêm phổi đã phát triển trên nền của viêm phế quản mãn tính; viêm phổi do dính Pfeiffer; trong trường hợp gia nhập viêm phổi của một thành phần dị ứng. Các triệu chứng giúp chẩn đoán căn nguyên: 1) việc phát hiện một đốm nhỏ, như với bệnh ban đào, phát ban kết hợp với nổi hạch là đặc điểm của nhiễm trùng adenovirus; 2) sự mở rộng cục bộ của các hạch bạch huyết cho thấy viêm phổi quanh ổ; 3) viêm phổi do nấm kết hợp với tổn thương niêm mạc, da và móng tay; 4) hội chứng gan mật và vàng da nhẹ được tìm thấy trong bệnh tràn khí màng phổi và Curickettsial; 5) Đối với bệnh viêm phổi thể phổi điển hình, biểu hiện của bệnh nhân là đặc trưng: mặt tái nhợt, đỏ mặt nóng bừng ở một bên tổn thương, nổi mụn nước, sưng cánh mũi khi thở. Phương pháp quan trọng nhất để làm rõ sự hiện diện của bệnh viêm phổi và mức độ tham gia của mô phổi trong quá trình này là chụp ảnh quang tuyến khung lớn và chụp X-quang các cơ quan trong lồng ngực. Bệnh bụi phổi do tụ cầu được phân biệt bằng một phân đoạn rõ ràng của tổn thương phổi với sự tham gia của một số phân đoạn trong quá trình này. Dấu hiệu X quang đặc trưng của chúng là sự hình thành nhiều khoang trong phổi của loại phế nang vào ngày thứ 5-7 kể từ khi bệnh khởi phát, và sau đó - các khoang hoại tử với sự hiện diện của dịch. Không giống như áp xe thực sự, cấu hình và số lượng các khoang thay đổi nhanh chóng. Tổn thương thùy là biểu hiện của bệnh viêm phổi hoặc viêm phổi do Klebsiella. Thùy trên, chủ yếu là phổi phải, thường bị ảnh hưởng nhất. Chụp X-quang cho thấy có tràn dịch trong khoang màng phổi. Thường thì tràn dịch như vậy xảy ra với viêm phổi do liên cầu, với viêm phổi do que của Pfeiffer, khu trú ở thùy dưới và ở 2/3 số bệnh nhân có nhiều hơn một thùy phổi. Dữ liệu kiểm tra X-quang đặc biệt quan trọng trong việc phát hiện viêm phổi với những thay đổi nhẹ về nghe tim (viêm phổi kẽ và viêm phổi). Trong một số trường hợp, để làm rõ chẩn đoán, chỉ định chụp cắt lớp và chụp cắt lớp, giúp làm rõ chẩn đoán trong các trường hợp thâm nhiễm thoái triển chậm, có diễn biến phức tạp (áp xe, tràn dịch khoang màng phổi). Chúng được sử dụng để loại trừ các quá trình bệnh lý khác với các biểu hiện lâm sàng và X quang tương tự. Chụp phế quản cho thấy các khoang phân hủy trong mô phổi, cũng như sự hiện diện của giãn phế quản, xung quanh đó, trong đợt cấp, có thể xảy ra các thay đổi thâm nhiễm (viêm phổi quanh ổ). Trong chẩn đoán viêm phổi nhồi máu, một nghiên cứu về hạt nhân phóng xạ về lưu lượng máu phổi đóng một vai trò nhất định, cho thấy những vi phạm của nó. Xét nghiệm vi khuẩn học đờm (hoặc rửa phế quản) trước khi kê đơn thuốc kháng sinh giúp phát hiện mầm bệnh và xác định độ nhạy cảm của nó với thuốc kháng sinh. Không phải lúc nào vi sinh vật cũng được xác định là tác nhân gây bệnh viêm phổi. Có thể chẩn đoán căn nguyên chính xác hơn bằng các nghiên cứu miễn dịch học: phản ứng cố định bổ thể (RCC) và phản ứng ức chế đông máu (HITA) với các kháng nguyên vi khuẩn và virus. Trong chẩn đoán viêm phổi do vi rút và vi rút-vi khuẩn, các nghiên cứu về vi-rút và huyết thanh học là rất quan trọng (kết quả của nghiên cứu nuôi cấy đờm, bao gồm xét nghiệm sinh học trên chuột, phương pháp nuôi cấy vi-rút trong phôi gà đang phát triển, phương pháp miễn dịch huỳnh quang, a phương pháp huyết thanh học sử dụng huyết thanh bắt cặp chống lại vi rút, chú trọng chỉ tăng 4 lần hiệu giá kháng thể). Xét nghiệm đờm giúp làm rõ bản chất của viêm phổi. Một số lượng lớn bạch cầu ái toan cho thấy các quá trình dị ứng, sự hiện diện của các tế bào không điển hình cho thấy viêm phổi có nguồn gốc ung thư; Mycobacterium tuberculosis được tìm thấy trong bệnh lao; sợi đàn hồi - bằng chứng về sự xẹp của mô phổi. Với bệnh viêm phổi do nấm, cùng với việc phát hiện nấm còn thiếu hệ sinh mủ do tác dụng ức chế các chất thải của nấm. Theo kính hiển vi soi đờm nhuộm Gram, chúng ta có thể nói về vi sinh vật Gram âm hoặc Gram dương sống trong phế quản ngay từ ngày đầu tiên bệnh nhân đến bệnh viện. Mức độ nghiêm trọng của quá trình viêm được đánh giá bởi mức độ nghiêm trọng của các thông số máu ở giai đoạn cấp tính và động lực của chúng (tăng bạch cầu với sự thay đổi công thức bạch cầu, tăng ESR, tăng hàm lượng α2-globulin, fibrinogen, sự xuất hiện của SRV, sự gia tăng mức độ axit sialic). Với một đợt viêm phổi kéo dài và sự phát triển của các biến chứng, phản ứng miễn dịch của cơ thể được nghiên cứu. Giảm miễn dịch thể dịch (IgM) và tế bào (bạch cầu di chuyển chậm, thay đổi trong các xét nghiệm đặc trưng cho hệ thống tế bào lympho T) đòi hỏi liệu pháp điều hòa miễn dịch. Điều trị. Ngay sau khi chẩn đoán, cần bắt đầu điều trị bằng etiotropic cho bệnh viêm phổi. Những ý tưởng thực nghiệm về mầm bệnh có thể có là rất quan trọng, vì việc kiểm tra vi khuẩn đờm được thực hiện trong một thời gian khá dài và ở hầu hết bệnh nhân, ngay cả với cách tiếp cận hiện đại đối với nghiên cứu này, cho kết quả không chắc chắn và đôi khi sai sót. Hiện tại, penicillin đã không còn quan trọng như một loại thuốc được lựa chọn trong điều trị viêm phổi. Điều này là do căn nguyên có ý nghĩa đối với sự phát triển của bệnh viêm phổi, ngoài phế cầu và Haemophilus influenzae, là các vi sinh vật nội bào bắt buộc - Mycoplasma pneumoniae và Chlamydia pneumoniae, có khả năng kháng lại tác dụng diệt khuẩn của các kháng sinh thuộc nhóm β-lactam. Không thể bỏ qua thực tế là quá mẫn cảm với các loại thuốc này nhanh chóng phát triển ở bệnh nhân. Liên quan đến những điều đã nói ở trên, trong điều trị viêm phổi, người ta chú ý nhiều đến macrolid, đã được chứng minh là có hiệu quả không chỉ chống lại phế cầu mà còn chống lại Mycoplasma pneumoniae, Chlarnydia pneumoniae. Tuy nhiên, điều quan trọng là không nên bỏ qua thực tế rằng erythromycin, là thuốc tiêu chuẩn của nhóm thuốc này do tính ổn định thấp trong môi trường axit (và do đó sinh khả dụng thấp), cũng như sự phổ biến rộng rãi của các chủng phế cầu khuẩn kháng thuốc. đối với erythromycin, đang mất đi giá trị lâm sàng. Là các loại thuốc được lựa chọn, nó đã được thay thế bằng các loại thuốc khác thuộc nhóm macrolide - azithromycin, roxithromycin, rovamycin, v.v. Một số macrolid cũng được sử dụng để uống và tiêm (ví dụ, rovamycin). Kết quả là, việc sử dụng chúng là hợp lý trong quá trình nghiêm trọng của quá trình viêm ở phổi (ví dụ, ban đầu rovamycin được tiêm tĩnh mạch trong 2-3 ngày, và sau đó, với động lực tích cực của quá trình bệnh lý, bệnh nhân chuyển sang lấy thuốc này bên trong). Lợi thế của rovamycin là không thể phủ nhận, vì nó không tương tác với theophylin, đồng thời ngăn ngừa khả năng quá liều của những loại thuốc này, vì theophylin và rovamycin được sử dụng cùng nhau trong điều trị bệnh nhân mắc bệnh phổi tắc nghẽn mãn tính. Người ta cũng biết rằng phân nhóm macrolide này (macrolide 16-membered) là những loại thuốc có mức độ tác dụng phụ tối thiểu. Ở những bệnh nhân trên 65 tuổi, do không đồng nhất về phổ căn nguyên của bệnh viêm phổi và đồng thời với các bệnh phổi tắc nghẽn mãn tính, các penicilin bán tổng hợp có thể được sử dụng cho liệu pháp kháng sinh ban đầu và nếu không có tác dụng tích cực sau liệu pháp này đối với 3-4 ngày, việc sử dụng cephalosporin là hợp lý. Điều quan trọng cần nhớ là phổ tác dụng của một số cephalosporin thế hệ I và II là các vi sinh vật gram dương và gram âm, và các cephalosporin thế hệ III tác động chủ yếu lên các mầm bệnh gram âm. Các cephalosporin thế hệ I được đại diện bởi cephalothin (keflin), cefazolin (kefzol), v.v. Các thuốc thế hệ II bao gồm cefuroxime (ketocef), cefoxitin (boncefin) và các loại khác. Các cephalosporin thế hệ III: cefotaxime (ceefobidoran), cefoperazon (cftriobid) longacef). Viêm phổi do thở ra có liên quan đến hệ vi sinh kỵ khí hoặc gram âm, điều này quyết định việc sử dụng aminoglycosid hoặc cephalosporin thế hệ III kết hợp với metronidazole-semisuccinate (500 mg tiêm tĩnh mạch 2-3 lần một ngày). Trạng thái suy giảm miễn dịch cũng ảnh hưởng đến bản chất của các loại thuốc được lựa chọn, trong trường hợp này phụ thuộc vào bản chất của mầm bệnh. Trong những trường hợp như vậy, chương trình được áp dụng bao gồm aminoglycoside và cephalosporin hiện đại. Thời gian điều trị kháng sinh hiệu quả cho một bệnh nhân bị viêm phổi là 7-10 ngày. Khi kê đơn điều trị, cần lưu ý rằng trong 7-15% trường hợp có thể không có tác dụng từ liệu pháp này. Điều này cho thấy sự cần thiết phải thay thế thuốc kháng sinh, dựa trên kết quả của một nghiên cứu vi sinh vật. Một lựa chọn khác là sử dụng các loại thuốc thay thế, được gọi là thuốc kháng sinh lựa chọn thứ hai: cephalosporin hiện đại, imipenem, monobactams, fluoroquinolones. Fluoroquinolon (ofloxacin, pefloxacin, ciprofloxacin) có hiệu quả chống lại các mầm bệnh gram âm, bao gồm Pseudomonas aeruginosa, và một số cầu khuẩn gram dương (Staphylococcus aureus), nhưng không hoạt động khi tiếp xúc với vi khuẩn kỵ khí. Fluoroquinolones có thể được coi là một chất thay thế cho macrolid trong các trường hợp nhiễm chlamydia, legionella và mycoplasma. Kháng sinh monobactam ở dạng hiện đại của chúng là aztreonam (azactam), hoạt động chủ yếu chống lại vi khuẩn gram âm (Salmonella, Shigella, Proteus, Escherichia coli, Klebsiella, v.v.); và cũng ổn định dưới tác dụng của β-lactamase. Imipenem - một loại thuốc kháng khuẩn thuộc nhóm carbapenem, chỉ được kê đơn kết hợp với cilastatin, có tác dụng ức chế sự chuyển hóa của imipenem. Thuốc có hiệu quả cao đối với nhiều loại vi khuẩn kỵ khí, cầu khuẩn gram dương và gram âm. Liều lượng thuốc kháng sinh được sử dụng trong điều trị viêm phổi. 1) Penicillin: benzylpenicillin (500-000 IU tiêm tĩnh mạch mỗi 1-000 giờ hoặc 000-6 IU tiêm bắp mỗi 8 giờ), ampicillin (500-000-1 g tiêm bắp mỗi 000-000 giờ hoặc 4 g mỗi 0,5 giờ tiêm tĩnh mạch), amoxicillin (1,0-2,0 g mỗi 6 giờ uống hoặc 8-0,5 g mỗi 6-0,5 giờ tiêm bắp, tiêm tĩnh mạch), oxacillin (1,0 g mỗi 8-0,5 giờ uống, tiêm bắp, tiêm tĩnh mạch). 2) Cephalosporin: thế hệ I - cephalothin (keflin) (0,5-2,0 g mỗi 4-6 giờ tiêm bắp, tiêm tĩnh mạch), cefazolin (kefzol) (0,5-2,0 g, cứ 8 giờ tiêm bắp, tiêm tĩnh mạch), thế hệ II - cefuroxime (zinacef , ketocef) (0,75-1,5 g mỗi 6-8 giờ tiêm bắp, tiêm tĩnh mạch), thế hệ III - cefotaxime (claforan) (1,0-2,0 g, tối đa lên đến 12 g / ngày cứ sau 12 giờ tiêm bắp, tiêm tĩnh mạch), ceftriaxone (longacef, rocefin) (1,0-2,0-4,0 g mỗi 24 giờ tiêm bắp, tiêm tĩnh mạch). 3) Aminoglycosid: gentamycin (80 mg mỗi 12 giờ tiêm bắp, tiêm tĩnh mạch), amikacin (10-15 mg / kg mỗi 12 giờ tiêm bắp, tiêm tĩnh mạch), tobramycin (brulamycin) (3-5 mg / kg mỗi 8 giờ tiêm bắp, tiêm tĩnh mạch) . 4) Macrolide: erythromycin (0,5 g mỗi 6-8 giờ uống hoặc 0,5-1,0 g mỗi 6-8 giờ tiêm tĩnh mạch), rovamycin (3,0 triệu IU mỗi 8-12 giờ uống hoặc 1,5-3,0 triệu IU mỗi 8-12 giờ giờ IV). 5) Fluoroquinolones: pefloxacin (leflacin) (400 mg mỗi 12 giờ uống, IV), ciprofloxacin (cyprobay) (500 mg mỗi 12 giờ uống hoặc 200-400 mg mỗi 12 giờ tiêm tĩnh mạch), ofloxacin (zanocin, Thuế quan) (200 mg uống 12 giờ một lần). 6) Tetracyclines: doxycycline (vibramycin) (200 mg vào ngày 1, vào những ngày tiếp theo - 100 mg mỗi 24 giờ bằng đường uống), minocycline (minocin) (200 mg vào ngày 1, vào những ngày tiếp theo - 100 mg mỗi 12 giờ bằng đường uống), aztreonam (azactam) (1,0-2,0 g mỗi 8-12 giờ), imipenem / cilstatin (thienam) (500 mg mỗi 6-8 giờ tiêm bắp). Điều quan trọng nữa là, theo quy luật, quá trình kéo dài hoặc tiến triển của bệnh là do liệu pháp kháng sinh ban đầu không đầy đủ. Tuy nhiên, bên cạnh đó còn có một số nguyên nhân tại chỗ và toàn thân dẫn đến quá trình viêm nhiễm kéo dài và dai dẳng ở phổi: đó là tắc nghẽn đường thở tại chỗ (ung thư, u tuyến, tắc nghẽn niêm mạc ...); giãn phế quản (bẩm sinh, mắc phải); bệnh xơ nang; khiếm khuyết hệ thống miễn dịch (mắc phải); chọc hút tái phát (achalasia, ung thư thực quản, v.v.); kích hoạt nhiễm trùng lao tiềm ẩn; phát triển áp xe phổi; liệu pháp kháng sinh không đầy đủ. BÀI GIẢNG SỐ 9. Các bệnh về đường tiêu hóa. Các bệnh về thực quản. Viêm thực quản và loét dạ dày tá tràng của thực quản 1. Viêm thực quản cấp Viêm thực quản cấp là tình trạng tổn thương viêm niêm mạc thực quản kéo dài từ vài ngày đến 2 - 3 tháng. Nguyên nhân và sinh bệnh học. Yếu tố căn nguyên: bệnh truyền nhiễm, chấn thương, bỏng, ngộ độc, dị ứng, sai sót về dinh dưỡng. Trong số các tác nhân truyền nhiễm, đặc trưng nhất của viêm thực quản cấp là bạch hầu, ban đỏ, thương hàn và sốt phát ban, cúm, parainfluenza, nhiễm adenovirus, quai bị. Các yếu tố gây hại vật lý và hóa học được thể hiện bằng bức xạ ion hóa, bỏng hóa chất, thực phẩm nóng và rất lạnh, và gia vị. Phân loại. Không có sự phân loại duy nhất. Có thể sử dụng cách phân loại viêm thực quản cấp tính. Về hình thái, các loại viêm thực quản cấp tính được liệt kê được phân biệt: catarrhal, phù nề, ăn mòn, giả mạc, xuất huyết, tróc vảy, hoại tử, tĩnh mạch. Theo căn nguyên: truyền nhiễm, hóa học, vật lý, bệnh lý. Theo giai đoạn nội soi: thứ nhất - phù nề và sung huyết niêm mạc, thứ hai - sự xuất hiện của vết ăn mòn đơn lẻ trên đỉnh của nếp gấp niêm mạc phù nề, thứ ba - phù nề và sung huyết đáng kể của niêm mạc với các ổ niêm mạc bị xói mòn và chảy máu, thứ 1 - " khóc ”- màng nhầy bị xói mòn lan rộng, chảy máu khi chạm nhẹ vào ống nội soi. Ảnh lâm sàng. Viêm thực quản Catarrhal là dạng viêm thực quản cấp tính phổ biến nhất. Nó xảy ra do những sai sót về dinh dưỡng: khi ăn đồ cay, lạnh, nóng, bị thương nhẹ, bỏng do rượu. Biểu hiện lâm sàng bằng cảm giác nóng rát và đau sau xương ức, buộc bệnh nhân phải từ chối thức ăn trong vài ngày. Nội soi ghi nhận viêm thực quản độ I-II, X-quang - tăng vận động của thực quản. Viêm thực quản ăn mòn xảy ra với các bệnh truyền nhiễm (vi khuẩn, sốt phát ban, nhiễm trùng huyết, các quá trình nấm) và dị ứng. Nó cũng xuất hiện với các vết bỏng do hóa chất và chấn thương thực quản. Trên thực tế, dạng viêm thực quản này là một giai đoạn tiến triển của viêm thực quản catarrhal. Hình ảnh lâm sàng chính bao gồm các triệu chứng của bệnh cơ bản. Các triệu chứng lâm sàng tương tự như của viêm thực quản catarrhal: đau tức ngực khi thức ăn đi qua; ợ chua, ợ hơi, tăng tiết nước bọt, mùi hôi từ miệng (cacosmia). Nội soi xác định dấu hiệu viêm thực quản độ II-III. Kiểm tra mô học cho thấy xung huyết, phù nề niêm mạc, xuất huyết, xói mòn. Kiểm tra bằng tia X cho thấy có nhiều chất nhầy trong thực quản, sự tái cấu trúc của sự giảm bớt với sự hình thành của các kho bari phẳng có hình dạng dọc dài tới 1 cm và tăng vận động của các thành thực quản. Viêm thực quản xuất huyết là một dạng lâm sàng hiếm gặp của viêm thực quản ăn mòn. Căn nguyên cũng giống như trong viêm thực quản ăn mòn. Hội chứng đau dữ dội và buồn nôn là điển hình về mặt lâm sàng. Nội soi phát hiện viêm độ III-IV với thành phần xuất huyết chiếm ưu thế. Có sự bong ra của màng nhầy chảy máu dưới dạng các dải mỏng hẹp. Viêm thực quản xơ (giả mạc). Các yếu tố căn nguyên trong đó là bệnh ban đỏ, bệnh bạch hầu, bệnh máu, bệnh nấm, ảnh hưởng của xạ trị. Phòng khám chủ yếu là chứng khó nuốt và đau dữ dội, trầm trọng hơn sau khi ăn, buồn nôn, nôn. Với chất nôn, màng fibrin được giải phóng, có thể có ho ra máu. Qua nội soi, trên các vùng niêm mạc bị tổn thương, người ta thấy các mảng xơ màu xám và xám vàng, hình thành bởi các lớp fibrin và mảnh vụn phủ trên bề mặt niêm mạc. Với sự từ chối của giả mạc, các vết ăn mòn phẳng từ từ lành được hình thành, đôi khi loét chảy máu. Sau một quá trình lây nhiễm nghiêm trọng, các chất tạo màng vẫn còn trong thực quản, chúng sẽ biến mất sau nhiều lần vệ sinh. Viêm thực quản màng (tróc vảy) do căn nguyên là hóa chất (bỏng thực quản), nhiễm trùng (nguyên nhân là nhiễm trùng huyết, zona, đậu mùa, nhiễm herpes toàn thân). Phòng khám của bệnh rất đa dạng - từ dạng nhẹ, được chẩn đoán bằng nội soi đến dạng nặng. Trong phòng khám viêm thực quản màng nặng, hội chứng nhiễm độc, khó nuốt và đau chiếm ưu thế. Có thể chảy máu, thủng thực quản, viêm trung thất, theo quy luật, kết thúc bằng cái chết. Trong kiểm tra nội soi, tổn thương tất cả các lớp của thực quản được quan sát thấy, biểu mô của chúng bị loại bỏ bởi các lớp. Khi bệnh cơ bản thuyên giảm, các vết rách màng trong hoặc thô đối xứng và không đối xứng đôi khi vẫn còn trong thực quản. Viêm thực quản hoại tử là một dạng viêm thực quản cấp tính hiếm gặp. Sự phát triển của nó được tạo điều kiện do giảm khả năng miễn dịch trong các bệnh nghiêm trọng như nhiễm trùng huyết, sốt thương hàn, nhiễm nấm Candida, suy thận giai đoạn cuối. Đặc điểm của phòng khám là khó nuốt đau đớn, nôn mửa, suy nhược toàn thân, chảy máu, thường xuyên phát triển thành viêm trung thất, viêm màng phổi, viêm phổi. Sau khi điều trị bệnh cơ bản, các chất xơ cứng vẫn còn trong thực quản, được chẩn đoán là những thay đổi tiền ung thư dễ nhận biết. Viêm thực quản nhiễm trùng là tình trạng viêm tại chỗ hoặc lan tỏa hiếm gặp của thành thực quản do nguyên nhân liên cầu hoặc xảy ra khi niêm mạc bị tổn thương bởi dị vật, có vết bỏng, vết loét và có thể lây lan từ các cơ quan lân cận. Đôi khi viêm thực quản tĩnh mạch cấp tính xảy ra như một biến chứng của bất kỳ dạng viêm thực quản cấp tính nào, dẫn đến sự hợp nhất có mủ của các thành thực quản. Sự sụp đổ của các bức tường đi kèm với sự đột phá của mủ vào mô của trung thất, sự phát triển của viêm trung thất, viêm màng phổi, viêm phế quản có mủ, viêm phổi, viêm cột sống, vỡ động mạch chủ hoặc các mạch lớn khác. Sự xâm nhập của nhiễm trùng kỵ khí có thể dẫn đến khí thũng trung thất hoặc tràn khí màng phổi tự phát. Bệnh cảnh lâm sàng đặc trưng bởi nhiễm độc nặng, sốt cao, đau sau xương ức và ở cổ, nôn mửa. Đi khám thì thấy cổ bị sưng tấy, khả năng vận động ở phần này bị hạn chế. Vị trí của đầu bị ép buộc, nghiêng về một bên. Bệnh thường chuyển biến thành viêm trung thất có mủ. Trong các xét nghiệm máu - tăng bạch cầu, ESR tăng tốc. Kiểm tra dụng cụ (X-quang, nội soi) trong giai đoạn cấp tính không được chỉ định. Trong giai đoạn sẹo, việc kiểm tra X-quang là bắt buộc do nguy cơ phát triển dị tật thô và hẹp thực quản. Điều trị. Nguyên tắc điều trị viêm thực quản cấp tính: etiotropic, bệnh sinh và triệu chứng. Điều trị nguyên nhân - điều trị bệnh cơ bản. Trong các bệnh truyền nhiễm phức tạp do viêm thực quản cấp tính, kháng sinh được sử dụng (đường tiêm). Với những thay đổi hoại tử và xuất huyết rõ rệt ở thực quản, nên hạn chế ăn trong 2-3 tuần. Trong giai đoạn này, dinh dưỡng qua đường tĩnh mạch, tiêm tĩnh mạch các sản phẩm thủy phân protein, hỗn hợp axit amin, intralipid, vitamin, liệu pháp giải độc được chỉ định. Sau khi giảm viêm, các loại thực phẩm tiết kiệm nhiệt và hóa học được kê đơn: sữa ấm, kem, súp rau củ, ngũ cốc lỏng. Để giảm các triệu chứng tại chỗ của viêm - giải pháp bên trong của tanin 1%, cổ áo - 2%, novocain - 1-2% trước bữa ăn. Chất làm se khít lỗ chân lông được đưa vào tư thế nằm ngang, đầu giường được hạ thấp. Trong trường hợp không có tác dụng của việc quản lý cục bộ các chế phẩm làm se, thuốc giảm đau không gây nghiện được kê đơn qua đường tiêm. Để giảm tác động của rối loạn vận động thực quản, thuốc tăng vận động (cerucal, raglan, cisapride) được sử dụng bằng đường uống trước bữa ăn. Với nhiều vết ăn mòn, các chế phẩm bismuth (denol, vikair), tiêm solcoseryl được chỉ định. Với viêm thực quản xuất huyết, phức tạp do chảy máu, các chế phẩm axit aminocaproic, vikasol, dicynone được sử dụng. Khi chảy máu ồ ạt, truyền máu hoặc huyết tương được chỉ định. Với tình trạng viêm thực quản có mủ, hoại tử, bệnh nhân cần được nuôi dưỡng bằng đường tĩnh mạch trong thời gian dài, điều trị ồ ạt với nhiều loại kháng sinh, và ổ áp xe được dẫn lưu. Sự thắt chặt thực quản được điều chỉnh bằng bougienage. Trong một số trường hợp hiếm hoi, phẫu thuật cắt dạ dày được đặt. Dự báo. Tiên lượng cho bệnh viêm thực quản do catarrhal và ăn mòn là thuận lợi. Sự biến mất tự nhiên của các triệu chứng viêm thực quản có thể xảy ra nếu căn bệnh tiềm ẩn được điều trị đầy đủ. Tiên lượng của viêm thực quản giả mạc, bong tróc và viêm thực quản là nghiêm trọng. Trong mọi trường hợp, tùy thuộc vào sự phục hồi của căn bệnh tiềm ẩn, viêm thực quản sẽ kết thúc bằng việc hình thành các vết sẹo hẹp, sau đó cần phải điều chỉnh. Bệnh nhân bị viêm thực quản nặng có biến chứng do hẹp thực quản không thể làm việc được. Phòng ngừa viêm thực quản cấp bao gồm chẩn đoán và điều trị đầy đủ, kịp thời các bệnh cơ bản. 2. Viêm thực quản mãn tính Viêm thực quản mãn tính là tình trạng viêm mãn tính của màng nhầy của thực quản kéo dài đến 6 tháng. Biến thể phổ biến nhất là viêm thực quản dạ dày tá tràng (viêm thực quản trào ngược), có thể biến chứng do loét dạ dày thực quản. Nguyên nhân và sinh bệnh học. Nguyên nhân chính gây bệnh là do dịch dạ dày trào ngược liên tục lên thực quản, đôi khi là dịch mật và ruột, tức là viêm thực quản dạ dày là tình trạng bỏng vô khuẩn thực quản do axit dạ dày gây ra. Trong cơ chế bệnh sinh của viêm thực quản trào ngược, việc trào ngược thành phần axit và vi phạm quá trình thanh lọc và làm rỗng thực quản khỏi nó là rất quan trọng. Tốc độ thanh thải của thực quản khỏi sự kích thích của hóa chất được gọi là độ thanh thải của thực quản. Với độ thanh thải bình thường, các chất tiết tích cực được bó bột đơn lẻ không gây ra viêm thực quản trào ngược. Thức ăn nóng, rượu bia, hút thuốc lá và các yếu tố ngoại sinh khác làm giảm độ thanh thải của thực quản. Những yếu tố này bao gồm thức ăn nhanh, trong đó một lượng không khí đáng kể được nuốt vào cùng với thức ăn. Chất lượng thực phẩm cũng rất quan trọng: thịt mỡ, mỡ lợn, mì ống, gia vị cay giúp trì hoãn quá trình di chuyển thức ăn khỏi dạ dày, dẫn đến trào ngược thức ăn vào thực quản. Thuốc làm giảm đáng kể trương lực của cơ thắt thực quản dưới và thúc đẩy trào ngược: thuốc đối kháng canxi, nitrat, thuốc giảm đau gây mê, thuốc kháng cholinergic, theophylline và các chất tương tự của nó, thuốc từ nhóm prostaglandin. Có năm tiêu chuẩn về khả năng gây bệnh của trào ngược trong nguồn gốc của viêm thực quản dạ dày: tần suất, thể tích, trào ngược, thành phần hóa học, tình trạng niêm mạc thực quản và độ nhạy cảm với một yếu tố hóa học (viêm thành mạch làm giảm độ nhạy cảm), tốc độ làm rỗng (độ thanh thải) , phụ thuộc chủ yếu vào nhu động hoạt động, hoạt động kiềm hóa nước bọt và chất nhầy. Sự xuất hiện của viêm thực quản trào ngược được thúc đẩy bởi thoát vị của cơ hoành mở thực quản, loét tá tràng, rối loạn sau phẫu thuật dạ dày và dị ứng. Cơ địa dị ứng cũng có vấn đề. Kiểm tra hình thái bệnh nhân viêm thực quản thấy phù nề, sung huyết niêm mạc, thâm nhiễm lớp dưới niêm mạc của đoạn cơ hoành của thực quản. Có hai lựa chọn cho sự lây lan của viêm mãn tính - viêm thực quản trào ngược toàn bộ và cục bộ. Với sự tham gia vào quá trình của hơn 2/3 niêm mạc thực quản, sự phát triển của viêm khí quản trào ngược, viêm phế quản trào ngược là hoàn toàn có thể. Ở đầu các nếp gấp thực quản xảy ra hiện tượng ăn mòn, loét nhỏ (ở những vị trí được tưới tối đa với các chất chứa trong dạ dày). Thực quản bị viêm mãn tính dẫn đến co cứng và rút ngắn cơ quan. Ảnh lâm sàng. Các dấu hiệu điển hình của viêm thực quản trào ngược bao gồm cảm giác nóng rát sau xương ức, ợ nóng, trào ngược, trầm trọng hơn khi nằm, khó nuốt và tác dụng tích cực của việc dùng thuốc kháng axit. Đau ngực có thể xảy ra sau khi ăn, gợi nhớ đến cơn đau thắt ngực. Sự xuất hiện của cơn đau trong viêm thực quản trào ngược có liên quan đến kích thích dạ dày của thành thực quản và sự co thắt của nó trong quá trình trào ngược thành phần axit trong dạ dày, cũng như sự xâm phạm của niêm mạc bị sa. Đặc điểm nổi bật của cơn đau này: đặc điểm kéo dài, bỏng rát, khu trú trong quá trình xiphoid, chiếu xạ dọc thực quản, ít thường xuyên hơn ở nửa bên trái của ngực, không có tác dụng đáng chú ý khi dùng thuốc kháng axit, thuốc chống co thắt, tăng ở vị trí nằm ngang, đặc biệt là sau Ăn. Đặc biệt chú ý trong chẩn đoán lâm sàng là các triệu chứng khó nuốt, chẳng hạn như cảm giác có khối u sau xương ức, cảm giác thức ăn nóng đi qua thực quản. Dấu hiệu của bệnh viêm thực quản dần dần bắt đầu có thể là tiết nước bọt và thói quen uống nước cùng thức ăn. Khám thực thể bệnh nhân bị trào ngược thực quản không cung cấp thông tin có ý nghĩa chẩn đoán. Các biến chứng của viêm thực quản trào ngược bao gồm chảy máu, loét, hẹp, rút ngắn thực quản và ác tính. Viêm thực quản trào ngược mãn tính có thể dẫn đến sự phát triển của thoát vị trục. Chẩn đoán và chẩn đoán phân biệt. Phương pháp nghiên cứu có giá trị nhất đối với bệnh lý này là nội soi, trong đó ghi nhận tình trạng tăng huyết áp, phù nề và dày lên các nếp gấp của màng nhầy. Một lớp phủ màu trắng bao phủ màng nhầy là đáng tin cậy, trong giai đoạn đầu của bệnh có thể mỏng, hầu như không đáng chú ý, nhưng với một quá trình lâu dài - màu trắng hoặc xám bẩn lớn. Ở một số vùng, trên nền mảng bám màu trắng, người ta thường nhìn thấy màng nhầy màu đỏ tươi của thực quản. Trong một số trường hợp, các khuyết tật ăn mòn và loét ở dạng sọc được phát hiện. Những thay đổi ở màng nhầy có thể tương ứng với bất kỳ giai đoạn nào trong bốn giai đoạn của viêm thực quản: từ sung huyết đến màng nhầy “khóc”. Khi bị viêm thực quản nặng, nhiều nước bọt và chất nhầy tích tụ trong lòng thực quản. Đo pH, không giống như nội soi, giúp đánh giá độ thanh thải thực quản một cách khách quan hơn. Chụp X-quang cho thấy trào ngược dạ dày thực quản. Cần phân biệt viêm thực quản trào ngược với viêm loét dạ dày tá tràng, bệnh mạch vành, viêm túi mật mãn tính và viêm tụy. Triệu chứng hàng đầu trong chẩn đoán phân biệt là đau. Sự phân biệt với loét dạ dày tá tràng được giúp đỡ bởi sự vắng mặt của các cơn đau muộn và "đói" trong viêm thực quản, cũng như dữ liệu thu được từ nội soi thực quản và dạ dày. Đau mạch vành, trái ngược với viêm thực quản, được đặc trưng bởi mối liên hệ với căng thẳng về thể chất và cảm xúc, ảnh hưởng của nitrat, các dấu hiệu của thiếu máu cục bộ trên điện tâm đồ, bao gồm cả những dấu hiệu theo phép đo xe đạp. Dữ liệu siêu âm của các cơ quan trong ổ bụng giúp loại trừ bệnh lý của túi mật và tuyến tụy là nguyên nhân của hội chứng đau. Điều trị. Điều trị viêm thực quản trào ngược bao gồm điều trị các bệnh gây ra nó và kê đơn thuốc chống trào ngược. Bệnh nhân được khuyến cáo tránh nâng tạ, cúi gập người. Cần nằm đúng tư thế khi nghỉ ngơi và ngủ (đầu giường kê cao 15-20 cm, nghiêng một góc 30-50 °). Nên bình thường hóa trọng lượng cơ thể, ăn chia nhỏ (bữa ăn cuối cùng - 3 giờ trước khi đi ngủ). Rượu và thức ăn cay được loại trừ khỏi chế độ ăn uống. Chỉ định chất hấp phụ và thuốc kiềm hóa có tác dụng bảo vệ màng nhầy. Các chất này bao gồm Venter, được dùng đường uống với liều 1 g (tốt nhất là dưới dạng hỗn dịch) 30 - 40 phút trước bữa ăn 3 lần mỗi ngày và lần thứ 4 khi bụng đói trước khi đi ngủ. Quá trình điều trị là 8-10 tuần. Almagel, phosphalugel, maalox, gastal cũng có tác dụng tương tự. Những loại thuốc này được sử dụng trong giai đoạn xung huyết (1 / 2-2 giờ sau bữa ăn và vào ban đêm) cho đến khi bệnh thuyên giảm hoàn toàn. Phosphalugel và Maalox được kê đơn 1-2 gói 2-3 lần một ngày, gastal - 2-3 viên một ngày. Soda trà, hỗn hợp Bourget, đất sét trắng do không đủ hiệu quả thì không nên sử dụng. Đương quy và tác dụng làm se có bismuth nitrat 1 g 3-4 lần một ngày. Một hoạt tính chống trào ngược cao của một loại thuốc kháng axit mới, topalkan, đã được ghi nhận. Nước khoáng - "Borjomi", "Essentuki No. 4", "Jermuk", "Smirnovskaya" có tác dụng kiềm dầu. Để giảm tiết dịch vị có tính axit, thuốc chẹn H được kê đơn.2thụ thể histamine (cimetidine, ranitidine, famotidine), chất ức chế Ka-K-ATPase (omeprazole), một chất chẹn chọn lọc các thụ thể M-cholinergic của tế bào thành, buscopan tương tự của nó. Cimetidine được kê đơn 400 mg 2 lần một ngày, ranitidine - 300 mg và famotidine - 40 mg một lần vào buổi tối sau bữa ăn tối. Omeprazole được khuyên dùng cho các dạng viêm thực quản do trào ngược ăn mòn và loét. Nó được kê đơn ở mức 30-40 mg mỗi ngày trong 3-4 tuần. Để bình thường hóa rối loạn di tản vận động trong bệnh trào ngược, metoclopramide (cerucal, raglan, perinorm, biomral), prepulsid (sizepride, motilium, domperidone, phối hợp) được kê đơn. Metoclopramide và các chất tương tự thế hệ thứ 2 của nó làm tăng trương lực của cơ vòng thực quản dưới, giảm áp lực trong dạ dày và đẩy nhanh quá trình di tản khỏi dạ dày. Chỉ định metoclopramide 1 viên 3-4 lần một ngày trước bữa ăn hoặc 2 ml tiêm bắp 2 lần một ngày. Thuốc thường được dung nạp tốt. Khi sử dụng nó có thể bị khô miệng, buồn ngủ, ù tai, giảm sau khi ăn. Sizepride là một chất hỗ trợ dạ dày ruột mới. Nó làm tăng trương lực của cơ vòng thực quản dưới, cải thiện độ thanh thải của thực quản, tăng cường chức năng vận động của đường tiêu hóa và ức chế trào ngược bệnh lý (dạ dày và tá tràng). Thuốc, không giống như metoclopramide, không chặn các thụ thể donamine, không phải là chất kích thích trực tiếp các thụ thể kháng cholinergic và không có tác dụng phụ vốn có trong cerucal và các chất tương tự của nó. Nó được kê đơn bằng đường uống với liều lượng 5 hoặc 10 mg 2-3 lần một ngày. Quá trình điều trị kéo dài từ 2-3 tuần đến 2-3 tháng. Cesapride với bệnh viêm thực quản trào ngược có thể được sử dụng như một liệu pháp đơn trị. Dự báo và phòng ngừa. Tiên lượng cho cuộc sống và công việc là thuận lợi. Trong những trường hợp phức tạp, tiên lượng được xác định bởi tính kịp thời và chất lượng chăm sóc y tế. Bệnh nhân mắc bệnh nặng được xếp vào nhóm khuyết tật. Bệnh nhân bị viêm thực quản trào ngược mãn tính nên được theo dõi bởi bác sĩ tiêu hóa. Nghiên cứu nội soi và hình thái được chỉ định ít nhất 2 lần một năm do khả năng ác tính. 3. Loét dạ dày thực quản Viêm loét dạ dày thực quản là một bệnh cấp tính hoặc mãn tính đặc trưng bởi tình trạng loét niêm mạc của thực quản đoạn xa dưới tác động của dịch vị hoạt động. Nguyên nhân và sinh bệnh học. Loét dạ dày thực quản mãn tính là biến chứng của viêm thực quản trào ngược và thoát vị gián đoạn. Sự xuất hiện của chúng được tạo điều kiện thuận lợi bởi thực quản ngắn bên trong, dị sản khu trú của niêm mạc, dị tật của niêm mạc dạ dày vào thực quản, bệnh trào ngược do suy tim, các bệnh kèm theo nôn mửa thường xuyên (hội chứng sau cắt dây thần kinh phế vị, hội chứng vòng hướng tâm, nghiện rượu mãn tính). Loét thực quản cấp tính có thể xảy ra với bệnh lý khô niêm mạc thực quản (xerosis), dị ứng thuốc, sử dụng NSAID, nhiễm nấm, nhiễm virus, bỏng da và các bệnh về hệ thần kinh trung ương. Những vết loét này được coi là có triệu chứng. Ảnh lâm sàng. Một số bệnh nhân có tổn thương loét kết hợp niêm mạc thực quản và vùng dạ dày tá tràng. Các triệu chứng của loét dạ dày thực quản giống với hình ảnh lâm sàng của viêm thực quản dạ dày: ợ chua dai dẳng, nặng hơn sau khi ăn, khi cúi người, ở tư thế nằm, nôn trớ, đau khi nuốt và suy giảm khả năng di chuyển thức ăn đặc. Các biến chứng điển hình của loét thực quản: thủng, chảy máu, xuyên thấu, chít hẹp. Chảy máu được biểu hiện bằng nôn ra máu, đại tiện phân đen, thiếu máu nhược sắc và giảm hoạt động của tim. Thủng thực quản được chẩn đoán cực kỳ hiếm. Các triệu chứng lâm sàng của thủng không thể phân biệt được với các triệu chứng của tổn thương cơ học xuyên thấu cấp tính và không xuyên thấu do dị vật. Khoảng 14% trường hợp loét thực quản xâm nhập vào các mô xung quanh. Chẩn đoán và chẩn đoán phân biệt. Rất khó để nghi ngờ loét dạ dày dựa trên các triệu chứng lâm sàng. Chẩn đoán được xác nhận trong quá trình nghiên cứu dụng cụ và phòng thí nghiệm. Thông tin hữu ích nhất là chụp X-quang và kiểm tra nội soi. Về mặt X quang, vết loét xuất hiện dưới dạng một hốc trong thực quản trên tim với phù nề nhẹ quanh màng nhầy. Thực quản ở khu vực vết loét bị co cứng và phát hiện thấy có sự giãn nở nhẹ trên mức hẹp. Vết loét đi kèm với dấu hiệu tăng động và viêm thực quản trào ngược, triệu chứng thoát vị gián đoạn rất phổ biến. Đôi khi vết loét giống như một túi thừa thượng vị nhỏ, nhưng sau này không có diễn biến lâm sàng điển hình và không kết hợp với suy tim, thoát vị hoặc viêm thực quản. Khó khăn hơn để phân biệt loét dạ dày tá tràng thực quản với ung thư nội mạc loét, đi kèm với sự cứng của thành và sự căng của màng nhầy, và trục không đối xứng, bằng các dấu hiệu X quang. Thông tin đáng tin cậy nhất trong việc xác minh loét dạ dày tá tràng của thực quản được cung cấp bằng nội soi và sinh thiết nhiều lần từ các cạnh của vết loét. Khi đưa ống nội soi tới chỗ loét dạ dày tá tràng, các dấu hiệu của viêm thực quản giai đoạn I-IV, rối loạn chức năng vận động của thực quản, phù nề quanh ổ và xung huyết niêm mạc được tiết lộ. Vết loét cấp tính thường có hình tròn hoặc bầu dục, mép dốc, phủ một lớp sơn màu trắng hoặc xanh lá cây. Vết loét mạn tính có đáy bằng phẳng với các thành dày đặc và không đều, các cạnh nhẹ, lắng đọng có mủ, các ổ dạng hạt và các lớp phủ da. Để loại trừ bệnh ác tính, 4-6 sinh thiết được lấy từ các cạnh của vết loét. Qua nội soi phát hiện dị tật dạ dày đơn lẻ, kéo dài theo trục của thực quản. Chiều dài của chúng thay đổi trong vòng 1-10 cm, nhưng thường không vượt quá 1 cm. Vết loét thường nông, đáy của nó được bao phủ bởi một lớp sơn màu trắng. Xung huyết, phù nề niêm mạc và ăn mòn đơn lẻ thường phản ánh một phản ứng viêm quanh nhu động vừa phải. Sau khi chữa lành vết loét dạ dày tá tràng, một vết sẹo hình sao hoặc tuyến tính thô ráp hoặc một biến dạng thô ráp giống như lưới diverticulum của thành và hẹp lòng mạch vẫn còn trong thực quản. Cần phân biệt loét dạ dày tá tràng thực quản với loét có tính chất đặc hiệu (với lao, giang mai). Trong những tình huống này, các xét nghiệm huyết thanh học cụ thể, kết quả của các nghiên cứu mô học và vi khuẩn học giúp ích đáng kể. Sự kết hợp giữa bệnh lý của thực quản với tổn thương phổi và các cơ quan khác làm cho bệnh nhân cần phải kiểm tra có mục đích liên quan đến một quá trình cụ thể. Điều trị. Điều trị bao gồm một chế độ ăn kiêng: nên dùng thực phẩm nhẹ nhàng về mặt cơ học và hóa học, chia thành nhiều phần nhỏ 5-6 lần một ngày. Để tránh trào ngược các chất từ dạ dày lên thực quản, tư thế nằm của bệnh nhân phải kê cao đầu giường. Thuốc được uống nằm. Đơn trị liệu được kê toa với một loại thuốc thuộc một trong các nhóm dược lý sau: thuốc chống tiết, bao gồm thuốc kháng axit và chất hấp phụ, thuốc kích thích chức năng vận động của dạ dày (prokinetic), thuốc - chất mô phỏng chất nhầy. Trị liệu được thực hiện trong một thời gian dài - 1,5-3 tháng. Chỉ định điều trị phẫu thuật - thiếu lành trong vòng 6-9 tháng, diễn biến phức tạp (thủng, thâm, hẹp, chảy máu). Dự báo và phòng ngừa. Diễn biến của bệnh đang tái phát. Tiên lượng cho cuộc sống và công việc là thuận lợi. Nên khám định kỳ (1-2 lần một năm) trên cơ sở ngoại trú bởi bác sĩ chuyên khoa tiêu hóa bằng phương pháp nội soi và sinh thiết. Thực hiện theo mùa (xuân - thu) phòng bệnh trào ngược thực quản. BÀI GIẢNG SỐ 10. Các bệnh về đường tiêu hóa. Các bệnh về dạ dày. Viêm dạ dày mãn tính Viêm dạ dày mãn tính là một bệnh đặc trưng về mặt lâm sàng là rối loạn tiêu hóa dạ dày và về mặt hình thái - bởi những thay đổi về viêm và thoái hóa ở niêm mạc dạ dày, suy giảm quá trình đổi mới tế bào và sự gia tăng số lượng tế bào huyết tương và tế bào lympho trong màng nhầy. Nguyên nhân và sinh bệnh học. Ở giai đoạn phát triển hiện nay của khoa tiêu hóa, người ta đã xác định rằng sự xuất hiện của viêm dạ dày mãn tính được tạo điều kiện thuận lợi bởi sự phát triển của vi khuẩn Helicobacter pylori (HP), gây ra viêm dạ dày hang vị ở 95% trường hợp và viêm dạ dày ở 56% trường hợp. Ngược lại, những yếu tố được gọi là căn nguyên của sự xuất hiện của viêm dạ dày mãn tính có thể được cho là có mức độ chắc chắn cao với các yếu tố nguy cơ (chế độ ăn uống không cân bằng không thường xuyên, hút thuốc, uống rượu, tăng tiết axit clohydric và pepsin). Vai trò hàng đầu trong sự phát triển của bệnh cũng thuộc về cơ chế tự miễn dịch, kèm theo sự tích tụ của các kháng thể đối với tế bào thành của niêm mạc dạ dày, làm trầm trọng thêm tính di truyền, cũng như sử dụng các loại thuốc có tác dụng làm tổn thương niêm mạc dạ dày. Phân loại. Năm 1990, tại Hội nghị bác sĩ tiêu hóa quốc tế lần thứ IX ở Úc, một hệ thống hóa mới về viêm dạ dày mãn tính, được gọi là hệ thống Sydney, đã được thông qua. Cơ sở mô học của phân loại. 1) Căn nguyên: viêm dạ dày mãn tính liên quan đến HP, tự miễn, vô căn, viêm dạ dày cấp tính do thuốc. 2) Địa hình: antral, fundic, pangastitis. 3) Hình thái: cấp tính, mãn tính, các thể đặc biệt. Nội soi cơ sở phân loại: 1) viêm dạ dày của dạ dày; 2) viêm dạ dày của cơ thể của dạ dày; 3) viêm ức; 4) thay đổi niêm mạc dạ dày: phù nề, ban đỏ, tổn thương niêm mạc, dịch tiết, bào mòn phẳng, ăn mòn cao, tăng sản nếp gấp, teo nếp gấp, nhìn thấy hình mạch máu, xuất huyết trên niêm mạc. Ảnh lâm sàng. Viêm dạ dày mãn tính là một trong những bệnh thường gặp tại phòng khám nội khoa. Tỷ lệ mắc bệnh của cư dân trên thế giới dao động từ 28 đến 75%. Viêm dạ dày mãn tính thường biểu hiện bằng các triệu chứng đầy hơi khó tiêu và đau tức vùng thượng vị. Hiếm khi, nó không có triệu chứng. Cơn đau thường khu trú ở vùng thượng vị. Có một mối liên hệ rõ ràng giữa sự xuất hiện của nó với lượng thức ăn và sự định vị của quá trình viêm trong dạ dày. Ở những bệnh nhân bị viêm dạ dày phần dưới tim và tim của dạ dày, cơn đau ở vùng thượng vị xảy ra 10-15 phút sau bữa ăn, với bệnh lý của dạ dày - 40-50 phút sau bữa ăn. Những cơn đau "muộn", "đói" là điển hình cho bệnh viêm dạ dày của phần đầu ra của dạ dày, hoặc viêm tá tràng. Đau "hai làn sóng" - sau khi ăn và lúc bụng đói - được quan sát thấy cùng với viêm dạ dày dưới tim và antrum. Với quá trình lan tỏa, cơn đau khu trú ở vùng thượng vị, xuất hiện sau khi ăn và có tính chất bức bách. Họ nói về quá trình không có triệu chứng của viêm dạ dày khi không thể thiết lập mối quan hệ giữa cơn đau ở vùng thượng vị và tổn thương, xảy ra khi nó có nguồn gốc nội sinh (viêm dạ dày trở thành thứ phát sau bệnh lý của các cơ quan và hệ thống khác). Một vị trí quan trọng không kém trong bệnh cảnh lâm sàng của viêm dạ dày mãn tính là hội chứng khó tiêu: buồn nôn, ợ hơi (chua, đắng, thối), ợ chua, táo bón hoặc tiêu chảy, phân không ổn định. Với bệnh viêm dạ dày do antral riêng lẻ, những phàn nàn về chứng ợ nóng và táo bón, phát sinh do sự tăng tiết axit clohydric và pepsin, trở thành điều tối quan trọng. Với bệnh viêm tuyến thượng vị với các dấu hiệu teo nặng, buồn nôn, ợ hơi "thối", phân không ổn định hoặc tiêu chảy là chủ yếu, đó là biểu hiện điển hình của giảm bài tiết axit clohydric và pepsin. Buồn nôn dai dẳng là đặc điểm của viêm dạ dày thứ phát trong viêm tụy mãn tính, viêm túi mật mãn tính, xảy ra với rối loạn vận động giảm vận động của túi mật. Chẩn đoán. Viêm dạ dày mãn tính kéo dài và các triệu chứng tăng dần theo thời gian. Các đợt trầm trọng được kích thích bởi rối loạn dinh dưỡng. Hình ảnh thực thể của bệnh viêm dạ dày mãn tính khá nghèo nàn. Ở 80-90% bệnh nhân trong đợt cấp của bệnh, một nghiên cứu khách quan xác định chỉ đau cục bộ vùng thượng vị. Khi viêm dạ dày mãn tính kết hợp với viêm tá tràng, viêm túi mật hoặc viêm tụy, có thể xác định được vị trí đau không điển hình cho viêm dạ dày, nhưng đặc trưng cho bệnh lý của cơ quan khác. Xét nghiệm máu và nước tiểu tổng quát, các thông số sinh hóa của máu ở bệnh nhân viêm dạ dày mãn tính không khác với các thông số tương ứng ở người khỏe mạnh. Trong một nghiên cứu khoa học, không có thay đổi nào trong các phân tích, hoặc có thể có dấu hiệu của rối loạn tiêu hóa. Khi nghiên cứu các thành phần trong dạ dày tiết axit bằng phương pháp đo pH, cả hai dấu hiệu của quá trình tăng tiết axit và hiện tượng giảm sản xuất axit đều được ghi nhận. Các chỉ số hình thành pepsin trong viêm dạ dày mãn tính dai dẳng hơn và giảm so với nền của tình trạng nhiễm độc dai dẳng trong tổn thương cơ quan lan tỏa. Kiểm tra X quang có nhiều khả năng loại trừ các bệnh khác của dạ dày (loét, ung thư), giúp chẩn đoán bệnh Menetrier hơn là xác định chẩn đoán viêm dạ dày mãn tính. Do sự ít biểu hiện lâm sàng của bệnh, cũng như tính không đặc hiệu của các xét nghiệm cận lâm sàng, việc chẩn đoán viêm dạ dày mãn tính dựa trên kết quả nội soi và nghiên cứu hình thái học. Nội soi cho thấy những thay đổi về mức độ nghiêm trọng của niêm mạc dạ dày với các mức độ nghiêm trọng khác nhau: phù nề, ban đỏ, tổn thương của niêm mạc, dịch tiết, xói mòn phẳng, ăn mòn nổi lên, tăng sản hoặc teo các nếp gấp, nhìn thấy mô hình mạch máu, xuất huyết dưới niêm mạc. Họ nói về bệnh viêm dạ dày mãn tính với sự gia tăng số lượng tế bào huyết tương và tế bào lympho trong màng nhầy của chính nó (ngược lại với viêm dạ dày cấp tính, khi bạch cầu đa nhân xuất hiện). Liên quan đến những điều đã nói ở trên, việc xác định hình thái của tình trạng viêm trong viêm dạ dày có thể không trùng khớp với cách giải thích dữ liệu của bác sĩ lâm sàng. Hoạt động của các biến đổi viêm trong niêm mạc dạ dày được đánh giá về hình thái và hình thái tùy theo mức độ thâm nhiễm bạch cầu của lớp đệm hoặc biểu mô. Chúng ta không được quên thực tế rằng bệnh viêm dạ dày tự miễn không hoạt động. Các thay đổi về hình thái (yếu, trung bình và nặng) - viêm, hoạt động, teo, chuyển sản - và mức độ nhiễm HP được định lượng. Biểu hiện lâm sàng đặc trưng của viêm dạ dày cũng được quan sát thấy trong các bệnh khác của hệ tiêu hóa, do đó, trong quá trình chẩn đoán, siêu âm ổ bụng, nội soi kỹ lưỡng và kiểm tra hình thái của cơ quan tiêu hóa là cần thiết. Chẩn đoán phân biệt. Khó khăn nhất là chẩn đoán phân biệt viêm dạ dày với các bệnh chức năng của dạ dày, loét dạ dày tá tràng, viêm túi mật mãn tính và viêm tụy và ung thư dạ dày. Các bệnh cơ năng của dạ dày, tương tự như viêm dạ dày mãn tính, có thể xảy ra âm ỉ hoặc kèm theo các triệu chứng đau, khó tiêu. Chúng được đặc trưng bởi một thời gian ngắn, sự hiện diện của các triệu chứng rối loạn thần kinh chung phổ biến trong bệnh cảnh lâm sàng của bệnh (như suy nhược, mệt mỏi, khó chịu, đau đầu, tâm trạng không ổn định, đổ mồ hôi). Với rối loạn chức năng của dạ dày, cơn đau không phụ thuộc vào chất lượng của thực phẩm, hoặc nó xảy ra sau khi sử dụng một sản phẩm được xác định nghiêm ngặt. Thường có hội chứng tiết acid (ợ chua, chua chua, chua trong miệng), không giống như viêm dạ dày chức năng bài tiết không tăng sau khi ăn, nhưng hưng phấn, lâu không ăn. Nôn trong các bệnh lý chức năng của dạ dày phát triển theo cơ chế của một phản xạ có điều kiện, mang lại cảm giác nhẹ nhõm cho người bệnh và không dẫn đến tình trạng chung xấu đi đáng kể. Trong bệnh viêm dạ dày mãn tính, nó thường xảy ra trong đợt cấp và không mang lại sự thuyên giảm cho người bệnh. Một triệu chứng thường xuyên của sự rối loạn chức năng của dạ dày là một lượng hơi lớn. Trong bệnh viêm dạ dày mãn tính, nó liên quan đến việc tiêu hóa thức ăn hoặc nhu động dạ dày bị suy giảm và có thể có tính axit nếu dịch tiết được giữ nguyên, hoặc có mùi trứng thối nếu giảm. Trong nghiên cứu về bài tiết dịch vị trong bệnh viêm dạ dày, các giá trị bình thường của bài tiết được phát hiện ở giai đoạn đầu của bệnh, và trong tương lai, xu hướng giảm bài tiết dịch vị. Với các bệnh chức năng của dạ dày, dị vật thường được quan sát thấy. Chụp X-quang dạ dày có thể xác nhận các dạng viêm dạ dày như cứng, mạch, tăng sản khổng lồ, đa polyp và trong trường hợp vi phạm chức năng vận động của dạ dày (viêm dạ dày, hạ huyết áp) cho thấy bản chất chức năng của bệnh tật. Phương pháp nghiên cứu có giá trị nhất để chẩn đoán phân biệt giữa viêm dạ dày mãn tính và các bệnh chức năng của dạ dày là nội soi dạ dày, trong những trường hợp còn tranh cãi, cho phép xác định chắc chắn những thay đổi của niêm mạc dạ dày đặc trưng của viêm dạ dày hoặc các bệnh chức năng của dạ dày. Chẩn đoán phân biệt của viêm dạ dày mãn tính với loét dạ dày tá tràng được mô tả trong bài giảng tiếp theo. Ung thư dạ dày có hình ảnh rất giống với bệnh viêm dạ dày với chức năng bài tiết giảm. Việc chẩn đoán sớm ung thư dạ dày trên cơ sở các dấu hiệu lâm sàng là rất khó, đặc biệt là ở những bệnh nhân bị viêm dạ dày lâu năm. Điều quan trọng đối với việc chẩn đoán ung thư là sự xuất hiện của các cơn đau dai dẳng dai dẳng, ít phụ thuộc vào lượng thức ăn, suy nhược chung và mệt mỏi, chán ăn, cũng như trọng lượng cơ thể của bệnh nhân giảm dần. Phát hiện khối u khi sờ nắn đề cập đến các giai đoạn sau của quá trình ung thư. Các triệu chứng như thay đổi sức khỏe của bệnh nhân, giảm nhanh độ axit của dịch vị, “thiếu hụt” axit clohydric, xuất hiện các tế bào không điển hình trong dịch dạ dày, phản ứng dương tính với máu ẩn trong phân nên khiến bác sĩ nghi ngờ ung thư dạ dày. Có tầm quan trọng quyết định trong chẩn đoán phân biệt là các nghiên cứu chụp X-quang và nội soi dạ dày với sinh thiết nhắm mục tiêu niêm mạc dạ dày. Ở những bệnh nhân bị viêm dạ dày mãn tính với chức năng bài tiết giảm, kiểm tra bằng tia X cho thấy màng nhầy của nó bị teo, điều này cũng được khẳng định bằng nội soi dạ dày. Với sinh thiết mục tiêu trong những trường hợp như vậy, những thay đổi cấu trúc và teo màng nhầy được tiết lộ. Đối với ung thư dạ dày, kiểm tra bằng tia X được đặc trưng bởi sự hiện diện của một khuyết tật lấp đầy, không có nếp gấp niêm mạc hoặc thay đổi bản chất của chúng và không có nhu động ở một số khu vực nhất định. Nội soi dạ dày giúp phát hiện khối u ở giai đoạn phát triển sớm nhất, khi khối u vẫn còn trong niêm mạc dạ dày, và điều trị phẫu thuật giúp phục hồi hơn 90% trường hợp. Viêm túi mật mãn tính. Trong viêm túi mật mãn tính, cơn đau khu trú ở hạ sườn phải và có tính chất âm ỉ. Với viêm túi mật sỏi, cơn đau cấp tính, đau bụng, lan xuống vùng dưới xương vai bên phải. Cơn đau khởi phát có liên quan đến việc ăn thức ăn béo hoặc lái xe xóc nảy. Trong viêm dạ dày mãn tính, cơn đau vùng thượng vị có tính chất lan tỏa, âm ỉ, không có tia xạ, xuất hiện ngay sau khi ăn thức ăn khô hoặc vi phạm chế độ ăn. Với bệnh viêm dạ dày và viêm túi mật, cơn đau đi kèm với các triệu chứng khó tiêu, nhưng cảm giác nặng vùng thượng vị, đầy bụng, ợ hơi thức ăn hoặc không khí, có vị kim loại trong miệng là đặc điểm của bệnh viêm dạ dày. Nôn mửa trong viêm dạ dày mãn tính là rất hiếm. Về mặt khách quan, trong viêm túi mật mãn tính, đặc biệt là thể tích, họ phát hiện thấy căng ở thành bụng trước, cảm giác da vùng hạ vị bên phải, đây không phải là điển hình của viêm dạ dày mãn tính. Khi sờ bụng trong trường hợp viêm túi mật mãn tính, đau được ghi nhận ở khu vực của túi mật. Viêm dạ dày mãn tính có đặc điểm là đau nhức lan tỏa. Ở những bệnh nhân bị viêm túi mật mãn tính, kiểm tra mật cho thấy sự gia tăng số lượng chất nhầy và bạch cầu. Viêm dạ dày mãn tính được đặc trưng bởi một hình ảnh bình thường của mật dựa trên nền tảng của những thay đổi trong bài tiết và độ axit của dịch vị, cũng như các chức năng khác của dạ dày (hấp thụ, vận động). Chụp X-quang túi mật ở những bệnh nhân bị viêm túi mật mãn tính cho thấy sự thay đổi chức năng di tản của nó, cũng như sỏi. Viêm tụy mãn tính. Trong viêm tụy mãn tính, cơn đau khu trú ở nửa bên trái của bụng, lan xuống vùng dưới xương bả vai trái, đến lưng dưới và vùng xung quanh. Sự xuất hiện của cơn đau có liên quan đến việc tiêu thụ nhiều thực phẩm béo, thường là chất béo và rượu. Nếu viêm dạ dày mãn tính được đặc trưng bởi một đợt bệnh kéo dài, đơn điệu, thì trong viêm tụy mãn tính, nó là từng bước. Một cuộc kiểm tra khách quan trong trường hợp viêm tụy mãn tính cho thấy giảm kích thích da ở vùng hạ vị trái, đau về mặt địa hình tương ứng với vị trí của tuyến tụy. Trong một nghiên cứu trong phòng thí nghiệm về dịch tụy trong bệnh viêm tụy mãn tính, người ta thấy có sự thay đổi dai dẳng về độ kiềm và enzym: mức độ diastase trong máu và nước tiểu có thể thay đổi, điều này không xảy ra với bệnh viêm dạ dày mãn tính. Về mặt X quang, viêm tụy mãn tính được đặc trưng bởi sự đảo ngược của vòng tá tràng tăng lên, sự gia tăng mạnh của các nhú chính của nó (triệu chứng Frostberg), và đôi khi sự hiện diện của các khu vực vôi hóa của tuyến tụy. Chẩn đoán nội khoa của các dạng viêm dạ dày mãn tính khác nhau cũng nên được thực hiện. Do đó, bệnh liên quan đến vi khuẩn HP tiến triển về mặt lâm sàng với các triệu chứng loét tá tràng, và trong một số trường hợp, bệnh có thể tiến triển âm ỉ. Nội soi và kiểm tra hình thái học cho thấy viêm phổi antropylorhoduodenitis. Ăn mòn trong viêm dạ dày do Helicobacter pylori thường khu trú ở vùng viêm nặng (vùng nhân trắc của dạ dày). Viêm dạ dày mãn tính tự miễn được đặc trưng lâm sàng bởi cảm giác nặng vùng thượng vị, dư vị khó chịu trong miệng, ợ hơi thối và buồn nôn. Do không sản xuất đủ axit clohydric, tiêu chảy xuất hiện. Trong 10% trường hợp, dựa trên nền tảng của bệnh viêm dạ dày tự miễn dịch, các triệu chứng được tìm thấy B12- thiếu máu do thiếu máu: suy nhược, xanh xao của da và niêm mạc, móng tay giòn, trong các xét nghiệm máu - thiếu máu hồng cầu khổng lồ tăng sắc tố. Các dạng đặc biệt của bệnh bao gồm u hạt, tăng bạch cầu ái toan, phì đại (bệnh Menetrier), viêm dạ dày lympho bào. Viêm dạ dày u hạt hoạt động như một dạng bệnh độc lập hoặc thường xuyên hơn - một trong những thành phần của bệnh lý nghiêm trọng hơn (bệnh Crohn, bệnh lao, bệnh sarcoidosis). Chẩn đoán luôn được khẳng định bằng kết quả xét nghiệm mô học của bệnh phẩm sinh thiết niêm mạc dạ dày. Viêm dạ dày tăng bạch cầu ái toan là cực kỳ hiếm và là do viêm mạch hệ thống. Tiền sử phản ứng dị ứng là bắt buộc. Kiểm tra mô học cho thấy thâm nhiễm bạch cầu ái toan của niêm mạc dạ dày. Viêm dạ dày phì đại (bệnh Menetrier) biểu hiện trên lâm sàng là đau vùng thượng vị và buồn nôn. Một số bệnh nhân có thể bị sụt cân do tiêu chảy. Trong các nghiên cứu nội soi, X quang và hình thái học, người ta tìm thấy các nếp gấp niêm mạc phì đại khổng lồ, giống như các nếp gấp của não. Viêm dạ dày lympho bào không có triệu chứng về mặt lâm sàng; về hình thái, dạng này được đặc trưng bởi sự xâm nhập rõ rệt vào niêm mạc dạ dày bởi các tế bào lympho. Điều trị. Bệnh nhân viêm dạ dày cần các biện pháp y tế tổng quát: dinh dưỡng cân bằng thường xuyên, bình thường hóa lịch trình làm việc và nghỉ ngơi, giải quyết các tình huống căng thẳng trong cuộc sống và công việc hàng ngày. Điều trị bằng thuốc chỉ được chỉ định khi có biểu hiện lâm sàng của viêm dạ dày mãn tính. Bệnh nhân bị viêm dạ dày liên quan đến HP được điều trị bằng chương trình loét dạ dày tá tràng (xem bài giảng tiếp theo). Những người bị viêm dạ dày tự miễn dịch cần bổ sung vitamin B12 (500 mcg mỗi ngày một lần tiêm dưới da trong 1 ngày, sau đó lặp lại các đợt điều trị), axit folic (30 mg mỗi ngày), axit ascorbic (tối đa 5 g mỗi ngày). Nếu cần thiết, điều trị thay thế bằng các chế phẩm enzym (mezim-forte, festal, enzistal, creon, pancitrate, acidin-pepsin) được thực hiện. Hội chứng đau thường được chấm dứt bằng cách chỉ định thuốc kháng axit (maalox, almagel, gastal) hoặc thuốc chẹn thụ thể H-histamine (ranitidine, famotidine) với liều điều trị trung bình. Với các dạng viêm dạ dày đặc biệt, việc điều trị bệnh cơ bản là cần thiết. Dự báo và phòng ngừa. Tiên lượng cho cuộc sống và công việc là thuận lợi. Bệnh nhân bị viêm dạ dày mãn tính nên được đăng ký với bác sĩ tiêu hóa. Họ được kiểm tra lâm sàng và nội soi bằng sinh thiết ít nhất mỗi năm một lần để loại trừ sự biến đổi khối u. Nguy hiểm nhất về mặt thoái hóa ung thư là viêm dạ dày phì đại, teo lan tỏa với chứng loạn sản biểu mô. Trong các dạng ăn mòn của bệnh phức tạp do chảy máu, cũng như ở dạng mất bù của bệnh Menetrier, tiên lượng được xác định bởi sự kịp thời và đầy đủ của điều trị phẫu thuật. Phòng ngừa bệnh viêm dạ dày là chế độ dinh dưỡng hợp lý, tuân thủ chế độ làm việc và nghỉ ngơi, hạn chế dùng NSAID. BÀI GIẢNG SỐ 11. Các bệnh về đường tiêu hóa. Các bệnh về dạ dày. loét dạ dày tá tràng Loét dạ dày tá tràng (loét dạ dày tá tràng) là một bệnh mãn tính, hay tái phát, biểu hiện lâm sàng bằng một bệnh lý chức năng của vùng dạ dày tá tràng và về mặt hình thái - do sự vi phạm tính toàn vẹn của các lớp niêm mạc và dưới niêm mạc, và do đó vết loét luôn lành với sự hình thành vết sẹo. Nguyên nhân. Yếu tố căn nguyên chính của bệnh loét dạ dày tá tràng là sự phát triển của vi khuẩn HP trên bề mặt biểu mô dạ dày. Tầm quan trọng của sự xâm nhập của vi khuẩn trong căn nguyên của bệnh đã được nghiên cứu từ năm 1983, khi J. Warren và B. Marshall báo cáo việc phát hiện ra một số lượng lớn vi khuẩn xoắn ốc S trên bề mặt biểu mô của dạ dày. Vi khuẩn Helicobacteria có khả năng tồn tại trong môi trường axit do sản xuất enzym urease, enzym này chuyển ure (từ máu) thành amoniac và carbon dioxide. Sản phẩm của quá trình thủy phân bằng enzym sẽ trung hòa axit clohydric và tạo điều kiện thay đổi pH của môi trường xung quanh từng tế bào vi khuẩn, tạo điều kiện thuận lợi cho hoạt động sống của vi sinh vật. Sự xâm chiếm toàn bộ HP xảy ra trên bề mặt tế bào biểu mô dạ dày, kèm theo tổn thương biểu mô dưới tác dụng của phospholipase. Sau đó cung cấp sự hình thành các lecithin và proteinase độc hại từ mật, gây ra sự phá hủy các phức hợp protein bảo vệ và chất nhầy. Trong bối cảnh "kiềm hóa" màng tế bào biểu mô bằng amoniac, điện thế màng của tế bào thay đổi, sự khuếch tán ngược của các ion hydro tăng lên, làm chết và bong vảy của biểu mô niêm mạc dạ dày. Tất cả những thay đổi này dẫn đến sự xâm nhập của HP vào sâu trong niêm mạc dạ dày. Không kém phần quan trọng trong sự phát triển của viêm loét dạ dày tá tràng là tác động thần kinh, khuynh hướng di truyền, tác nhân lây nhiễm, sai sót trong thuốc men và việc uống một số loại thuốc, và thói quen xấu. Lần đầu tiên, khái niệm sinh thần kinh về sự khởi phát của bệnh được đưa ra bởi Bergman, người đã lập luận rằng các rối loạn cấu trúc di truyền của hệ thần kinh tự chủ dẫn đến co thắt cơ và mạch máu trong thành dạ dày, thiếu máu cục bộ và giảm trong khả năng chống lại các tác động tích cực của dịch vị. Lý thuyết này được phát triển thêm bởi K. N. Bykov và I. T. Kurtsin (1952). Họ đã chứng minh lý thuyết hình thành loét ở vỏ não, dựa trên dữ liệu về những thay đổi trong hoạt động thần kinh cao hơn do chấn thương thần kinh mãn tính. Được bổ sung và chi tiết hóa bởi học thuyết về các liên kết sinh hóa và nội tiết tố trong việc điều hòa bài tiết dịch vị, nhu động và tính chất, lý thuyết về sự tạo loét này một lần nữa lại được nhiều người ủng hộ trong những năm gần đây. Các yếu tố di truyền phổ biến trong các nhà nghiên cứu: tính ì của các quá trình thần kinh chính, tính chất nhóm cụ thể của máu, các đặc điểm miễn dịch và sinh hóa, hội chứng gánh nặng di truyền. Trong trường hợp loét dạ dày tá tràng, rối loạn dinh dưỡng có tầm quan trọng lớn. Tuy nhiên, các nghiên cứu lâm sàng và thực nghiệm được thực hiện trong hai thập kỷ qua trong hầu hết các trường hợp không cho thấy tác hại của thực phẩm đối với niêm mạc dạ dày tá tràng. Tỷ lệ mắc bệnh loét dạ dày tá tràng trong số những người có thói quen ăn uống khác nhau cũng chứng minh tầm quan trọng hàng đầu của các yếu tố dinh dưỡng. Sự xáo trộn trong nhịp điệu và sự đều đặn của chế độ dinh dưỡng, nghỉ dài giữa các bữa ăn, ăn uống không đúng giờ là những yếu tố cần thiết cho sự xuất hiện của viêm loét dạ dày tá tràng. Các nhà nghiên cứu đã bày tỏ quan điểm tương đối trái ngược nhau về vai trò của rượu trong quá trình hình thành vết loét. Rượu được biết là nguyên nhân làm teo niêm mạc dạ dày. Những quan sát này mâu thuẫn với khái niệm chung về sự hình thành vết loét. Tuy nhiên, việc sử dụng rượu bia thường xuyên kèm theo vi phạm chế độ ăn uống, thay đổi chất lượng trong thành phần thức ăn, cuối cùng có thể gây ra viêm loét dạ dày, tá tràng. Vai trò của tác dụng thuốc trong quá trình sinh loét đang được nghiên cứu tích cực. Kết quả của các nghiên cứu được công bố trong tài liệu và dữ liệu riêng của chúng tôi chỉ ra rằng thuốc chống viêm không steroid và hormone glucocorticoid có đặc tính gây loét rõ rệt nhất. Sinh bệnh học. Cơ chế bệnh sinh của bệnh loét dạ dày tá tràng vẫn chưa được hiểu đầy đủ. Khi xem xét các quá trình hình thành vết loét, cần nêu bật một số định đề: 1) đặc trưng bởi tính theo mùa của các đợt cấp của loét dạ dày tá tràng; 2) có một bản địa hóa chủ yếu của loét dạ dày tá tràng ở vùng tiền tá tràng; 3) sự hiện diện của axit clohydric và pepsin trong dịch dạ dày đã được ghi nhận; 4) tần suất cao (lên đến 70%) các vết loét dạ dày và tá tràng tự chữa lành là đáng chú ý; 5) bị viêm dạ dày mạn tính do vi khuẩn HP; 6) nhân vị của dạ dày và phần ban đầu của tá tràng là "vùng dưới đồi" của đường tiêu hóa; 7) có một khuynh hướng di truyền đối với sự xuất hiện của loét dạ dày tá tràng; 8) sự xuất hiện của một vết loét, sự tái phát và thuyên giảm của nó có thể xảy ra với sự hiện diện của tất cả các yếu tố trên. Do đó, khái niệm thống nhất về bệnh loét như sau. Ở một bệnh nhân có khuynh hướng di truyền đối với loét dạ dày tá tràng kèm theo viêm dạ dày mãn tính do vi khuẩn trong giai đoạn mùa thu hoặc mùa xuân, chỉ có sự tăng sản và tăng chức năng của các tế bào nội tiết tiết ra gastrin, histamine, melatonin và serotonin được ghi nhận. Các kích thích tố chính và các amin sinh học được sản xuất bởi vùng anthropyloruduodenal có liên quan đến cả việc kích thích bài tiết dịch vị và thay đổi tính dinh dưỡng và tăng sinh tế bào, chủ yếu ở vùng này. Trong bối cảnh viêm dạ dày và tá tràng do vi khuẩn hoạt động, tạo điều kiện thuận lợi cho sự hình thành vết loét. Với sự hình thành của một khiếm khuyết ở đường tiêu hóa, hoạt động chức năng của các tế bào nội tiết giảm. Điều này dẫn đến giảm sự xâm nhập của axit-dạ dày, cải thiện tính dinh dưỡng của mô trong vùng nhân tá tràng và tạo điều kiện để chữa lành các vết loét dạ dày và tá tràng, thậm chí chống lại sự mở rộng vi sinh vật đang diễn ra của HP. Trong giai đoạn cấp tính của loét dạ dày tá tràng, sự tăng sản của các tế bào sản xuất α-endorphin, là chất bảo vệ tế bào phổ quát, được ghi nhận. Chúng hoạt động như cơ chế bảo vệ chính trong loét dạ dày tá tràng và cung cấp quá trình tự giới hạn vết loét và chữa lành vết loét, cả trực tiếp và bằng cách kích thích hệ thống miễn dịch. Đồng thời, các kháng thể chống lại HP, được tổng hợp trong lớp dưới niêm mạc của dạ dày và tá tràng, liên kết hiệu quả với các tế bào vi khuẩn và vô hiệu hóa độc tố HP và góp phần làm chết chúng. Tất cả những điều trên góp phần tạo nên sự cân bằng giữa cái gọi là yếu tố gây hấn và yếu tố bảo vệ, đồng thời chữa lành khiếm khuyết đường tiêu hóa ở vùng dạ dày tá tràng. Phân loại. Phân loại (Panfilov Yu. A., Osadchuk M. A., 1991) Xác định vị trí của khiếm khuyết đường tiêu hóa: 1) loét dạ dày (phần dưới tim và tim, phần môn vị và ống môn vị, độ cong nhỏ hơn và lớn hơn); 2) loét tá tràng (phần bóng đèn và thanh bài); 3) loét dạ dày và tá tràng. Quá trình loét dạ dày tá tràng. 1. Dễ dàng. Đợt cấp của vết loét không quá 1 lần trong 1-3 năm, quá trình lành vết loét kết thúc vào tuần thứ 5-6 kể từ khi bắt đầu điều trị, mức độ nghiêm trọng của các hội chứng đau và khó tiêu là trung bình. 2. Vừa phải. Tái phát ít nhất 2 lần một năm, biểu mô hóa vết loét - trong vòng 7-12 tuần, mức độ nghiêm trọng của đau và các hội chứng khó tiêu. 3. Nặng. Thời gian miễn nhiệm không quá 3-4 tháng. Ngoài những cơn đau dữ dội, còn có những biến chứng. Các giai đoạn của bệnh: 1) đợt cấp của tái phát loét hoặc rối loạn chức năng của hệ thống dạ dày tá tràng; 2) thuyên giảm hoàn toàn (về mặt lâm sàng, X quang, nội soi và chức năng); 3) không hoàn toàn (với sự bảo tồn của các rối loạn chức năng hoặc cấu trúc trong vùng dạ dày tá tràng). Tình trạng của màng nhầy của dạ dày và tá tràng: 1) viêm dạ dày mãn tính; 2) viêm tá tràng mãn tính. Trạng thái chức năng của hệ thống dạ dày tá tràng Tiết: bình thường, tăng, giảm. Chuyển động: bình thường, tăng tốc, chậm; sơ tán: bình thường, tăng tốc, hòa hoãn, hành tá tràng. Các biến chứng: chảy máu, thủng, thâm nhập, viêm quanh dạ dày, viêm tá tràng, biến dạng thành dạ dày và tá tràng. Ảnh lâm sàng. Hình ảnh lâm sàng của loét dạ dày tá tràng rất đa hình. Các triệu chứng phụ thuộc vào giới tính và độ tuổi của bệnh nhân, thời gian trong năm, vị trí và kích thước của vết loét, đặc điểm cá nhân và xã hội của bệnh nhân cũng như phẩm chất chuyên môn của người đó. Phòng khám được xác định bởi sự kết hợp của các dấu hiệu: diễn biến mãn tính của bệnh kể từ thời điểm khởi phát, sự hiện diện của các dấu hiệu trầm trọng và thuyên giảm của bệnh, chữa lành các khiếm khuyết ở niêm mạc dạ dày và tá tràng với sự hình thành một khối u. vết sẹo. Loét dạ dày tá tràng được biểu hiện bằng hai biến thể lâm sàng và hình thái: loét dạ dày và loét tá tràng. Theo truyền thống, các hội chứng đau và khó tiêu được phân biệt. Dấu hiệu lâm sàng hàng đầu là đau vùng bụng trên. Về bản chất của hội chứng đau, hầu như không thể phân biệt giữa viêm dạ dày mãn tính do vi khuẩn và loét dạ dày tá tràng. Đau vùng thượng vị, lúc bụng đói, chủ yếu vào mùa xuân và mùa thu, thường gặp ở cả viêm loét dạ dày tá tràng và viêm dạ dày mạn tính do vi khuẩn. Giảm hội chứng đau bằng thức ăn và thuốc kháng axit có thể đạt được cả trong viêm dạ dày mãn tính do vi khuẩn và loét dạ dày tá tràng. Phân biệt với viêm loét dạ dày tá tràng chỉ là biểu hiện đau vùng thượng vị về đêm. Nôn do loét dạ dày tá tràng là rất hiếm. Buồn nôn phổ biến hơn nhiều với loét dạ dày và loét tá tràng. Táo bón kèm theo loét tá tràng mãn tính. Các triệu chứng của bệnh loét dạ dày tá tràng được xác định bởi số lượng vết loét và khu trú của chúng. Viêm loét dạ dày nhiều gấp 3 lần nam giới. Hình ảnh lâm sàng trong trường hợp này phụ thuộc vào việc định vị các khuyết tật ở đường tiêu hóa. Với các vết loét trong dạ dày, đau âm ỉ vùng thượng vị mà không cần chiếu xạ, xảy ra sau khi ăn 20-30 phút và buồn nôn được ghi nhận. Với loét vùng dưới tim, đặc trưng là những cơn đau âm ỉ dưới quá trình xiphoid, lan ra nửa bên trái của ngực. Loét dạ dày và loét tá tràng kết hợp là sự kết hợp giữa một ổ loét dạ dày hoạt động và một ổ loét tá tràng đã lành. Chúng được đặc trưng bởi hội chứng đau duy trì lâu dài, diễn biến dai dẳng của bệnh, bệnh tái phát thường xuyên, vết loét chậm liền sẹo và thường xuyên có biến chứng. Loét ngoài bao gồm các vết loét nằm trong vùng của cơ thắt hành tá tràng và xa nó. Bệnh cảnh lâm sàng của họ có những đặc điểm riêng và có nhiều điểm chung với loét tá tràng. Chúng xảy ra chủ yếu ở những bệnh nhân từ 40-60 tuổi. Loét hậu môn rất nghiêm trọng và dễ bị kịch phát, kèm theo chảy máu ồ ạt. Đau khu trú ở phần tư trên bên phải của bụng, lan ra sau hoặc dưới xương bả vai phải, xảy ra trong 100% trường hợp. Cường độ, mức độ đau giảm dần sau khi uống thuốc giảm đau có chất gây mê đưa bệnh nhân đến tình trạng suy nhược thần kinh nặng. Tính chất theo mùa của các đợt cấp trong loét ngoài củ được ghi nhận ở gần 90% bệnh nhân. Ở nhiều bệnh nhân, xuất huyết tiêu hóa trở thành một triệu chứng chính. Loét ống môn vị được đặc trưng bởi một phức hợp triệu chứng được gọi là hội chứng môn vị: đau vùng thượng vị, buồn nôn, nôn và sụt cân đáng kể. Đợt cấp của bệnh rất lâu. Trong bối cảnh điều trị bằng thuốc chống đông đặc, vết loét liền sẹo trong vòng 3 tháng. Lượng máu cung cấp dồi dào đến ống môn vị gây chảy máu dạ dày ồ ạt. Chẩn đoán. Trong quá trình loét dạ dày tá tràng không biến chứng, không có thay đổi nào trong xét nghiệm máu nói chung, có thể giảm nhẹ ESR và tăng hồng cầu nhẹ. Khi các biến chứng phát sinh trong xét nghiệm máu, thiếu máu xuất hiện, tăng bạch cầu - khi phúc mạc tham gia vào quá trình bệnh lý. Không có thay đổi trong phân tích chung của nước tiểu. Trong phân tích sinh hóa máu trong các trường hợp loét dạ dày tá tràng có diễn tiến phức tạp, có thể thay đổi các thông số của xét nghiệm sialic, protein phản ứng C, phản ứng DPA. Phương pháp nghiên cứu truyền thống trong bệnh lý dạ dày là xác định nồng độ axit trong dạ dày. Có thể có các chỉ số khác nhau: tăng và bình thường, trong một số trường hợp thậm chí còn giảm. Loét tá tràng xảy ra khi dịch vị có tính axit cao. Khi kiểm tra bằng tia X, một ổ loét dạ dày tá tràng là một "ngách" - một kho chứa hỗn dịch bari. Ngoài triệu chứng chụp X quang trực tiếp như vậy, các dấu hiệu gián tiếp của khiếm khuyết ở dạ dày rất quan trọng trong chẩn đoán: tăng tiết các chất trong dạ dày khi bụng đói, rối loạn di tản, trào ngược tá tràng, rối loạn chức năng tim, co thắt cục bộ, hội tụ các nếp gấp niêm mạc, dị dạng cicatricial của dạ dày và tá tràng. Nội soi dạ dày tá tràng với sinh thiết là phương pháp đáng tin cậy nhất để chẩn đoán loét dạ dày tá tràng. Nó cho phép bạn đánh giá bản chất của những thay đổi trong màng nhầy ở rìa vết loét, trong vùng quanh ổ và đảm bảo độ chính xác của chẩn đoán ở cấp độ hình thái. Trong các nghiên cứu nội soi và hình thái học, người ta nhận thấy rằng hầu hết các vết loét dạ dày nằm ở vùng có độ cong nhỏ hơn và vùng hang vị, ít thường xuyên hơn - ở vùng có độ cong lớn hơn và ở vùng của ống môn vị. 90% loét tá tràng nằm ở vùng bulbar. Vết loét dạ dày tá tràng thường có hình tròn hoặc hình bầu dục. Đáy của nó gồm các khối hoại tử, dưới có mô hạt. Sự xuất hiện của các vết sẫm màu dưới đáy chứng tỏ đang chảy máu. Giai đoạn lành vết loét được đặc trưng bởi sự giảm sung huyết của màng nhầy và trục viêm trong vùng quanh mô. Vết khuyết trở nên ít sâu hơn, sạch dần các mảng xơ vữa. Vết sẹo trông giống như một vùng xung huyết của màng nhầy với các vết co rút tuyến tính hoặc hình sao của thành. Trong tương lai, trong quá trình kiểm tra nội soi tại vị trí của vết loét trước đây, người ta xác định được nhiều vi phạm khác nhau về sự giảm nhẹ của màng nhầy: biến dạng, sẹo, hẹp. Khi nội soi, sẹo trưởng thành do khuyết tật thay thế bằng mô hạt có màu trắng đục, không có dấu hiệu viêm hoạt động. Một nghiên cứu hình thái học của một mẫu sinh thiết thu được từ đáy và các cạnh của vết loét cho thấy mảnh vụn tế bào ở dạng tích tụ chất nhầy với sự kết hợp của bạch cầu đang phân hủy, hồng cầu và các tế bào biểu mô bong tróc với các sợi collagen nằm bên dưới. Chẩn đoán phân biệt. Với việc sử dụng rộng rãi nội soi, việc chẩn đoán phân biệt các vết loét dạ dày và tá tràng (loét có triệu chứng, loét cụ thể ở bệnh lao, giang mai, bệnh Crohn, ung thư loét nguyên phát, loét ác tính thứ phát) trở nên đặc biệt quan trọng. Đối với loét có triệu chứng, phải xác định được nguyên nhân gây ra (tiếp xúc quá mức, dấu hiệu lâm sàng và hình thái của các bệnh nội tiết, rối loạn tim mạch và hô hấp, bệnh thấp khớp). Hơn cả đối với loét dạ dày tá tràng, chúng được đặc trưng bởi nhiều tổn thương, khu trú chủ yếu trong dạ dày và kích thước đáng kể. Với loét dạ dày tá tràng, hội chứng đau chiếm ưu thế, và với viêm dạ dày mãn tính - hiện tượng khó tiêu. Trong viêm dạ dày mãn tính, cơn đau nhẹ hoặc không có, không có tính chất theo mùa của bệnh và hạn chế khi sờ nắn; mức độ nặng thêm của bệnh thường phụ thuộc vào bản chất của thức ăn. Tình trạng chức năng bài tiết của dạ dày với bệnh viêm dạ dày có thể khác nhau. Có tầm quan trọng quyết định là nội soi dạ dày và sinh thiết dạ dày, trong đó phát hiện những thay đổi niêm mạc đặc trưng của viêm dạ dày và vết loét trong loét dạ dày tá tràng. Thoát vị Hiatus (HH) cũng thường kèm theo đau vùng thượng vị. Tuy nhiên, không giống như bệnh viêm loét dạ dày tá tràng, bệnh này có đặc điểm chủ yếu là bệnh nhân tuổi càng cao, mối liên hệ của cơn đau với vị trí của cơ thể (đau tăng khi nằm ngửa, yếu dần khi nằm thẳng). Chẩn đoán HH được xác nhận bằng kết quả chụp X-quang. Viêm túi mật mãn tính có đặc điểm là đau vùng hạ vị và thượng vị bên phải, thường lan tỏa xuống bả vai phải, đến vai, đến góc hàm dưới bên phải. Với viêm túi mật có tính chất, chúng có đặc điểm buồn tẻ, đơn điệu, bức bách, và với viêm túi mật có tính chất, chúng có đặc tính đau bụng. Buồn nôn, táo bón, đầy hơi được ghi nhận. Có thể xảy ra tình trạng viêm gan dưới dai dẳng. Với sự tắc nghẽn kéo dài của đường mật, vàng da có thể tham gia. Chẩn đoán tổn thương hệ thống đường mật được xác minh qua dữ liệu siêu âm ổ bụng, chụp X-quang (chụp túi mật), chụp mật tụy ngược dòng nội soi (ERCP), cũng như kết quả đo âm tá tràng, chỉ được chỉ định cho quy trình không sỏi. Trong viêm tụy cấp và đợt cấp của cơn đau mãn tính, cơn đau khu trú ở nửa bên trái của vùng thượng vị, có đặc điểm giống bệnh zona và bị kích thích khi ăn bất kỳ thức ăn nào. Trong tiền sử - bệnh lý của hệ thống mật, lạm dụng rượu, sử dụng lâu dài các loại thuốc tuyến tụy. Khách quan tiết lộ giảm cân, đa phân, tăng tiết mỡ, tạo máu. Chẩn đoán được xác nhận bằng kết quả xét nghiệm máu sinh hóa tìm enzym tuyến tụy, phân - về khả năng tiêu hóa, cũng như dữ liệu công cụ. Điều trị. Liệu pháp điều trị loét dạ dày tá tràng hợp lý cần bao gồm một chế độ, dinh dưỡng hợp lý, điều trị bằng thuốc, tâm lý trị liệu, vật lý trị liệu và phương pháp spa. Trong giai đoạn bệnh loét dạ dày trầm trọng hơn, cần tuân thủ nghiêm ngặt chế độ ăn kiêng theo từng phần (từ 4 đến 6 lần một ngày với lượng nhỏ mỗi khẩu phần ăn vào những giờ nhất định). Sản phẩm thực phẩm phải có đặc tính đệm tốt và chứa đủ lượng protein (120–140 g). Liệu pháp tâm lý là điều cần thiết để ngăn chặn hoặc giảm các phản ứng tâm thần kinh phát sinh từ hội chứng đau dai dẳng và sự mong đợi của nó. Thuốc điều trị viêm loét dạ dày tá tràng được chia thành 5 nhóm: 1) thuốc ảnh hưởng đến yếu tố axit-pepic (thuốc kháng axit và H2thuốc chẹn histamine, các chất chống bài tiết khác); 2) thuốc cải thiện hàng rào niêm mạc dạ dày; 3) thuốc làm tăng tổng hợp các prostaglandin nội sinh; 4) chất kháng khuẩn và chất khử trùng; 5) thuốc bình thường hóa rối loạn vận động sơ tán của dạ dày và tá tràng. Thuốc kháng axit: 1) hòa tan (có thể hấp thụ) - bicacbonat soda, canxi cacbonat (phấn) và magie oxit (magie cháy); 2) không hòa tan (không hấp thụ): magie trisilicat và nhôm hydroxit. Thuốc kháng axit hòa tan có tác dụng kiềm hóa nhanh, mạnh nhưng ngắn hạn nhưng thường gây ra tác dụng phụ nên không được sử dụng trong điều trị loét dạ dày tá tràng. Thuốc kháng axit không hòa tan dựa trên nhôm hydroxit và magie hydroxit (Almagel, Phosphalugel, Gelusillac, Topaal, Maalox, v.v.) giúp trung hòa lâu dài axit clohydric, bao bọc màng nhầy, bảo vệ nó khỏi tác hại của axit và thức ăn. Ngoài việc trung hòa axit clohydric, chúng còn giúp làm giảm hoạt động phân giải protein của dịch dạ dày, liên kết lysolecithin và axit mật, đồng thời có tác dụng bảo vệ tế bào phổ quát. Thuốc kháng axit nên được dùng sau bữa ăn và buổi tối 1-2 giờ. Maalox được kê đơn dưới dạng hỗn dịch (15 ml 4 lần một ngày) hoặc viên nén (1-2 viên 4 lần một ngày), phosphalugel - ở dạng gel (16 g 3-4 lần một ngày). Một trong những tác dụng phụ chính của thuốc kháng axit không hấp thụ là rối loạn phân. Các chế phẩm hydroxit nhôm gây táo bón, và các chế phẩm magie hydroxit (Maalox) có tác dụng nhuận tràng phụ thuộc vào liều lượng. Một kỷ nguyên mới trong điều trị loét dạ dày tá tràng bắt đầu với sự ra đời của H2- Thuốc chẹn histamine. Trong điều kiện sinh lý, histamine làm trung gian cho thần kinh ngoài dạ dày và các kích thích dịch thể gây ra sự sản xuất axit. Sự kích thích sản xuất axit clohydric của histamine là do sự gia tăng hoạt động của cAMP, hoạt động trên enzyme adenylcyclase, có trong vùng sản xuất axit của dạ dày, giúp tăng cường bài tiết các ion hydro. Dữ liệu thu được là cơ sở để tổng hợp các loại thuốc làm gián đoạn sự tham gia của histamine vào quá trình bài tiết ở cấp độ tế bào, chẳng hạn như cimetidine, ranitidine, famotidine, nizatidine, v.v. Ngoài ra, thuốc kháng H.2Các thụ thể histamine ngăn ngừa các rối loạn vi tuần hoàn trong niêm mạc dạ dày và do đó ngăn ngừa sự phát triển của các vết loét. Ngoài ra, chúng làm giảm sản xuất pepsin, tăng tiết bicarbonat, bình thường hóa nhu động dạ dày tá tràng, tăng số lượng tế bào biểu mô tổng hợp DNA, kích thích quá trình tái tạo và đẩy nhanh quá trình chữa lành các vết loét mãn tính dạ dày và tá tràng. Tuy nhiên, thuốc thế hệ 1 (cimetidine, cinamet, belomet, tagamet) có thể gây ra những thay đổi trong hệ thần kinh, viêm gan nhiễm độc, rối loạn nhịp và dẫn truyền trong hệ thống tim mạch, và những thay đổi trong cơ quan tạo máu. Thuốc chẹn H2các thế hệ tiếp theo của thụ thể histamine - ranitidine (zantac, ranisan, gistak), famotidine (kvamatel, lecedil, gastrosidin), nizatidine (roxatidine) khác với cimetidine ở khả năng dung nạp tốt. Ranitidine được kê đơn với liều 150 mg 2 lần một ngày, famotidine - 20 mg 2 lần một ngày trong 4-6 tuần. Để ngăn ngừa hội chứng cai nghiện sau khi lành vết loét, nên tiếp tục dùng ranitidine (150 mg) hoặc famotidine (20 mg) vào ban đêm trong 2-3 tháng. Trong những năm gần đây, một loại thuốc kháng tiết mới omeprazole (omenrol, omez, mấtk), thuộc dẫn xuất benzimidazole, đã xuất hiện. Nó ngăn chặn enzym H + -K + -ATPase của bơm proton của tế bào thành. Thời gian bán thải ngắn (khoảng 1 giờ) và thời gian tác dụng dài (18-24 giờ) nên có thể dùng thuốc này một lần. Omeprazole được kê đơn 20 mg vào ban đêm, 1 lần mỗi ngày trong 2-3 tuần. Omeprazole đứng đầu về mức độ nghiêm trọng của tác dụng kháng tiết trong số các loại thuốc chống tiết máu hiện đại. Tác dụng phụ của thuốc không rõ rệt. Việc sử dụng rộng rãi trong điều trị loét dạ dày tá tràng đã được tìm thấy là Gastcepin (nirenzepine, Gastzepine), thuộc nhóm thuốc kháng cholinergic. Thuốc ngăn chặn một cách chọn lọc các thụ thể muscarinic acetylcholine nằm trong các tế bào niêm mạc dạ dày sản xuất axit clohydric và pepsin. Gastrocepin có tác dụng ức chế bài tiết cơ bản và kích thích dạ dày, ức chế sản xuất pepsin, làm chậm quá trình di chuyển khỏi dạ dày, ức chế sản xuất gastrin, làm giảm mức độ polypeptide của tuyến tụy, có tác dụng bảo vệ tế bào bằng cách tăng sản xuất glycoprotein chất nhầy dạ dày. , cũng như bằng cách cải thiện việc cung cấp máu cho màng nhầy của vùng dạ dày tá tràng. Chỉ định nó cho 50 mg 2 lần một ngày trước bữa ăn 30 phút. Quá trình điều trị là trung bình 4 tuần. Thuốc tăng cường hàng rào nhầy của dạ dày bao gồm chế phẩm keo bismuth (denol), tạo thành màng bảo vệ trên màng nhầy, làm giảm hoạt động tiêu hóa của dạ dày, tạo thành hợp chất không hòa tan với pepsin, tăng cường hình thành chất nhầy, có tác dụng bảo vệ tế bào. có tác dụng làm tăng hàm lượng prostaglandin trong thành dạ dày. Denol có khả năng ức chế hoạt động của HP ở niêm mạc dạ dày. Thuốc được kê đơn 2 viên (240 mg) 2 lần một ngày nửa giờ trước bữa ăn hoặc 2 giờ sau bữa ăn. Để tránh sự tích tụ muối bismuth trong cơ thể, không nên thực hiện điều trị bằng các loại thuốc này trong hơn 8 tuần. Với mục đích điều trị kháng khuẩn cho loét dạ dày và tá tràng, tetracycline, amoxicillin và clarithromycin được sử dụng. Chúng được sử dụng kết hợp với các thuốc chống loét khác. Một số chương trình điều trị phối hợp (hai, ba, bốn thành phần) đã được đề xuất. Liệu pháp hai thành phần: amoxicillin 1000 mg 2 lần một ngày trong 2 tuần; omeprazole 40 mg x 2 lần / ngày. Chương trình ba thành phần bao gồm việc chuẩn bị bismuth dạng keo 120 mg 4 lần một ngày; tetracyclin 250 mg x 4 lần một ngày; metronidazole 250 mg 4 lần một ngày. Chu kỳ điều trị là 14 ngày. Chương trình bốn thành phần bao gồm omeprazole 20 mg 2 lần một ngày từ ngày thứ nhất đến ngày thứ 1; de-nol 10 mg 120 lần một ngày từ ngày thứ 4 đến ngày thứ 4; tetracyclin 10 mg x 500 lần / ngày từ ngày thứ 4 đến ngày thứ 4; metronidazole 10 mg x 500 lần / ngày từ ngày thứ 3 đến ngày thứ 4. Bài thuốc 10 vị trong điều trị viêm loét dạ dày, tá tràng được công nhận là hiệu quả nhất. 6 tuần sau đó, 93-96% bệnh nhân lành vết thương. Sau khi bị sẹo loét dạ dày và tá tràng, người ta thường áp dụng hai cách điều trị theo phương pháp truyền thống. 1) Điều trị duy trì liên tục được thực hiện với thuốc kháng tiết với liều lượng một nửa hàng ngày trong thời gian lên đến một năm. 2) Liệu pháp "theo yêu cầu", liên quan đến việc sử dụng một trong các chất chống bài tiết với liều lượng một nửa hàng ngày trong hai tuần khi các triệu chứng của loét dạ dày tá tràng xuất hiện. Dự báo và phòng ngừa. Các dạng bệnh không biến chứng có tiên lượng thuận lợi cho cuộc sống và công việc. Trong trường hợp biến chứng của bệnh loét dạ dày tá tràng, tiên lượng được xác định bởi tính kịp thời của việc chăm sóc phẫu thuật. Phòng ngừa tái phát loét dạ dày tá tràng bao gồm theo dõi năng động với việc tái khám bắt buộc bởi bác sĩ 2 lần một năm. Kiểm tra nên bao gồm lâm sàng và nội soi, và nếu cần thiết, kiểm tra hình thái học. Để phòng ngừa, bạn nên bình thường hóa giấc ngủ và nghỉ ngơi, từ bỏ các thói quen xấu, hạn chế uống thuốc gây loét, 3 bữa ăn hợp lý mỗi ngày và sử dụng liệu pháp XNUMX hoặc XNUMX thành phần trong một tuần sau mỗi XNUMX tháng. BÀI GIẢNG SỐ 12. Các bệnh về đường tiêu hóa. Các bệnh về đường ruột. Các bệnh của ruột non. Viêm ruột mãn tính Viêm ruột mãn tính là một bệnh của ruột non, được đặc trưng bởi sự vi phạm các chức năng của nó (tiêu hóa và hấp thụ) trên nền của những thay đổi loạn dưỡng và rối loạn tái tạo, đỉnh điểm là sự phát triển của viêm, teo và xơ cứng màng nhầy của ruột non. Nguyên nhân và sinh bệnh học. Đây là một bệnh đa nguyên nhân có thể là kết quả của tình trạng viêm cấp tính ở ruột non hoặc một quá trình mãn tính nguyên phát. Trong những năm gần đây, Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, rotavirus, nhiều đại diện của động vật nguyên sinh và giun sán (giardia, giun đũa, sán dây, opisthorchia, cryptosporidium) đã được coi trọng như một yếu tố căn nguyên gây bệnh viêm ruột mãn tính. Điều quan trọng trong sự xuất hiện của viêm ruột mãn tính là các yếu tố gia vị - ăn quá nhiều, ăn thức ăn khô, thức ăn không cân bằng, chủ yếu là carbohydrate, lạm dụng gia vị. Viêm ruột là do bức xạ ion hóa, tiếp xúc với chất độc hại và thuốc. Trong số các cơ chế sinh bệnh phổ biến của các bệnh mãn tính ở ruột non, có những thay đổi trong hệ vi sinh đường ruột trên cơ sở giảm khả năng miễn dịch cục bộ và nói chung. Những thay đổi trong tình trạng miễn dịch - giảm hàm lượng IgA tiết, tăng mức IgE, giảm chuyển dạng tế bào lympho và ức chế sự di chuyển của bạch cầu - dẫn đến sự xâm nhập của ruột non bởi các đại diện của hệ vi sinh cơ hội và giảm hệ thực vật kỵ khí bình thường. Khuẩn lạc ở ruột non giúp tăng cường bài tiết dịch ruột do hoạt hóa cAMP của tế bào biểu mô, làm tăng tính thấm của ruột, tăng cường sản xuất điện giải và nước của tế bào. Sự tiết nước và chất điện giải dẫn đến vi phạm chuyển hóa nước-muối. Dưới tác động của hệ vi sinh vật, quá trình lưu thông đường ruột của mật bị rối loạn. Các axit béo liên kết các ion canxi, tạo thành xà phòng hòa tan ít được thải ra ngoài theo phân. Vi phạm chuyển hóa canxi được thúc đẩy bởi những thay đổi trong chuyển hóa của vitamin D, làm giảm sự hấp thu canxi. Dưới tác động của rối loạn chuyển hóa các vitamin tan trong mỡ, hàm lượng các nguyên tố vi lượng trong máu giảm dần. Tình trạng rối loạn sinh học kéo dài thúc đẩy sự nhạy cảm với các kháng nguyên vi sinh vật và thức ăn, gây viêm màng nhầy miễn dịch, dẫn đến hình thành các kháng nguyên mô. Sự gia tăng tính thấm của hàng rào niêm mạc đi kèm với sự tái hấp thu các đại phân tử protein không đúng vị trí, chúng trở thành chất gây dị ứng, và phản ứng miễn dịch bị suy giảm. Khi bị dị ứng, các hoạt chất sinh học được giải phóng làm tăng tính thấm của thành ruột, thay đổi tính chất chức năng của tế bào ruột. Vi phạm cấu trúc vi mô của màng tế bào chất của tế bào ruột dẫn đến ức chế hoạt động của lactase trước tiên, sau đó là hoạt động của maltase và sucrase. Với những thay đổi loạn dưỡng, rối loạn tái tạo trong tế bào biểu mô, sự tổng hợp các enzym và sự hấp thụ của chúng trên màng tế bào biểu mô - disaccharidases, peptidases, enterokinase, alkaline phosphatase - bị giảm, gây ra rối loạn tiêu hóa cả màng và khoang. Tất cả điều này trở thành cơ sở của hội chứng kém hấp thu. Trong giai đoạn đầu của bệnh, rối loạn chuyển hóa lipid phát triển do giảm hấp thu chất béo, mất chất béo theo phân và những thay đổi trong giai đoạn tuần hoàn mật ruột của gan ruột. Do đó, vi phạm chuyển hóa mật dẫn đến rối loạn chuyển hóa lipid, ảnh hưởng đến cấu trúc và chức năng của màng tế bào. Liên quan đến việc hấp thụ không đủ chất béo, sự vi phạm tổng hợp steroid xảy ra, gây ra sự vi phạm các chức năng của các tuyến nội tiết. Về mặt hình thái, viêm ruột mãn tính được biểu hiện bằng những thay đổi viêm và rối loạn tái tạo ở màng nhầy của ruột non. Nếu quá trình tiến triển, chúng ta có thể quan sát thấy hiện tượng teo và xơ cứng của nó. Phân loại (Zlatkina A. R., Frolkis A. V., 1985). 1) Căn nguyên: nhiễm trùng đường ruột, sự xâm nhập của giun xoắn, các yếu tố vật lý và hóa học, các bệnh về dạ dày, tuyến tụy, đường mật. 2) Các giai đoạn của bệnh: đợt cấp; thuyên giảm. 3) Mức độ nặng nhẹ: nhẹ; vừa phải; nặng. 4) Hiện tại: đơn điệu; tái diễn; liên tục tái diễn; ngầm. 5) Đặc điểm biến đổi hình thái: eunit không teo; viêm bao quy đầu với teo lông nhung một phần vừa phải; viêm bao quy đầu với teo một phần nhung mao; eunit bị teo toàn bộ lông nhung. 6) Bản chất của rối loạn chức năng: rối loạn tiêu hóa qua màng (thiếu men disaccharidase), kém hấp thu nước, điện giải, nguyên tố vi lượng, vitamin, protein, chất béo, chất bột đường. 7) Các biến chứng: viêm đơn độc, viêm trung bì không đặc hiệu. Ảnh lâm sàng. Hình ảnh lâm sàng của viêm ruột mãn tính bao gồm các hội chứng ruột cục bộ và toàn thân. Nguyên nhân đầu tiên là do vi phạm các quá trình tiêu hóa thành (màng) và khoang (chứng kém tiêu hóa). Bệnh nhân phàn nàn về đầy hơi, đau ở vùng cạnh rốn, đầy hơi hình mũ, ầm ầm, tiêu chảy và ít gặp hơn là táo bón. Sờ nắn cho thấy cơn đau ở vùng trung vị, cũng như ở bên trái và phía trên rốn (dấu hiệu Porges dương tính), tiếng ồn ào ở khu vực manh tràng (dấu hiệu Obraztsov). Phân có dạng đất sét và đặc trưng là chất đa phân. Hội chứng đường ruột nói chung có liên quan đến sự suy giảm hấp thu các thành phần thức ăn (kém hấp thu), dẫn đến rối loạn tất cả các loại chuyển hóa, thay đổi cân bằng nội môi. Đặc trưng bởi rối loạn chuyển hóa nhiều mặt, chủ yếu là protein, biểu hiện bằng sự sụt giảm trọng lượng cơ thể. Các thay đổi trong chuyển hóa carbohydrate ít rõ rệt hơn, biểu hiện bằng đầy hơi, sôi bụng và tiêu chảy nhiều hơn khi dùng các sản phẩm từ sữa. Ở mức độ lớn, sự thiếu hụt trọng lượng cơ thể của bệnh nhân không chỉ do protein, mà còn do mất cân bằng lipid. Thay đổi chuyển hóa lipid có liên quan mật thiết đến rối loạn chuyển hóa vitamin và khoáng chất hòa tan trong mỡ (canxi, magie, photpho). Các dấu hiệu đặc trưng của tình trạng thiếu canxi là triệu chứng dương tính của cơ lăn, co giật, gãy xương “không động lực” tái phát, loãng xương, nhuyễn xương. Ngoài ra còn bị sưng mặt, tím tái môi, viêm lưỡi, bứt rứt, ăn ngủ kém. Vi phạm cân bằng nước và điện giải được biểu hiện bằng suy nhược chung, kém hoạt động thể chất, hạ huyết áp cơ, buồn nôn, nôn và những thay đổi trong hệ thống thần kinh trung ương. Các triệu chứng của polyhypovitaminosis trở thành điển hình cho bệnh viêm ruột mãn tính ở mức độ trung bình và nặng. Hypovitaminosis C biểu hiện lâm sàng bằng chảy máu nướu răng, chảy máu mũi, tử cung nhiều lần, bầm tím trên da. Hypovitaminosis B đi kèm với xanh xao của da, viêm lưỡi, viêm miệng góc (cheilez). Dấu hiệu thiếu hụt các vitamin tan trong chất béo (A, O, E, K): thị lực lúc chạng vạng kém, da và niêm mạc bị khô, tăng chảy máu nướu. Các dạng nặng của viêm ruột mãn tính xảy ra với các triệu chứng của rối loạn chức năng nội tiết (suy tuyến sinh dục). Chứng suy nhược thần kinh biểu hiện bằng hạ huyết áp động mạch, rối loạn nhịp tim, chán ăn, da mất sắc tố. Giảm hoạt động của tuyến sinh dục kèm theo rối loạn chức năng buồng trứng, rối loạn kinh nguyệt, ở nam giới - liệt dương, nữ hóa tuyến vú, rụng tóc. Rối loạn chức năng tuyến giáp được đặc trưng bởi suy nhược chung, da khô, nhịp tim chậm, giảm hiệu suất và rối loạn trí nhớ-trí tuệ. Chẩn đoán và chẩn đoán phân biệt. Xét nghiệm máu tổng quát cho thấy thiếu máu vi mô và hồng cầu vĩ mô, tăng ESR và trong những trường hợp nghiêm trọng - giảm bạch cầu và bạch cầu ái toan. Nếu bệnh có nguồn gốc ký sinh, có thể thấy tăng bạch cầu lympho và tăng bạch cầu ái toan trong máu. Kiểm tra bằng phương pháp soi cầu cho thấy một loại tăng tiết mỡ ở ruột do axit béo và xà phòng, chất tạo mủ, bệnh amylorrhea. Hàm lượng enterokinase và phosphatase kiềm trong phân tăng lên. Khối lượng phân hàng ngày tăng lên đáng kể. Phân tích vi khuẩn học trong phân cho thấy chứng loạn khuẩn ở các mức độ khác nhau. Có sự giảm sút về lacto- và bifidobacteria, enterococci, các chủng Escherichia coli với các đặc tính enzym bị thay đổi xuất hiện. Trong phân tích chung về nước tiểu trong bệnh viêm ruột mãn tính nặng, albumin niệu vi lượng và tiểu ít được ghi nhận. Trong xét nghiệm máu sinh hóa, người ta phát hiện thấy giảm protein huyết, giảm albumin máu, hạ đường huyết, hạ canxi máu, giảm mức magiê, phốt pho và các nguyên tố vi lượng khác, rối loạn chuyển hóa điện giải dưới dạng giảm mức natri và kali. Rối loạn chuyển hóa lipid kèm theo sự thay đổi phổ lipid: mức cholesterol, phospholipid giảm, và phổ acid mật, phospholipid và triglycerid cũng thay đổi. Kết quả của một nghiên cứu X-quang cho phép chúng tôi làm rõ chức năng vận động của ruột non và sự giảm nhẹ của niêm mạc, những thay đổi về rối loạn vận động và rối loạn vận động dưới dạng làm chậm lại hoặc tăng tốc quá trình truyền hỗn dịch bari sulfat qua tiểu ruột, và sự giảm bớt của niêm mạc thay đổi dưới dạng dày lên không đồng đều, biến dạng và làm mịn các nếp gấp. Nội soi dạ dày tá tràng cho thấy viêm teo dạ dày và viêm tá tràng. Hình ảnh hình thái của một dạng nhẹ của viêm ruột mãn tính được đặc trưng bởi sự dày lên của các nhung mao, sự biến dạng của chúng, giảm độ sâu của các khía, giảm trương lực của cơ trơn, phù nề dưới biểu mô, những thay đổi thoái hóa trên bề mặt của biểu mô. , làm mỏng đường viền bàn chải của các tế bào, giảm số lượng tế bào hình cốc trong vùng nhung mao, tăng số lượng các crypts, thâm nhiễm niêm mạc lớp riêng với các yếu tố lymphoplasmacytic, giảm các tế bào Paneth trong khu vực ở dưới cùng của các đoạn mã. Đối với dạng trung bình, teo một phần nhung mao, giảm số lượng các nếp nhăn, mỏng màng nhầy, giảm đường viền bàn chải, và thâm nhiễm lymphoplasmacytic của các lớp dưới niêm mạc và cơ là những điển hình. Thể nặng của bệnh được đặc trưng bởi tình trạng teo nhung mao tiến triển, được chẩn đoán bằng các tiêu chuẩn mô học, mô bệnh học và hình thái học. Quá trình tăng sinh của các tế bào ruột chiếm ưu thế trong quá trình biệt hóa của chúng, một lượng lớn các tế bào chưa trưởng thành, khiếm khuyết xuất hiện. Chẩn đoán phân biệt trong viêm ruột mãn tính được thực hiện với bệnh celiac, bệnh Crohn, bệnh Whipple, bệnh amyloidosis ruột, bệnh túi thừa, ung thư hạch, khối u của ruột non. Chung cho tất cả các tình trạng này là các hội chứng lâm sàng về khó tiêu, hấp thu và loạn khuẩn. Chẩn đoán cuối cùng được xác nhận bằng cách kiểm tra hình thái của màng nhầy của ruột non. Vì vậy, đối với bệnh ruột celiac, một dấu hiệu bệnh học về mối quan hệ của các đợt cấp của bệnh với việc sử dụng các sản phẩm có chứa gliadin là điển hình. Phòng khám của bệnh ruột celiac tương tự như bệnh viêm ruột mãn tính. Thông thường, phần ruột trên bị ảnh hưởng và không có thay đổi ở hồi tràng. Vị trí tối ưu để lấy bệnh phẩm sinh thiết là vùng niêm mạc gần dây chằng Treitz. Kiểm tra hình thái cho thấy sự giảm số lượng tế bào cốc và sự gia tăng số lượng tế bào lympho trên biểu mô, teo nhung mao phụ và thâm nhiễm tế bào viêm trên chính lớp của nó. Với bệnh ruột celiac, những thay đổi về hình thái trên nền của một chế độ ăn không có gluten có thể đảo ngược được, ngược lại với viêm ruột mãn tính tầm thường, trong đó những thay đổi về hình thái là không thể đảo ngược. Trong bệnh Crohn, đa hình lâm sàng được ghi nhận, do nguồn gốc tự miễn của bệnh và các biểu hiện toàn thân đặc trưng của nó (như viêm tuyến giáp tự miễn, viêm đa khớp, viêm mống mắt, viêm gan, kết hợp thường xuyên của viêm ruột và viêm đại tràng xa). Các xét nghiệm nội soi và hình thái học có độ phân giải cao trong việc xác minh bệnh Crohn, cho thấy bản chất khảm của tổn thương ruột, những thay đổi điển hình của kiểu "vỉa hè lát sỏi" xen kẽ với những vùng niêm mạc còn nguyên vẹn. Chụp Xquang, nội soi có thể phát hiện thấy các vết thắt ruột, đôi khi hình thành các lỗ rò ruột. Chẩn đoán hình thái cho biết sự xâm nhập của tế bào viêm vào tất cả các lớp của thành ruột với tổn thương tối đa ở lớp dưới niêm mạc và những thay đổi tối thiểu trên niêm mạc. Trong lớp dưới niêm mạc, các u hạt giống sarcoid lymphocytic, bệnh tiên lượng cho bệnh này, được tìm thấy. Đối với bệnh Whipple, ngoài các dấu hiệu của viêm ruột, các biểu hiện ngoài đường tiêu hóa như sốt, viêm khớp, nổi hạch, hạ huyết áp động mạch và sắc tố da là đặc trưng. Các tiêu chí hình thái thông tin nhất của bệnh. Sinh thiết lấy từ ruột non cho thấy sự tích tụ chất béo trong và ngoài tế bào trong niêm mạc ruột non và các hạch bạch huyết mạc treo; xâm nhập vào lớp của chính nó bởi các vi lớn chứa các hạt không béo dương tính với CHIC, và sự hiện diện của trực khuẩn trong niêm mạc. Điều trị. Điều trị viêm ruột mãn tính phải toàn diện, bao gồm các tác nhân ảnh hưởng đến yếu tố căn nguyên, cơ chế gây bệnh, cũng như các triệu chứng cục bộ và chung của bệnh. Cơ sở là chế độ dinh dưỡng, giúp giảm áp suất thẩm thấu tăng lên trong khoang ruột, giảm bài tiết và bình thường hóa sự vận chuyển của các chất trong ruột. Loại trừ các sản phẩm có chứa chất xơ thực vật thô (rau sống, trái cây, bánh mì lúa mạch đen, các loại hạt, bánh ngọt, thực phẩm đóng hộp, gia vị, món ăn cay, sữa nguyên kem, bia, kvass, đồ uống có ga và cồn). Việc sử dụng muối ăn bị hạn chế. Các bữa ăn chia nhỏ là cần thiết, lên đến 5-6 lần một ngày. Trong thời kỳ thuyên giảm, một số loại rau và trái cây được đưa vào chế độ ăn uống, lên đến 100-200 g mỗi ngày. Chỉ định xà lách, cà chua chín bóc vỏ, lê mềm, táo ngọt, cam, quýt, mâm xôi, dâu tây, dâu rừng. Thức ăn nên được luộc hoặc hấp. Điều trị bằng thuốc phải có tác dụng gây bệnh, gây bệnh và triệu chứng. Điều trị Etiotropic: đối với chứng rối loạn sinh học độ II-IV, thuốc kháng khuẩn được kê đơn: metronidazole (0,5 g 3 lần một ngày), clindamycin (0,5 g 4 lần một ngày), cehalexin (0,5 g 2 lần một ngày). ngày), biseptol ( 0,48 g 2 lần một ngày), sulgin (1 g 3-4 lần một ngày), furazolidone (0,1 g 4 lần một ngày). Sau khi sử dụng thuốc kháng khuẩn, eubiotic được kê đơn - bifidumbacterin hoặc biificol 5 liều 3 lần một ngày trước bữa ăn 30 phút, coli-bacterin hoặc lactobacterin 3 liều 3 lần một ngày trước bữa ăn, hilakforte 40 giọt 3 lần một ngày trước bữa ăn. Điều trị bằng chế phẩm vi khuẩn được thực hiện trong thời gian dài: 3 đợt, mỗi đợt 3 tháng. Đối với chứng rối loạn vi khuẩn tụ cầu, một loại vi khuẩn chống tụ cầu được kê toa (20 ml 3 lần một ngày trong 15-20 ngày), đối với chứng rối loạn vi khuẩn proteus - vi khuẩn coliprotean bằng đường uống, 20 ml 3 lần một ngày, quá trình điều trị là 2-3 tuần. Là một thuốc điều trị triệu chứng tiêu chảy, imodium (loperamide) được kê đơn 1 viên 2-3 lần một ngày trước bữa ăn trong 3-5 ngày. Để cải thiện quá trình tiêu hóa, các loại men được khuyến nghị: pancreatin, panzinorm forte, festal, digal, pankurmen, mezim forte, trienzyme, liều lượng được lựa chọn riêng lẻ (từ 1 viên 3 lần một ngày đến 3-4 viên 4 lần một ngày ) và được kê đơn trực tiếp trước hoặc trong bữa ăn trong 2-3 tháng. Nếu cần thiết, liệu pháp thay thế enzym được tiếp tục trong thời gian dài hơn. Để bình thường hóa tình trạng chung của bệnh nhân bị viêm ruột và loại bỏ các rối loạn chuyển hóa, liệu pháp thay thế được chỉ định. Để bù đắp sự thiếu hụt vitamin, vitamin B và B được kê đơn trong 4-5 tuần.6 Mỗi loại 50 mg, PP - 10-30 mg, C - 500 mg mỗi loại. Đối với chứng tăng tiết mỡ, tiêm vitamin B được chỉ định.2 (100-200 mcg) kết hợp với các vitamin tan trong chất béo. Riboflavin 0,02 g, axit folic 0,003 g mỗi ngày một lần, vitamin E 3300 IU 2 lần một ngày được kê đơn bên trong. Trong viêm ruột mãn tính xảy ra với sự thiếu hụt protein nghiêm trọng, cùng với chế độ ăn kiêng, tiêm huyết tương, 150-200 ml protein thủy phân và hỗn hợp các axit amin (aminopeptide, alvesin, polyamine, intrafusin, 250-500 ml tiêm tĩnh mạch trong 20 ngày) trong kết hợp với hormon đồng hóa (tiêm lại 2,0 ml 1 lần trong 7-10 ngày trong 3-4 tuần) và hỗn hợp béo như intralipid. Việc bổ nhiệm steroid chỉ được chỉ định khi thiếu protein đáng kể, giảm protein huyết, sự hiện diện của suy thượng thận. Để điều chỉnh rối loạn nước và điện giải, tiêm tĩnh mạch panangin 20-30 ml, calci gluconat 10% 10-20 ml trong 200-400 ml dung dịch đẳng trương hoặc dung dịch glucose, dung dịch polyionic "Disol", "Trisol", "Quartasol" được chỉ ra. Các dung dịch điện giải được tiêm tĩnh mạch trong 10 - 20 ngày dưới sự kiểm soát của tình trạng axit-bazơ và mức độ điện giải trong máu. Dự báo và phòng ngừa. Tiên lượng về cuộc sống và khả năng làm việc trong hầu hết các trường hợp đều thuận lợi. Các dấu hiệu không thuận lợi về mặt tiên lượng là bệnh tái phát liên tục, giảm cân đột ngột, thiếu máu, hội chứng rối loạn nội tiết (giảm ham muốn tình dục, đau bụng kinh, vô sinh). Phòng ngừa viêm ruột mãn tính bao gồm điều trị kịp thời các bệnh nhiễm trùng đường ruột cấp tính và các bệnh đồng thời của vùng dạ dày tá tràng, tuân thủ chế độ ăn uống, sử dụng dự phòng các chế phẩm vi khuẩn trong quá trình chụp X-quang và xạ trị. BÀI GIẢNG SỐ 13. Các bệnh về đường tiêu hóa. Các bệnh về đường ruột. Bệnh Crohn Bệnh Crohn là một bệnh đường ruột mãn tính với các biểu hiện toàn thân; cơ sở hình thái của đó là viêm tự miễn nhiễm u hạt của đường tiêu hóa. Nguyên nhân và sinh bệnh học. Nguyên nhân và cơ chế bệnh sinh của bệnh chưa được nghiên cứu đầy đủ. Phổ biến nhất là các khái niệm truyền nhiễm và miễn dịch về sự xuất hiện của bệnh. Trong những năm gần đây, đã xuất hiện các báo cáo về vai trò căn nguyên của vi sinh vật thuộc chi Yersinia. Tuy nhiên, rất khó để xác định xem những tác nhân vi sinh vật này là mầm bệnh hay hội sinh. Đồng thời, những thay đổi trong hệ vi sinh đường ruột đóng vai trò quan trọng trong cơ chế bệnh sinh của bệnh. Điển hình là sự giảm số lượng vi khuẩn loại bifidum với sự gia tăng đồng thời của vi khuẩn đường ruột với các dấu hiệu gây bệnh. Cơ chế tự miễn dịch đóng một vai trò trong sự phát triển của bệnh. Trong bệnh Crohn, xuất hiện các tự kháng thể (IgC, IgM) chống lại các mô ruột. Cơ sở hình thái của bệnh là một quá trình viêm tự miễn dịch xảy ra ban đầu ở lớp dưới niêm mạc, lan đến toàn bộ bề dày của thành ruột và được đặc trưng bởi sự hiện diện của thâm nhiễm u hạt, sau đó là loét màng nhầy, sự phát triển của áp xe và lỗ rò có thể chữa lành với sự hình thành sẹo và hẹp lòng ruột. Với sự gia tăng thời gian của bệnh, mức độ tổn thương tăng lên và các triệu chứng rối loạn tiêu hóa ngoài xuất hiện. Phân loại. Phân loại (F.I. Komarov, A.I. Kazanov, 1992). 1) Khóa học: cấp tính; mãn tính. 2) Đặc điểm của quá trình: tổn thương trong ruột non; tổn thương trong vùng hồi tràng; tổn thương trong ruột kết. 3) Các biến chứng: hẹp ruột; giãn đại tràng nhiễm độc; lỗ rò rỉ; bệnh amyloidosis; sỏi thận, sỏi đường mật; TẠI12thiếu máu thiếu máu. Ảnh lâm sàng. Hình ảnh lâm sàng của bệnh Crohn được đặc trưng bởi sự đa dạng đáng kể, được xác định bởi vị trí và mức độ của quá trình bệnh lý ở ruột, dạng bệnh và sự bổ sung các biến chứng. Khởi phát của bệnh có thể là cấp tính, khi bệnh tiến triển ngay từ đầu, và mãn tính khi bệnh bắt đầu từ từ. Trong trường hợp đầu tiên, chẩn đoán thường được thực hiện khi phẫu thuật mở bụng được thực hiện để nghi ngờ viêm ruột thừa, hoặc tắc ruột phát triển mà không có lý do rõ ràng ở những người trẻ tuổi. Đồng thời, một vùng xung huyết của ruột non, các hạch bạch huyết mở rộng của rễ mạc treo tràng, đặc trưng của bệnh Crohn, được tìm thấy. Bệnh nhân kêu đau bụng không khu trú cụ thể, phân lỏng không có tạp chất bệnh lý, sụt cân, thân nhiệt thấp. Một nghiên cứu khách quan chú ý đến sự xanh xao của da, tương quan với mức độ nghiêm trọng của tình trạng thiếu máu, phù chân do suy giảm khả năng hấp thụ và chuyển hóa protein. Khi sờ bụng, có thể thấy đầy hơi và kêu ầm ầm. Khi quá trình này khu trú ở ruột già, có sự xen kẽ của táo bón với tiêu chảy, đau bụng quặn thắt, phân lỏng hoặc bán thành hình có chứa hỗn hợp máu. Khi đường tiêu hóa trên bị ảnh hưởng, các triệu chứng giống như viêm thực quản mãn tính, viêm dạ dày mãn tính và viêm tá tràng mãn tính xảy ra. Có thể đau sau xương ức khi thức ăn qua thực quản, đau về đêm và “đói” ở thượng vị, đau khi sờ thấy ở vùng hành tá tràng. Khi khám sức khỏe bệnh nhân, người ta xác định được tình trạng xanh xao, xanh xao, thiếu hụt trọng lượng cơ thể, sờ thấy các quai ruột co thắt, đau vùng liệt, vùng chậu phải. Trong bệnh Crohn, các dấu hiệu ngoài đường tiêu hóa của bệnh được ghi nhận: viêm miệng, phình và lỗ rò khoang miệng, viêm khớp, giống viêm khớp dạng thấp tại phòng khám, với các triệu chứng đặc trưng là tổn thương đối xứng các khớp nhỏ, cứng khớp vào buổi sáng. Những thay đổi điển hình ở mắt: viêm mống mắt, viêm mống mắt, bệnh vàng da. Da có thể phát triển ban đỏ nốt sần và viêm da mủ gangrenosum. Tiêu chảy được đặc trưng bởi sự gia tăng số lượng phân lên đến 10 lần một ngày hoặc nhiều hơn, phân nhiều phân. Thể tích của phân được xác định bởi sự định vị giải phẫu của quá trình: với tổn thương ở đoạn gần ruột non, thể tích của phân lớn hơn nhiều so với tổn thương ở các đoạn xa. Giảm cân được ghi nhận ở tất cả các bệnh nhân. Chẩn đoán và chẩn đoán phân biệt. Xét nghiệm máu lâm sàng trong đợt trầm trọng cho thấy tăng bạch cầu, thiếu máu và tăng ESR. Những thay đổi trong phân tích nước tiểu nói chung xuất hiện ở dạng nghiêm trọng, đặc trưng bởi việc bổ sung bệnh amyloidosis ở thận (protein niệu). Xét nghiệm máu sinh hóa cho thấy giảm protein máu, giảm albumin máu, tăng α-globulin, giảm hàm lượng sắt, vitamin B12, axit folic, kẽm, magiê và kali. Các dữ liệu của xét nghiệm tán xạ cho phép đánh giá gián tiếp mức độ tổn thương. Trong chương trình coprogram với nội địa hóa ruột non của quá trình, các chất đa phân, tăng tiết mỡ, tạo trĩ được tìm thấy; trong ruột kết - một hỗn hợp của chất nhầy, bạch cầu, hồng cầu. Chẩn đoán bằng tia X cho phép bạn xác định vị trí và mức độ phổ biến của quá trình bệnh lý trong ruột. Các khu vực của ruột bị ảnh hưởng xen kẽ với các khu vực của ruột không thay đổi. Các vòng bị thay đổi trở nên cứng nhắc, hình ảnh được khảm với các khuyết tật lấp đầy nhỏ và với sự xâm nhập của chất cản quang ra ngoài thành ruột ở dạng túi. Ruột trong khu vực bị ảnh hưởng có đặc điểm của tua mịn, với sự hình thành của các lỗ giả. Khả năng co bóp của thành ruột giảm hoặc mất hoàn toàn, quá trình thoát bari chậm lại. Quan sát thấy sự thu hẹp không đồng đều của lòng ruột, kết quả là nó trở nên hẹp đến mức có dạng như một đường ren. Phía trên vùng thu hẹp, ruột giãn ra. Nội soi chẩn đoán có tầm quan trọng quyết định trong việc xác minh chẩn đoán. Đối với bệnh Crohn, đặc điểm nổi bật nhất là sự thay đổi thành bụng và đoạn ban đầu của tá tràng. Qua nội soi, có thể phát hiện thấy lỗ ức đòn chít hẹp hình tròn, giống như hẹp khối u. Thời kỳ ban đầu của bệnh Crohn được đặc trưng bởi dữ liệu nội soi kém: màng nhầy mờ, có thể nhìn thấy các vết ăn mòn kiểu aphthae, bao quanh bởi các hạt màu trắng. Mô hình mạch máu không có hoặc mịn. Trong lòng ruột và trên thành của nó, chất nhầy có mủ được xác định. Khi thuyên giảm lâm sàng, những thay đổi được mô tả có thể biến mất hoàn toàn. Khi bệnh tiến triển, niêm mạc trở nên dày lên không đồng đều, có màu hơi trắng, và các vết loét bề mặt lớn hoặc vết nứt sâu được ghi nhận. Lòng ruột thu hẹp lại, gây khó khăn cho việc soi ống soi ruột già. Nội soi đại tràng giúp thực hiện sinh thiết nhắm mục tiêu màng nhầy ở bất kỳ phần nào của đại tràng và ở đoạn cuối hồi tràng. Trong bệnh Crohn, quá trình bệnh lý bắt đầu ở lớp dưới niêm mạc, vì vậy sinh thiết phải được thực hiện theo cách sao cho một phần của lớp dưới niêm mạc đi vào vật liệu sinh thiết. Liên quan đến những điều trên, trong 54% trường hợp không phát hiện được chất nền hình thái của bệnh. Cần phân biệt bệnh Crohn với viêm loét đại tràng không đặc hiệu, lao đường tiêu hóa, viêm đại tràng do thiếu máu cục bộ, bệnh Whipple, bệnh túi thừa, viêm đại tràng giả mạc, u lympho, amyloidosis ruột non nguyên phát, viêm ruột mãn tính. Chung cho tất cả các bệnh này là hội chứng rối loạn tiêu hóa đường ruột và một số tổn thương toàn thân. Tuy nhiên, viêm loét đại tràng được đặc trưng bởi sự thay đổi ở các phần xa của đại tràng với sự tham gia bắt buộc của trực tràng và đại tràng xích ma trong quá trình này. Trong viêm loét đại tràng không đặc hiệu, không có sự phân đoạn của tổn thương; ít thường xuyên hơn trong bệnh Crohn, các biểu hiện toàn thân được xác định, và hội chứng kém hấp thu ít rõ ràng hơn. Tuy nhiên, chẩn đoán chính xác nhất của bệnh Crohn được xác nhận bằng nội soi với sinh thiết trúng đích. Dạng bệnh lao đường tiêu hóa được phân biệt với bệnh Crohn bởi khu trú thường xuyên ở hồi tràng, các phát hiện nội soi cho phép phát hiện các vết loét với các cạnh nổi lên, tróc vảy chứa đầy chất màu xám. Những vết loét như vậy sẽ lành lại với sự hình thành của một vết sẹo ngắn, điều này không được quan sát thấy trong bệnh Crohn. Ở người cao tuổi, cần phân biệt bệnh Crohn và viêm đại tràng do thiếu máu cục bộ. Đối với trường hợp thứ hai, các cơn đau dữ dội ở bụng sau khi ăn là điển hình, viêm đại tràng có thể phát hiện bằng phương pháp tưới nước có thể phát hiện ra những thay đổi ở cơ gấp lách, đi xuống và đại tràng sigma. Dấu hiệu X quang quan trọng nhất của bệnh viêm đại tràng do thiếu máu cục bộ là triệu chứng "dấu ngón tay cái". Kiểm tra hình thái và nội soi cho thấy điển hình cho viêm đại tràng do thiếu máu cục bộ các tế bào chứa hemosiderin và xơ hóa trong vật liệu sinh thiết. Việc chẩn đoán bệnh u bạch huyết và bệnh amyloidosis ruột nguyên phát được thực hiện trên cơ sở xét nghiệm mô học. Trong trường hợp đầu tiên, tế bào Berezovsky-Sternberg được tìm thấy trong mẫu sinh thiết từ hạch bạch huyết mạc treo, trong trường hợp thứ hai, có lắng đọng amyloid trong niêm mạc trực tràng. Điều trị. Một chế độ ăn nhẹ nhàng về mặt cơ học và hóa học với hàm lượng protein, vitamin, nguyên tố vi lượng cao được quy định, loại trừ sữa nếu không dung nạp và hạn chế chất xơ thực vật thô. Việc sử dụng các chất thủy phân lỏng qua đường ruột được chỉ định. Các chế phẩm salazop và corticosteroid là cơ sở của liệu pháp điều trị bằng thuốc di truyền bệnh. Liều hàng ngày của thuốc là 3-6 g. Trong trường hợp không có tác dụng của việc sử dụng sulfasalazine, với các tổn thương chủ yếu ở ruột non và các dấu hiệu rõ rệt của viêm miễn dịch, cũng như khi có các biểu hiện toàn thân của bệnh, việc sử dụng corticosteroid được chỉ định. Hiệu quả của việc sử dụng chúng được ghi nhận trong 8 tuần đầu tiên kể từ khi bắt đầu điều trị. Prednisolone được kê đơn theo sơ đồ sau: ở mức cao của đợt cấp, 60 mg mỗi ngày, sau đó giảm dần liều và đến tuần thứ 6-10 được điều chỉnh thành liều duy trì 5-10 mg mỗi ngày. Khi đến tình trạng thuyên giảm lâm sàng, thuốc dần dần bị hủy bỏ. Nếu không thuyên giảm, điều trị bằng prednisolone được tiếp tục trên cơ sở ngoại trú cho đến 52 tuần. Trong quá trình nghiêm trọng của bệnh, trong trường hợp có các biến chứng ở dạng rò rỉ âm đạo, da-ruột, ruột hiện tại, việc bổ nhiệm 6-mercaptopurine uống 0,05 g 2-3 lần một ngày được chỉ định trong các liệu trình 10 ngày với khoảng thời gian 3 ngày cho đến khi thuyên giảm lâm sàng. Sau đó, họ chuyển sang dùng liều duy trì của thuốc trong năm. Liều 6-mercaptopurine trong trường hợp này là 75 mg mỗi ngày. Hiệu quả của việc điều trị bằng thuốc ức chế miễn dịch có thể được xác định không sớm hơn sau 3-4 tháng. Metronidazole được sử dụng rộng rãi trong điều trị bệnh Crohn, với các chỉ định chính là rò và rò quanh hậu môn, thiếu tác dụng của các chế phẩm salazoprep và glucocorticoid, cũng như các đợt tái phát của bệnh sau khi phẫu thuật cắt bỏ. Thuốc được kê đơn với liều 500-1000 mg mỗi ngày. Thời gian của khóa học liên tục không quá 4 tuần. Điều trị triệu chứng của bệnh Crohn được giảm xuống chỉ định các liệu trình ngắn (2-3 ngày mỗi đợt) thuốc chống tiêu chảy (imodium, loperamide). Liều lượng được lựa chọn riêng lẻ tùy theo hiệu quả lâm sàng. Không kê đơn thuốc chống tiêu chảy trong thời gian dài (hơn 5 ngày). Do sự hiện diện của hội chứng kém hấp thu trong bệnh Crohn, các chế phẩm enzym không chứa axit mật (pancreatin, mesimforte, solizim, somilase) được sử dụng với liều lượng từ 2 đến 6 viên trong mỗi bữa ăn. Theo các chỉ định, thiếu máu và giảm albumin máu được điều chỉnh bằng cách kê đơn các chế phẩm sắt (đường tiêm) và quản lý Alvezin, chất thủy phân protein, aminopeptide, aminoblood. Chỉ định vitamin tổng hợp dạng viên, Essentiale dạng viên nang. Điều trị bệnh loạn khuẩn được thực hiện theo các quy tắc chung. Dự báo và phòng ngừa. Với bệnh Crohn, tiên lượng cuộc sống nếu được chẩn đoán kịp thời và theo dõi hiệu quả là thuận lợi, nhưng đối với công việc thì không chắc chắn. Ở những bệnh nhân mắc bệnh nặng, có biến chứng và biểu hiện toàn thân, nhóm khuyết tật I hoặc II được xác định. Bệnh Crohn là một bệnh tiền ung thư. Bệnh nhân cần được làm quen chi tiết với các đặc điểm của diễn biến bệnh và được cảnh báo về các biến chứng có thể xảy ra, mô tả các biểu hiện lâm sàng của chúng ở dạng dễ tiếp cận. BÀI GIẢNG SỐ 14. Các bệnh về đường tiêu hóa. Các bệnh về đại tràng. Viêm loét đại tràng không đặc hiệu Viêm loét đại tràng không đặc hiệu là một bệnh viêm ảnh hưởng đến màng nhầy của đại tràng với những thay đổi phá hủy loét, có đợt tái phát mãn tính, thường kèm theo sự phát triển của các biến chứng đe dọa tính mạng. Nguyên nhân và sinh bệnh học. Viêm loét đại tràng không đặc hiệu là một bệnh vô căn. Những lý do cho sự xuất hiện của nó không được biết đến. Trong số rất nhiều lý thuyết giải thích nguồn gốc của bệnh (nhiễm trùng, do enzym, dị ứng, miễn dịch, thần kinh, v.v.), lý thuyết lây nhiễm được quan tâm nhiều nhất, nhưng những nỗ lực để cô lập mầm bệnh từ các chất chứa trong ruột kết đã không thành công. Quá trình bệnh lý trong viêm loét đại tràng mãn tính bắt đầu từ trực tràng và lan rộng theo hướng gần, chiếm các phần bên trên của đại tràng. Tình trạng viêm có thể giới hạn ở trực tràng (viêm đại tràng), trực tràng và đại tràng xích ma (viêm đại tràng), lan ra toàn bộ phần bên trái (viêm đại tràng trái), hoặc ảnh hưởng đến toàn bộ đại tràng (viêm đại tràng toàn bộ). Về chức năng, chiều dài của đại tràng trong viêm đại tràng không đặc hiệu giảm đi khoảng 1/3. Trong nghiên cứu tài liệu bệnh lý cho thấy viêm lan tỏa của màng nhầy của đại tràng (phù nề rõ rệt và màng phổi, dày lên của các nếp gấp). Các vết loét với nhiều kích thước khác nhau được hình thành trong niêm mạc, có hình dạng không đều, đáy nằm trong niêm mạc, ít gặp hơn ở lớp dưới niêm mạc, trong cơ và niêm mạc. Về mặt hình thái, trong thời kỳ đầu, người ta xác định được thâm nhiễm ở lớp đệm của màng nhầy, bao gồm các tế bào lympho với sự kết hợp của bạch cầu đa nhân, sự giãn nở của các mạch máu và sưng nội mô của các mạch này. Vi phạm vi tuần hoàn đi kèm với sự phát triển của tình trạng thiếu oxy, làm trầm trọng thêm các vi phạm cấu trúc và chức năng của biểu mô niêm mạc. Giai đoạn biểu hiện lâm sàng rõ rệt đi kèm với sự thâm nhập bạch cầu của lớp bề mặt của biểu mô, sự phát triển của viêm màng túi, trong đó sự tích tụ của bạch cầu trung tính xảy ra trong lòng của các màng ngăn. Các phần xa của mật mã bị biến mất, áp xe hầm lò xuất hiện, trong đó sự hình thành của nó có vai trò quan trọng là do sự trưởng thành suy giảm của các tế bào biểu mô. Với sự hoại tử của biểu mô lót bên trong miệng túi, áp xe hầm hố mở ra, hình thành các vết loét. Trong thời gian thuyên giảm, màng nhầy được phục hồi, nhưng tình trạng teo, biến dạng của các crypts và sự dày lên không đồng đều của lớp đệm vẫn còn. Phân loại (Yu. V. Baltaitis và cộng sự, 1986). Đặc điểm lâm sàng. 1. Thể lâm sàng: 1) cấp tính; 2) mãn tính. 2. Hiện tại: 1) tiến triển nhanh chóng; 2) liên tục tái phát; 3) tái diễn; 4) tiềm ẩn. 3. Mức độ hoạt động: 1) đợt cấp; 2) đợt cấp mờ dần; 3) thuyên giảm. 4. Mức độ nghiêm trọng: 1) ánh sáng; 2) vừa phải; 3) nặng. Đặc điểm giải phẫu. 1. Đặc tính vĩ mô: 1) proctitis: 2) viêm tuyến tiền liệt (proctosigmoiditis); 3) tổn thương tổng phụ; 4) thất bại toàn diện. 2. Đặc tính hiển vi: 1) ưu thế của các quá trình viêm phá hủy; 2) giảm các quá trình viêm với các yếu tố phục hồi; 3) hậu quả của quá trình viêm. 1. Địa phương: 1) chảy máu ruột; 2) thủng ruột kết; 3) hẹp đại tràng; 4) bệnh giả tạo; 5) nhiễm trùng ruột thứ phát; 6) sự biến mất của màng nhầy; 7) sự giãn nở độc hại của ruột kết; 8) bệnh ác tính. 2. Tổng quát: 1) chứng đạo đức giả chức năng; 2) nhiễm trùng huyết; 3) biểu hiện toàn thân - viêm khớp, viêm xương cùng, tổn thương da, viêm mống mắt, amyloidosis, viêm tĩnh mạch, viêm đường mật xơ cứng, loạn dưỡng gan. Ảnh lâm sàng. Hình ảnh lâm sàng của viêm loét đại tràng rất đa hình và phụ thuộc vào mức độ nghiêm trọng của diễn biến và mức độ nghiêm trọng của quá trình. Quá trình viêm, thường được coi là mãn tính, trong một số trường hợp trở nên cấp tính. Mức độ tổn thương ở ruột kết cũng có thể khác nhau. Viêm loét đại tràng không đặc hiệu được đặc trưng bởi 3 triệu chứng chính: chảy máu đỏ tươi khi đi tiêu, rối loạn chức năng đường ruột và đau bụng. Phân lập máu (từ các vệt trên bề mặt phân đến 300 ml hoặc hơn) khi đi đại tiện là dấu hiệu đầu tiên của bệnh. Ở thể cấp tính của bệnh, máu được tiết ra theo tia nước, dẫn đến giảm huyết áp dẫn đến suy sụp và sốc xuất huyết. Rối loạn chức năng đường ruột biểu hiện dưới dạng phàn nàn về tình trạng phân không ổn định lặp đi lặp lại, đó là kết quả của việc màng nhầy bị tổn thương nhiều và giảm khả năng hấp thụ nước và muối. Thông thường, tiêu chảy xảy ra khi bị viêm loét đại tràng nặng. Tuy nhiên, tiêu chảy không phải là một chỉ số đáng tin cậy về mức độ nghiêm trọng của quá trình. Mức độ nghiêm trọng của tiêu chảy kết hợp với sự hiện diện của máu đỏ trong phân là vấn đề. Ở một số lượng đáng kể bệnh nhân bị viêm loét đại tràng, định kỳ xuất hiện máu và chất nhầy trên bề mặt phân, thường bị nhầm lẫn là biểu hiện của bệnh trĩ. Bệnh nhân phàn nàn về cơn đau ở bụng dưới với tính chất đau quặn hoặc dai dẳng, thường khu trú ở vùng hạ vị hoặc vùng chậu trái, tăng trước khi đại tiện và biến mất sau đó. Tenesmus thường được ghi nhận. Khi các lớp dưới niêm mạc, cơ và thanh mạc của ruột tham gia vào quá trình này, cơn đau sẽ tăng lên; sờ bụng thấy có sự phòng thủ của các cơ thành bụng trước. Diễn biến nhẹ của viêm loét đại tràng không đặc hiệu được đặc trưng bởi tình trạng bệnh nhân đạt yêu cầu. Đau ở bụng vừa phải và ngắn hạn. Ghế được trang trí, tăng tốc, lên đến 2-3 lần trong ngày. Máu và chất nhầy được tìm thấy trong phân. Quá trình này được bản địa hóa trong trực tràng và đại tràng sigma. Diễn biến lâm sàng tái phát. Hiệu quả của việc điều trị với các chế phẩm salazoprep là đạt yêu cầu. Tái phát xảy ra không quá 2 lần một năm. Các đợt bồi thường có thể kéo dài (hơn 2-3 năm). Diễn biến trung bình của bệnh được chẩn đoán nếu bệnh nhân bị tiêu chảy. Ghế thường xuyên (lên đến 6-8 lần một ngày), trong mỗi phần có thể nhìn thấy một hỗn hợp máu và chất nhầy. Các cơn đau quặn ở bụng dữ dội hơn. Có những cơn sốt không liên tục với sự gia tăng nhiệt độ cơ thể lên đến 38 ° C, suy nhược toàn thân dữ dội. Cũng có thể có các biểu hiện ngoài đường tiêu hóa của bệnh (viêm khớp, viêm màng bồ đào, ban đỏ nốt sần). Quá trình này liên tục tái phát, tác dụng của các chế phẩm salazop không ổn định, nội tiết tố được kê đơn trong đợt cấp. Dạng nặng của bệnh được đặc trưng bởi sự khởi phát cấp tính. Một tổn thương toàn bộ của ruột già phát triển nhanh chóng với sự lan rộng của quá trình bệnh lý sâu vào thành ruột. Tình trạng bệnh nhân xấu đi rõ rệt. Đặc điểm của phòng khám là bệnh nhân khởi phát đột ngột, sốt cao, tiêu chảy nhiều lần lên đến 24 lần một ngày, chảy máu nhiều đường ruột và tăng nhanh tình trạng mất nước. Nhịp tim nhanh xuất hiện, huyết áp giảm, các biểu hiện ngoài tiêu hóa của viêm loét đại tràng không đặc hiệu tăng lên. Điều trị thận trọng không phải lúc nào cũng hiệu quả và thường phải phẫu thuật khẩn cấp. Chẩn đoán và chẩn đoán phân biệt. Trong các xét nghiệm máu lâm sàng ở dạng nhẹ của bệnh, tăng bạch cầu trung tính nhẹ, tăng ESR và số lượng hồng cầu không thay đổi. Khi mức độ nghiêm trọng của bệnh tăng lên và thời gian của đợt trầm trọng tăng lên, thiếu máu có nguồn gốc hỗn hợp xảy ra (B12thiếu và thiếu sắt), tăng ESR. Trong phân tích sinh hóa máu ở các dạng vừa và nặng, chứng rối loạn protein máu, giảm albumin máu, tăng glucaglobulin máu, mất cân bằng điện giải và trạng thái axit-bazơ được ghi nhận. Trong phân tích chung về nước tiểu, những thay đổi chỉ xuất hiện khi các biến chứng phát sinh dưới dạng hội chứng thận hư dựa trên nền tảng của bệnh amyloidosis, khi các thay đổi đặc trưng trong xét nghiệm nước tiểu được ghi nhận - protein niệu, cặn nước tiểu "chết", đồng thời có sự gia tăng trong máu. và mức độ creatinine, urê. Vai trò chính trong chẩn đoán được thực hiện bằng kiểm tra nội soi với sinh thiết đích, vì trong viêm loét đại tràng không đặc hiệu, niêm mạc đại tràng bị ảnh hưởng chủ yếu. Trực tràng luôn tham gia vào quá trình bệnh lý, tức là những thay đổi ăn mòn và loét được phát hiện trong quá trình nội soi ngay phía sau cơ thắt hậu môn trong quá trình nội soi đại tràng sigma. Trong bệnh viêm loét đại tràng, không phải lúc nào cũng có thể khắc phục được đoạn uốn cong trực tràng do tình trạng co thắt nghiêm trọng. Nỗ lực giữ ống soi sẽ kèm theo cơn đau dữ dội. Trong tình huống này, ống soi nên được đưa vào độ sâu không quá 12-15 cm. Nội soi đại tràng trong đợt cấp nặng của viêm loét đại tràng không đặc hiệu là không an toàn để thực hiện. Nó nên được sử dụng có nguy cơ ác tính cao. Cần lưu ý rằng nội dung thông tin cao của nội soi sigmoidoscopy. Hình ảnh nội soi phụ thuộc vào dạng bệnh. Ở thể nhẹ, có thể nhìn thấy màng nhầy phù nề, lớp nhầy màu trắng dày trên thành ruột và có thể nhìn thấy chảy máu khi tiếp xúc nhẹ. Hình thái mạch máu của lớp dưới niêm mạc không được xác định bằng mắt thường. Với một đợt bệnh vừa phải, xung huyết và phù nề niêm mạc, chảy máu do tiếp xúc nghiêm trọng, xuất huyết, ăn mòn và loét có hình dạng bất thường, lớp chất nhầy dày trên thành ruột được tiết lộ. Trong một giai đoạn nặng của bệnh, màng nhầy của đại tràng bị phá hủy trên một mức độ đáng kể. Bề mặt bên trong có dạng hạt, chảy máu, các vùng loét rộng với cặn xơ, các ổ giả có kích thước và hình dạng khác nhau, mủ và máu trong lòng ruột được tìm thấy. Chống chỉ định nội soi đại tràng và soi đại tràng sigma là những dạng viêm loét đại tràng nặng ở giai đoạn cấp tính của bệnh. Kiểm tra bằng tia X cho phép bạn xác định mức độ tổn thương; làm rõ chẩn đoán trong trường hợp dữ liệu nội soi không đủ thuyết phục; chẩn đoán phân biệt với bệnh Crohn, bệnh túi thừa, viêm đại tràng do thiếu máu cục bộ; phát hiện kịp thời các dấu hiệu ác tính. X quang thường có thể cho thấy ruột ngắn lại, thiếu hơi, giãn độc, khí tự do dưới vòm hoành trong quá trình thủng. Soi cầu thận phải được thực hiện hết sức cẩn thận. Nó có thể gây ra tình trạng xấu đi của bệnh nhân. Trong một số trường hợp, việc chuẩn bị cho bệnh nhân thụt bari với thuốc xổ và thuốc nhuận tràng phải được thay thế bằng một chế độ ăn uống đặc biệt được chỉ định 2 ngày trước khi nghiên cứu. Trong một số trường hợp, việc sử dụng thuốc cản quang có thể đẩy nhanh quá trình thủng hoặc gây giãn đại tràng độc hại. Do đó, soi tưới tiêu được thực hiện sau khi lún các hiện tượng cấp tính. Phương pháp này cho thấy sự không đồng đều và "sần sùi" của niêm mạc, thành ruột dày lên, loét, tạo mủ, thiếu máu. Chẩn đoán phân biệt viêm loét đại tràng không đặc hiệu được thực hiện chủ yếu với nhiễm trùng đường ruột cấp tính. Khi có dịch nhiễm trùng đường ruột, chẩn đoán dễ dàng được xác định. Nhưng ngay cả trong trường hợp bệnh xuất hiện lẻ tẻ trong nhiễm trùng đường ruột cấp tính, hội chứng viêm đại tràng chảy máu không tái phát, trong khi viêm loét đại tràng có một đợt tái phát. Các phương pháp chính xác nhất để xác định nhiễm trùng đường ruột cấp tính bao gồm vi khuẩn học và huyết thanh học. Thông thường, viêm loét đại tràng được phân biệt với bệnh Crohn. Trong các trường hợp điển hình, bệnh Crohn khác với viêm đại tràng không đặc hiệu ở chỗ không có tổn thương trực tràng, thường xuyên có sự tham gia của hồi tràng vào quá trình bệnh lý và tổn thương từng đoạn của thành ruột. Chẩn đoán xác định có thể được thực hiện bằng cách phát hiện các u hạt lympho đặc hiệu cho bệnh Crohn trong các mẫu sinh thiết. Với bệnh viêm đại tràng có u hạt, viêm phần phụ và lỗ rò trực tràng được phát hiện thường xuyên hơn so với bệnh viêm loét đại tràng không đặc hiệu. Trong một số trường hợp, cần phân biệt giữa viêm loét đại tràng và bệnh lao ruột. Đối với bệnh lao ruột, một bản địa hóa nhất định của quá trình là đặc trưng (hồi tràng, vùng hồi tràng), tổn thương ruột từng đoạn. Nhưng đôi khi với bệnh lao ruột, trực tràng và toàn bộ ruột già bị ảnh hưởng. Hình ảnh nội soi của bệnh lao ruột được đặc trưng bởi sự hiện diện của các vết loét với các cạnh nổi lên chứa đầy chất màu xám. Các vết loét do lao có xu hướng lan rộng theo chiều ngang và để lại những vết sẹo ngắn trong đó các vết loét xuất hiện trở lại. Với viêm loét đại tràng không đặc hiệu, sẹo không hình thành tại vị trí của vết loét trước đây. Ở những bệnh nhân lớn tuổi và cao tuổi, viêm loét đại tràng cần được phân biệt với viêm đại tràng do thiếu máu cục bộ. Loại thứ hai được đặc trưng bởi cơn đau dữ dội, kịch phát ở vùng bụng 20-30 phút sau khi ăn, trong khi ở bệnh viêm loét đại tràng, cơn đau xuất hiện trước khi đi đại tiện. Dấu hiệu X quang quan trọng nhất là triệu chứng "dấu ngón tay cái". Hình ảnh nội soi của viêm đại tràng do thiếu máu cục bộ được đặc trưng bởi ranh giới rõ ràng của tổn thương, xuất huyết dưới niêm mạc, hình thành giả xanh tím nhô vào lòng ruột. Kiểm tra mô học cho thấy các tế bào chứa hemosiderin và xơ hóa. Việc không có máu do tiếp xúc tại thời điểm sinh thiết cũng là dấu hiệu của viêm đại tràng do thiếu máu cục bộ. Điều trị. Việc không có một yếu tố căn nguyên duy nhất và sự phức tạp trong cơ chế bệnh sinh của viêm loét đại tràng không đặc hiệu khiến việc điều trị căn bệnh này trở nên khó khăn. Các loại thuốc có tác dụng chống viêm, kháng khuẩn được sử dụng: salazopyridazine, sulfasalazine, salazodimethoxin, salofalk. Sulfasalazine dùng đường uống, với sự tham gia của hệ vi sinh đường ruột, phân hủy thành axit 5-aminosalicylic và sulfapyridine. Sulfapyridine không được hấp thu sẽ ức chế sự phát triển của hệ vi sinh vật kỵ khí trong ruột, bao gồm clostridia và vi khuẩn. Và nhờ axit 5-aminosalicylic, thuốc không chỉ gây ra những thay đổi trong hệ vi sinh vật đường ruột mà còn điều chỉnh các phản ứng miễn dịch và ngăn chặn các chất trung gian của quá trình viêm. Thuốc được kê đơn với liều 2-6 g mỗi ngày trong toàn bộ thời gian viêm hoạt động. Khi hội chứng đau bụng giảm bớt, liều sulfasalazine giảm dần, đưa về mức duy trì (trung bình 1-1,5 viên mỗi ngày). Việc chỉ định các dẫn xuất 5-aminosalicylic acid (salofalk, mesacol, salosan, tidikol) là phương pháp cơ bản và có thể được sử dụng như đơn trị liệu cho các dạng viêm loét đại tràng nhẹ và vừa. Việc điều trị được thực hiện dựa trên nền tảng của liệu pháp ăn kiêng, ngoại trừ các sản phẩm từ sữa, với sự hiện diện của hàm lượng cân bằng của protein, chất béo, carbohydrate và vitamin trong chế độ ăn. Nó được khuyến khích để loại trừ trái cây tươi, rau, thực phẩm đóng hộp. Thức ăn nên được chế biến nhẹ nhàng về mặt cơ học và hóa học. Cho ăn chia nhỏ 4-5 lần một ngày. Sự mất cân bằng vitamin làm gián đoạn quá trình hấp thụ các nguyên tố vi lượng và được bù đắp bằng việc bổ nhiệm các chế phẩm phức tạp trong máy tính bảng ("Duovit", "Oligovit", "Unicap"). Trong hội chứng tiêu chảy nặng ở những người có đợt bệnh nhẹ và vừa, việc chỉ định sandostatin được chỉ định, thuốc này ức chế sự tổng hợp các hormone đường tiêu hóa và các amin sinh học (peptide hoạt động trong ruột, gastrin, serotonin), việc sản xuất chúng tăng mạnh trong viêm loét đại tràng và bệnh Crohn. Và thuốc cũng làm giảm sự bài tiết và cải thiện sự hấp thu ở ruột, ức chế lưu lượng máu nội tạng và giảm nhu động. Khi sử dụng sandostatin (trong vòng 7 ngày với liều 0,1 mg x 2 lần, tiêm dưới da), tiêu chảy giảm, chứng đi ngoài thực tế biến mất, và bài tiết máu theo phân giảm. Trong một dạng nặng của viêm loét đại tràng không đặc hiệu, điều trị được thực hiện dựa trên nền tảng của dinh dưỡng ngoài đường tiêu hóa. Hàm lượng protein của các chế phẩm này phải xấp xỉ 1,5-2,0 g / kg trọng lượng cơ thể. Corticosteroid, được sử dụng qua đường tiêm, là một phương pháp điều trị bệnh sinh cho một dạng bệnh nặng: trong ngày đầu tiên, prednisone được tiêm tĩnh mạch cách nhau 12 giờ (90-120 mg hoặc hơn), trong 5 ngày tiếp theo - tiêm bắp, giảm dần liều lượng. Với hiệu quả tích cực, họ chuyển sang thuốc uống (prednisolone 40 mg mỗi ngày). Không nên sử dụng lâu dài các hormone trong thời gian thuyên giảm ổn định. Ở những bệnh nhân có một đợt bệnh nặng, một tác dụng tích cực của quá trình oxy hóa tăng cao (HBO) đã được ghi nhận. Việc sử dụng một đợt HBO (7-10 liệu trình) trong thời gian bệnh thuyên giảm có thể làm giảm tần suất tái phát. Chỉ định điều trị ngoại khoa cấp cứu: thủng ruột, dãn ruột nhiễm độc, chảy máu ruột nhiều, bệnh lý ác tính. Ở dạng vừa của đợt loét loét không đặc hiệu, cần có một chế độ ăn kiêng nghiêm ngặt với việc hạn chế chất xơ, các sản phẩm từ sữa và hàm lượng protein cao. Prednisolone được kê đơn bằng đường uống với liều khởi đầu 20-40 mg mỗi ngày. Việc điều trị có thể được bổ sung bằng sulfasalazine và các chất tương tự của nó, được dùng bằng đường uống hoặc tiêm dưới dạng viên nén siêu nhỏ và thuốc đạn vào trực tràng. Liều khởi đầu của sulfasalazine là 1 g mỗi ngày, sau đó tăng lên 4-6 g. Như một phương pháp điều trị bổ trợ, có thể sử dụng nước sắc của các loại thảo mộc có tác dụng chống viêm và cầm máu (rễ cây bìm bịp, lá tầm ma, địa y, cây mã đề xám, rễ cam thảo), thuốc thảo dược thường cho phép bạn giảm liều lượng thuốc salazoprepression, kéo dài thời gian. thuyên giảm. Dự báo và phòng ngừa. Trong những trường hợp nặng và có các biến chứng toàn thân và cục bộ, tiên lượng rất nghiêm trọng. Người bệnh hoàn toàn không thể làm việc. Ở dạng bệnh nhẹ và trung bình, tiên lượng cuộc sống thuận lợi. Bệnh nhân cần được chuyển sang công việc nhẹ nhàng. Trong thời gian thuyên giảm, khuyến cáo điều trị duy trì bằng các chế phẩm salazoprep, tác nhân vi khuẩn, liệu pháp tâm lý và liệu pháp ăn kiêng. Bệnh nhân bị viêm loét đại tràng không đặc hiệu trong một thời gian dài (trên 5-7 năm) nên được xếp vào nhóm nguy cơ xuất hiện ung thư ruột và đưa vào hồ sơ khám bệnh. Những bệnh nhân này được soi ruột già mỗi năm một lần với sinh thiết mục tiêu. BÀI GIẢNG SỐ 15. Các bệnh về thận. Viêm thận cầu thận cấp Viêm cầu thận cấp (AGN) là một bệnh thận lan tỏa cấp tính có tính chất nhiễm trùng-dị ứng, khu trú ở các cầu thận. AGN có thể là một bệnh độc lập (nguyên phát) hoặc thứ phát như một phần của bệnh khác, làm phức tạp thêm bệnh cảnh lâm sàng và chẩn đoán bệnh sau này. AGN thường ảnh hưởng đến nam giới trẻ và trung niên. Nguyên nhân. AGN xảy ra thường xuyên nhất sau khi bị nhiễm trùng cầu khuẩn (cúm, viêm amidan cấp tính, viêm họng do cái gọi là chủng vi sinh vật gây bệnh thận). Ở 60-80% bệnh nhân, liên cầu tan huyết β nhóm A được phát hiện; 1/3 trường hợp không xác định được căn nguyên của AGN. Hạ thân nhiệt kéo dài, đặc biệt là trong điều kiện độ ẩm cao, góp phần vào sự phát triển của AGN. Tiêm phòng cũng là một yếu tố khiến bệnh khởi phát, 75% trường hợp thận bị ảnh hưởng sau khi tiêm mũi thứ hai hoặc thứ ba. Sinh bệnh học. Cơ chế bệnh sinh của bệnh có cơ chế miễn dịch: khi các kháng nguyên (liên cầu, dược liệu, protein lạ) xâm nhập vào cơ thể, các kháng thể được hình thành để đáp ứng, liên kết các kháng nguyên này và cùng với phần thứ 3 của bổ thể hình thành phức hợp miễn dịch tuần hoàn trong mạch máu. giường. Các phức hợp có khả năng lắng đọng ở mặt ngoài của màng đáy của mao mạch cầu thận, gây tổn thương thông qua việc giải phóng các sản phẩm phân hủy bổ thể, làm tăng tính thấm của mao mạch và gây ra những thay đổi cục bộ sau này. Bạch cầu trung tính lao đến vị trí lắng đọng các phức hợp miễn dịch, các enzyme lysosomal của chúng làm nặng thêm tổn thương ở nội mô và màng đáy, tách chúng ra khỏi nhau. Sự thoái hóa tiểu cầu gây ra sự giải phóng serotonin, dẫn đến đông máu và lắng đọng fibrin trên màng đáy. Việc loại bỏ các phức hợp miễn dịch khỏi cơ thể được tạo điều kiện bởi phản ứng đại thực bào dưới dạng tăng sinh các tế bào trung mô và nội mô, với hiệu quả của quá trình này, sự phục hồi sẽ xảy ra. Ảnh lâm sàng. Hình ảnh lâm sàng của bệnh bao gồm các hội chứng sau. hội chứng tiết niệu. 1. Protein niệu do sự di chuyển của các phân tử protein qua các khoảng trống của thành mao mạch của cầu thận, được hình thành trong quá trình lắng đọng các phức hợp miễn dịch trên chúng. Protein niệu có tính chất chọn lọc, trong đó chủ yếu là các albumin đi qua “bộ lọc” cầu thận. 2. Đái máu do sự tham gia của trung bì mao mạch và mô kẽ vào quá trình bệnh lý. Erythrocytes thâm nhập qua các vết vỡ nhỏ nhất trong màng đáy, thay đổi hình dạng của chúng. 3. Cylindruria - bài tiết nước tiểu của các tế bào hình trụ của ống. Trong quá trình loạn dưỡng trong các ống của các tế bào bị phân hủy của biểu mô thận, hình trụ hạt được hình thành, bao gồm một khối hạt dày đặc; hình trụ sáp có đường viền sắc nét và cấu trúc đồng nhất; phôi hyaline là thành tạo giàu protein. Hội chứng tăng huyết áp được quan sát do: 1) giữ natri và nước; 2) hoạt hóa hệ thống renin-angiotensin-aldosterone và thần kinh giao cảm; 3) giảm chức năng của hệ thống suy giảm của thận. Hội chứng phù nề có liên quan đến các yếu tố sau: 1) giảm độ lọc cầu thận do sự thất bại của chúng; 2) giảm điện tích lọc của natri và tăng tái hấp thu; 3) giữ nước do giữ natri trong cơ thể; 4) sự gia tăng BCC; 5) cường aldosteron thứ phát; 6) tăng tiết ADH và tăng độ nhạy của nephron xa với nó, dẫn đến giữ nước; 7) sự gia tăng tính thấm của thành mao mạch và sự giải phóng huyết tương vào các mô; 8) giảm áp lực huyết tương với protein niệu lớn. Các phàn nàn được trình bày trong AGN không cụ thể và xảy ra ở nhiều bệnh khác nhau. Điều rất quan trọng là chỉ ra trong bệnh án một cơn đau họng gần đây, đợt cấp của viêm amidan mãn tính, hạ thân nhiệt, vv Một số bệnh nhân lưu ý rằng lượng nước tiểu giảm, kết hợp với một số sưng (nhão) mặt vào buổi sáng. Ở 1 / 3-3 / 4 bệnh nhân trong những ngày đầu tiên của bệnh, có những cơn đau nhức, không mạnh ở vùng thắt lưng kết hợp với sự gia tăng kích thước của thận. Ngoài ra còn có tăng mệt mỏi, nhức đầu, khó thở khi gắng sức, nhiệt độ cơ thể tăng trong thời gian ngắn đến mức thấp. Tăng huyết áp động mạch, chỉ được phát hiện ở một nửa số bệnh nhân, được đặc trưng bởi sự gia tăng số lượng lên 140-160 / 85-90 mm Hg. Mỹ thuật. (hiếm khi - lên đến 180/100 mm Hg. Điều.). Chẩn đoán. Trong 100% trường hợp, xét nghiệm nước tiểu cho thấy protein niệu có mức độ nghiêm trọng khác nhau, trụ niệu và điều quan trọng nhất để chẩn đoán là tiểu máu với mức độ nghiêm trọng khác nhau - từ tiểu máu vi thể (lên đến 10 tế bào hồng cầu trong trường quan sát) đến tiểu máu đại thể (mặc dù khá hiếm). ). Tuy nhiên, nếu nghi ngờ AGN, cần phải tiến hành một loạt xét nghiệm nước tiểu lặp đi lặp lại hoặc thực hiện xét nghiệm Nechiporenko (xác định số lượng thành phần được hình thành trong 1 μl), vì hồng cầu có thể không được phát hiện trong một phần nước tiểu. Khi kiểm tra máu, các chỉ số giai đoạn cấp tính được phát hiện (tăng hàm lượng fibrinogen và α2-globulin, protein phản ứng C, tăng tốc ESR), số lượng bạch cầu ít thay đổi, thiếu máu trung bình. Với một đợt điều trị AGN không biến chứng, hàm lượng các chất đạm (creatinin, indican, urê) trong máu không thay đổi. Trong giai đoạn đầu của bệnh, xét nghiệm Reberg có sự thay đổi - giảm mức lọc cầu thận và tăng tái hấp thu ở ống thận, sẽ bình thường hóa khi nó hồi phục. Kiểm tra X quang ở bệnh nhân tăng huyết áp động mạch nặng có thể thấy tâm thất trái tăng vừa phải, có kích thước tương đương khi bệnh nhân hồi phục. Có 3 biến thể lâm sàng của AGN. 1) Biến thể không có triệu chứng: phàn nàn nhỏ, không có phù và tăng huyết áp động mạch, chỉ có hội chứng tiết niệu; biến thể phổ biến nhất của quá trình bệnh (86% trường hợp). 2) Biến thể thận hư: phù, thiểu niệu rõ rệt, có thể làm tăng huyết áp đến con số tương đối thấp, nó được phát hiện ở 8% bệnh nhân. 3) Phiên bản mở rộng: tăng huyết áp động mạch, đạt số lượng cao (180/100 mm Hg), phù rõ rệt vừa phải, suy tuần hoàn, xảy ra trong 6% trường hợp. Chẩn đoán phân biệt. AGN phải được phân biệt với viêm cầu thận mãn tính, bệnh này không khó khăn khi AGN khởi phát cấp tính và sau đó các triệu chứng sẽ biến mất hoàn toàn. Tuy nhiên, trong trường hợp không có khởi phát cấp tính cũng như sự tồn tại lâu dài của một số dấu hiệu bệnh, việc chẩn đoán trở nên phức tạp hơn nhiều. Nếu khó phân biệt, chọc dò sinh thiết thận sẽ được sử dụng. Rất khó phân biệt AGN với viêm bể thận do sự hiện diện của bạch cầu niệu trong cả hai bệnh. Tuy nhiên, AGN đi kèm với protein niệu nhiều hơn và trong một số trường hợp, phù nề. Chẩn đoán phân biệt cũng được giúp đỡ bởi các triệu chứng lâm sàng của viêm bể thận dưới dạng đau rõ rệt hơn ở lưng dưới, kèm theo sốt và rối loạn khó tiêu. Cũng có giá trị chẩn đoán là định nghĩa vi khuẩn niệu trong viêm bể thận, xác định bạch cầu "hoạt động", cũng như các nghiên cứu chụp x-quang (biến dạng của cốc) và đồng vị-cải tạo (sự bất đối xứng của chức năng thận). AGN với tư cách là một bệnh độc lập phải được phân biệt với các bệnh mô liên kết lan tỏa mạn tính, trong đó AGN là một trong những biểu hiện của bệnh. Tình trạng này thường xảy ra với mức độ nghiêm trọng của các hội chứng tiết niệu, tăng huyết áp và phù nề và không rõ ràng các triệu chứng khác của bệnh, thường xảy ra với SLE (lupus ban đỏ hệ thống). Chẩn đoán chính xác trong SLE có thể được thực hiện bằng cách tính đến hội chứng khớp, tổn thương da và các cơ quan khác (tim), những thay đổi rõ rệt về miễn dịch (phát hiện kháng thể chống tổ chức ở hiệu giá cao, tế bào lupus ban đỏ, kháng thể với DNA và RNA ), cũng như theo dõi động thái của bệnh cảnh lâm sàng. Điều trị. Điều trị AGN rất phức tạp và bao gồm các biện pháp sau. 1. Chế độ. Nếu nghi ngờ AGN hoặc ngay sau khi chẩn đoán được xác lập, bệnh nhân cần được nhập viện ngay lập tức. Nghỉ ngơi tại giường nghiêm ngặt phải được theo dõi trong khoảng 2-4 tuần cho đến khi loại bỏ phù và huyết áp bình thường. Nằm trên giường giúp cơ thể ấm lên đồng đều, dẫn đến giảm co thắt mạch (do đó, giảm huyết áp), tăng lọc cầu thận và bài niệu. Sau khi xuất viện, điều trị tại nhà được chỉ định trong tối đa 4 tháng kể từ ngày bệnh khởi phát, là biện pháp ngăn ngừa tốt nhất sự chuyển AGN sang giai đoạn mãn tính. 2. Chế độ ăn uống. Tùy thuộc vào mức độ nghiêm trọng của các triệu chứng lâm sàng, điều rất quan trọng là hạn chế chất lỏng và natri clorua. Với dạng giãn nở và thận hư, nên nhịn ăn hoàn toàn trong 1-2 ngày với lượng chất lỏng tương đương với bài niệu. Vào ngày thứ 2-3, cho thấy việc tiêu thụ thức ăn giàu muối kali (cháo gạo, khoai tây). Tổng lượng nước uống mỗi ngày phải bằng lượng nước tiểu được phân bổ cho ngày hôm trước cộng với 300-500 ml. Sau 3-4 ngày, bệnh nhân được chuyển sang chế độ ăn hạn chế đạm (tối đa 60 g mỗi ngày), và tổng lượng muối không quá 3-5 g / ngày. Chế độ ăn kiêng như vậy được khuyến nghị cho đến khi biến mất tất cả các triệu chứng ngoại cảm và cải thiện đáng kể lượng cặn trong nước tiểu. 3. Điều trị bằng thuốc bao gồm, trước hết, liệu pháp kháng khuẩn, tuy nhiên, chỉ nên được thực hiện nếu tính chất lây nhiễm của AGN được thiết lập một cách đáng tin cậy (mầm bệnh đã được phân lập và không quá 3 tuần kể từ khi bắt đầu dịch bệnh). Penicillin thường được kê đơn hoặc các chất tương tự bán tổng hợp của nó ở liều lượng thông thường. Sự hiện diện của các ổ nhiễm trùng mãn tính rõ ràng (viêm amiđan, viêm xoang, v.v.) cũng là một chỉ định trực tiếp cho liệu pháp kháng sinh. Thuốc lợi tiểu trong điều trị AGN chỉ được chỉ định khi giữ nước, tăng huyết áp và xuất hiện suy tim. Furosemide hiệu quả nhất (40-80 mg), được sử dụng cho đến khi loại bỏ phù và tăng huyết áp. Các loại thuốc này không cần kê đơn lâu dài, 3-4 liều là đủ. Trong trường hợp không bị phù, nhưng tăng huyết áp dai dẳng hoặc không đủ tác dụng hạ huyết áp của thuốc lợi tiểu, thuốc hạ huyết áp (clophelin, dopegyt) được kê đơn với thời gian dùng thuốc phụ thuộc vào sự kéo dài của tăng huyết áp động mạch. Ở dạng thận hư của AGN, liệu pháp ức chế miễn dịch được kê đơn (corticosteroid - prednisone 60-120 mg mỗi ngày, sau đó giảm dần liều lượng, thời gian sử dụng trong 4-8 tuần). Trong trường hợp AGN bị phù nặng và giảm bài niệu đáng kể, heparin được dùng với liều 20-000 IU mỗi ngày trong 30-000 tuần, giúp tăng thời gian đông máu lên 4-6 lần. Với protein niệu kéo dài, indomethacin hoặc voltaren được kê đơn với liều 75-150 mg mỗi ngày (trong trường hợp không tăng huyết áp và thiểu niệu). Tiên lượng là thuận lợi, tuy nhiên, với các hình thức kéo dài, có khả năng quá trình sẽ trở thành mãn tính. Phòng ngừa AGN đi xuống để điều trị hiệu quả nhiễm trùng khu trú, làm cứng hợp lý. Để phát hiện kịp thời giai đoạn khởi phát của bệnh sau khi tiêm vắc xin, SARS chuyển giao ở tất cả các bệnh nhân, cần phải xét nghiệm nước tiểu. BÀI GIẢNG SỐ 16. Các bệnh về thận. Viêm bể thận Viêm đài bể thận là một bệnh truyền nhiễm trong đó đài bể thận, đài và chất của thận tham gia vào quá trình này, với tổn thương chủ yếu là mô kẽ. Về vấn đề này, viêm thận bể thận là viêm thận mô kẽ (kẽ). Đây là một khái niệm rộng hơn so với viêm bể thận. Trước hết, nó biểu thị một loại viêm thận do bất kỳ nguyên nhân nào có liên quan chủ yếu đến kẽ thận, và thứ hai, là một căn bệnh đặc biệt mà tình trạng viêm này là biểu hiện chính và duy nhất của nó. Gần với viêm thận kẽ là cái gọi là viêm thận kẽ tubulo, trong đó có một tổn thương thân thiện của các ống và mô đệm của thận. Phân loại. Dựa trên dữ liệu lâm sàng và hình thái, viêm bể thận cấp tính và mãn tính được phân biệt, thường có diễn biến tái phát dưới dạng các đợt tấn công của viêm bể thận cấp tính. Ngoài ra, viêm bể thận có thể là một và hai mặt. Theo dạng diễn biến (đối với viêm bể thận mạn): dạng tái phát, viêm bể thận mạn tính tiềm ẩn, đài bể thận nhăn nheo. Nguyên nhân và sinh bệnh học. Viêm bể thận là một bệnh truyền nhiễm. Tác nhân gây bệnh của nó là các tác nhân lây nhiễm có tính chất không đặc hiệu: E. coli, enterococcus, staphylococcus và các vi khuẩn khác, nhưng trong hầu hết các trường hợp, chúng ta đang nói về E. coli (40%) và hệ thực vật hỗn hợp (38%). Sự chú ý được tập trung vào các dạng L của vi khuẩn, nguyên sinh chất (cơ thể của vi khuẩn, không có màng có thể hỗ trợ nhiễm trùng), nấm candida, có thể gây viêm bể thận mãn tính. Nguồn lây nhiễm có thể là amiđan, các bệnh của cơ quan sinh dục và ruột già, tức là các tác nhân truyền nhiễm có thể xâm nhập vào thận, bao gồm cả khung chậu, theo dòng máu (viêm bể thận giảm dần theo huyết thống), được quan sát thấy trong nhiều bệnh truyền nhiễm (sốt thương hàn, cúm , đau thắt ngực, nhiễm trùng huyết). Thông thường hơn, vi khuẩn được đưa vào thận theo cách tăng dần từ niệu quản, bàng quang, niệu đạo (viêm bể thận tăng tiết niệu), được tạo điều kiện bởi rối loạn vận động của niệu quản và khung chậu, tăng áp lực nội chậu (trào ngược lỗ tiểu và tiểu khung), cũng như tái hấp thu các chất trong bể thận vào các tĩnh mạch của tủy thận (hồi lưu pyelovenous). Theo quy luật, viêm bể thận tăng dần sẽ làm biến chứng các bệnh của hệ thống sinh dục, trong đó nước tiểu khó chảy ra ngoài (sỏi và hẹp niệu quản, hẹp niệu đạo, các khối u của hệ sinh dục), do đó nó thường phát triển trong thời kỳ mang thai. Nhiễm trùng bạch huyết ở thận (viêm bể thận sinh bạch huyết) cũng có thể xảy ra, khi đại tràng và cơ quan sinh dục là nguồn lây nhiễm. Đối với sự phát triển của viêm bể thận, ngoài sự xâm nhập của nhiễm trùng vào thận, phản ứng của cơ thể và một số nguyên nhân tại chỗ gây ra sự vi phạm dòng nước tiểu và ứ đọng nước tiểu là rất quan trọng. Những lý do tương tự giải thích khả năng tái phát một đợt mãn tính của bệnh. Các vi sinh vật bị nhiễm với những thay đổi về chức năng và hình thái trong đường tiết niệu dẫn đến ứ đọng nước tiểu, suy giảm dòng chảy của tĩnh mạch và bạch huyết từ thận, góp phần cố định nhiễm trùng ở thận, gây ra các vùng thâm nhiễm viêm khu trú và đa hình và chèn ép các kẽ của một hoặc cả hai thận. Mô kẽ của các ống bị ảnh hưởng, và sau đó là các nephron. Có viêm nội mạc sinh sản, tăng sản lớp vỏ giữa của mạch, hiện tượng nhiễm mặn, xơ vữa động mạch phát triển đến thận thứ phát nhăn nheo. Trong những năm gần đây, một vai trò nhất định trong sự phát triển của viêm thận bể thận mãn tính được gán cho các phản ứng tự miễn dịch: dưới ảnh hưởng của kháng nguyên vi khuẩn, immunoglobulin G và bổ thể được lắng đọng trên màng đáy của mao mạch cầu thận, gây ra tổn thương cho nó. Sự chuyển đổi của viêm thận bể thận cấp tính sang mãn tính được tạo điều kiện thuận lợi bởi: chẩn đoán muộn màng thận cấp tính, nhập viện không kịp thời, sự hiện diện của nhiễm trùng mãn tính, đái tháo đường, bệnh gút và lạm dụng thuốc giảm đau - phenacetin. Viêm thận bể thận mãn tính phổ biến hơn ở phụ nữ (50%), được tạo điều kiện thuận lợi cho việc mang thai, đặc biệt là những lần mang thai lặp đi lặp lại (estrogen gây mất trương lực cơ trơn của đường tiết niệu), ở trẻ em gái, có liên quan đến cấu trúc của đường tiết niệu. , sự bất thường của chúng. Ảnh lâm sàng. Như đã đề cập ở trên, cả bệnh viêm bể thận cấp tính và mãn tính đều có thể xảy ra. Hình ảnh lâm sàng của giai đoạn cấp tính của bệnh được đặc trưng bởi nhiệt độ cơ thể tăng đột ngột, mạnh lên đến 39-40 ° C, khởi đầu suy nhược, nhức đầu, ớn lạnh, kết hợp với đổ mồ hôi nhiều, buồn nôn và nôn. Cùng với sự gia tăng nhiệt độ cơ thể, các cơn đau xuất hiện ở vùng thắt lưng, theo quy luật, được ghi nhận ở một bên. Tính chất cơn đau âm ỉ, cường độ của chúng khác nhau. Trong trường hợp sự phát triển của bệnh trên nền sỏi niệu, một cuộc tấn công của viêm thận bể thận là một cuộc tấn công của cơn đau quặn thận. Trong trường hợp không được điều trị đầy đủ, bệnh có thể trở thành mãn tính hoặc điều này dẫn đến sự phát triển của các quá trình hỗ trợ trong thận, biểu hiện lâm sàng bằng sự suy giảm tình trạng chung của bệnh nhân và thay đổi nhiệt độ đột ngột (từ 35-36 ° C vào buổi sáng đến 40-41 ° C vào buổi tối). Về nguyên tắc, viêm thận bể thận mãn tính là hậu quả của viêm bể thận cấp tính được điều trị, khi có thể loại bỏ tình trạng viêm cấp tính, nhưng không thể tiêu diệt triệt để tất cả các mầm bệnh trong thận, cũng như không thể khôi phục lại dòng chảy sinh lý của nước tiểu từ thận. Viêm thận mãn tính gây lo lắng về những cơn đau âm ỉ liên tục ở vùng thắt lưng, trầm trọng hơn khi thời tiết lạnh ẩm. Ngoài ra, viêm thận bể thận mãn tính dễ bị đợt cấp định kỳ, khi bệnh nhân có tất cả các dấu hiệu của một quá trình cấp tính. Chẩn đoán. Vấn đề chẩn đoán bệnh là do các triệu chứng của viêm bể thận giống với triệu chứng của các bệnh khác do viêm đường tiết niệu. Kế hoạch kiểm tra chẩn đoán bao gồm xét nghiệm máu, xét nghiệm nước tiểu, cũng như các nghiên cứu cho thấy tình trạng của hệ tiết niệu: siêu âm thận, nghiên cứu X-quang, phân tích PCR để tìm tác nhân lây nhiễm. Để xác minh loại tác nhân lây nhiễm, cần phải tiến hành nuôi cấy vi khuẩn của một mẫu nước tiểu và phương pháp chụp cắt lớp vi tính được sử dụng để loại trừ các quá trình của khối u. Vì vậy, phòng thí nghiệm và các phương pháp nghiên cứu đặc biệt có tầm quan trọng lớn đối với việc nhận biết bệnh. Và trong viêm thận bể thận mãn tính, biểu hiện quyết định và đôi khi chỉ là những thay đổi trong nước tiểu, máu và đường tiết niệu. Cần theo dõi động huyết áp và cân nặng của bệnh nhân. Tăng bạch cầu, tăng ESR, dịch chuyển bạch cầu trung tính được ghi nhận trong máu, tăng mức nitơ dư (ở mức 20-40 mg), urê (mức 40-60 mg), creatinine (mức 53-106 μmol / l ), indican (định mức 1,41, 3,76-180 µmol / l), cholesterol (định mức 200-83 mg), clorua máu (định mức XNUMX mmol / l). Quan trọng đối với việc chẩn đoán những thay đổi trong nước tiểu: giảm trọng lượng riêng, protein niệu (kể cả hàng ngày), tiểu máu và tiểu cầu. Tuy nhiên, các phương pháp xác định định lượng các thành phần hình thành trong trầm tích nước tiểu đang ngày càng có tầm quan trọng chẩn đoán: Kakovsky-Addis (bạch cầu bình thường lên tới 4 triệu; hồng cầu - lên tới 1 triệu, hình trụ - lên tới 2 nghìn trong 24 giờ), Amburger (bạch cầu bình thường lên đến 2000 , hồng cầu - lên tới 1400, phôi - lên tới 20 mỗi 1 phút), Nechiporenko (bạch cầu bình thường lên tới 2500, hồng cầu - lên tới 1000, phôi - lên tới 20 trong 1 ml nước tiểu mới thải ra). Tỷ lệ giữa số lượng tuyệt đối của hồng cầu và bạch cầu trong cặn lắng nước tiểu trong viêm thận bể thận thay đổi đột ngột theo hướng chiếm ưu thế đáng kể của bạch cầu gấp 10 - 20 lần. Trong viêm thận bể thận mãn tính, tế bào Stenheimer-Malbin xuất hiện trong nước tiểu: bạch cầu lớn, với chuyển động màu nâu của các hạt tế bào chất, xuất hiện với sự giảm tính chất thẩm thấu của nước tiểu (trọng lượng riêng dưới 10-14), nhuộm màu xanh lam với tím gentian và safronin, bạch cầu "hoạt động": bạch cầu bị thay đổi, có chuyển động Brown của nguyên sinh chất, được bộc lộ khi nhuộm bằng dung dịch nước 1% xanh methylen có thêm nước cất. Giá trị chẩn đoán của sự gia tăng số lượng bạch cầu "hoạt động" và tế bào Stenheimer-Malbin (lên đến 40%), vi khuẩn niệu (số lượng vi sinh vật hơn 100 nghìn trên 1 ml nước tiểu), xét nghiệm nitrit (với số lượng vi sinh vật nhiều hơn hơn 100 nghìn U, vi sinh vật phân hủy nitrit trong nước tiểu) được nhấn mạnh., với việc bổ sung axit sulfanilic và L-naphthylamine, màu đỏ xuất hiện), thử nghiệm TTX so màu (dưới tác dụng của dehydrogenase vi sinh vật, clorua triphenyltetrazolyte bị khử thành màu đỏ không tan triphenylformazan trong vòng 4-10 giờ ở nhiệt độ -37 ° C), thử nghiệm prednisolone khiêu khích (bệnh nhân thu thập trong một đĩa vô trùng, phần giữa của nước tiểu là phần đối chứng, sau đó 30 mg prednisolone trong 10 ml nước muối là được tiêm chậm vào tĩnh mạch và phần giữa của nước tiểu được thu thập ba lần trong khoảng thời gian hàng giờ và sau 24 giờ; trong viêm thận bể thận mãn tính, số lượng bạch cầu, vi khuẩn tăng gấp đôi, bạch cầu "hoạt động" xuất hiện, ít nhất trong một phần), kháng sinh đồ. Cần đặc biệt chú ý đến kính hiển vi lao thận (soi kính hiển vi nhuộm theo Tsil, cấy nước tiểu trên môi trường đặc biệt - phương pháp Preis và Shkolnikova, phương pháp sinh học). Nếu nghi ngờ quá trình đơn phương, cần tiến hành xét nghiệm nước tiểu, lấy riêng từng quả thận bằng các ống thông đặc biệt. Đóng vai trò quan trọng trong chẩn đoán viêm bể thận mạn tính bằng các phương pháp nghiên cứu X quang: chụp X quang khảo sát và chụp cắt lớp (mô tả vị trí, kích thước và hình dạng của thận), chụp bể thận bài tiết và ngược dòng (giảm nồng độ và khả năng bài tiết của thận, co thắt. , dị tật, dị dạng của khung chậu, đài hoa), chụp khí động học (để nhận biết sỏi không cản quang), chụp mạch thận (cho thấy sự vi phạm của kiến trúc mạch máu - động mạch và tĩnh mạch). Để xác định mức độ an toàn của chức năng và nhu mô thận, đặc biệt là với một quá trình đơn phương, các phương pháp chỉ định phóng xạ được sử dụng - chụp cắt lớp (hippuran iốt 131) và chụp cắt lớp (sử dụng neohydride Hg 203). Sinh thiết chọc dò trong trường hợp viêm bể thận do các ổ của quá trình có thể không cung cấp thông tin. Soi tế bào sắc tố có thể chỉ ra tổn thương thận. Điều trị. Thông thường, điều trị viêm bể thận là bảo tồn, tuy nhiên, nếu viêm bể thận cấp tính có mủ thì có thể cần phải can thiệp bằng phẫu thuật. Điều trị bảo tồn bao gồm chế độ điều trị, chế độ ăn uống, sử dụng kháng sinh cũng như các loại thuốc khác nhau giúp ổn định chức năng của thận và toàn bộ cơ thể bệnh nhân. Trong viêm thận bể thận cấp, nghỉ ngơi tại giường nghiêm ngặt được chỉ định. Thực phẩm nên được tiêu thụ là thực phẩm có chứa lượng protein, chất béo và carbohydrate tối ưu. Trong giai đoạn cấp tính cần ăn xen kẽ các loại thức ăn đạm và thực vật. Khi bị say nặng, bạn cần uống nhiều nước. Điều trị viêm thận bể thận mãn tính bao gồm tác động vào ổ nhiễm trùng (etiotropic) trong viêm bể thận nguyên phát và loại bỏ nguyên nhân này hoặc nguyên nhân khác trong viêm bể thận thứ phát, cơ chế bệnh sinh và điều trị các biến chứng. Điều trị hiệu quả nhất là sau khi xác định kháng sinh đồ. Điều trị liên tục (ít nhất 2 tháng) bằng thuốc kháng khuẩn được thực hiện. Ngay sau khi nhập viện, một loại thuốc kháng sinh, sulfanilamide hoặc nitrofuran được kê đơn. Sau 1-10 ngày, các loại thuốc được thay đổi, điều trị được thực hiện cho đến khi sự biến mất dai dẳng của bạch cầu và vi khuẩn niệu. Ngay sau khi đợt cấp được loại bỏ, điều trị ngắt quãng với một trong các chất kháng khuẩn được thực hiện trong 4-5 tháng: thuốc được đưa ra trong 7 ngày, sau đó nghỉ ngơi trong 8-10 ngày, hoặc thuốc được cho 10 ngày với khoảng cách 15-20 ngày, hoặc thuốc được dùng trong 15 ngày, khoảng thời gian được thực hiện trong 15 ngày, sau đó điều trị kháng sinh lại được kê đơn. Thời gian và khoảng thời gian điều trị được xác định bởi các triệu chứng lâm sàng và kiểm soát trong phòng thí nghiệm. Cần chỉ ra rằng trong trường hợp viêm bể thận đã phát triển ở bệnh nhân bị viêm amidan mãn tính, kháng sinh thuộc dòng penicillin có hiệu quả nhất; trong trường hợp nhiễm trùng sinh dục ở nam và nữ, kháng sinh phổ rộng được sử dụng (xem Bảng 12) . Với sự hiện diện của vi khuẩn gram âm, điều trị bằng axit nalidixic cho kết quả tốt (người da đen, tức vi khuẩn - 1,0 g 4 lần một ngày trong 7 ngày, nhưng các chế phẩm của nó nên được kê đơn ít thường xuyên hơn các loại thuốc khác (2 lần)). Từ các chế phẩm sulfanilamide, etazol (1,0 g x 4 lần - 10 ngày), solafur (0,1 g 3 lần), sulfonamid tác dụng kéo dài được sử dụng. Ngoài ra, các khóa học được điều trị bằng furazolidone, furadonin, furagin (0,1 g 4 lần một ngày). Cần phải nhấn mạnh rằng chức năng thận cần được xác định trước khi bắt đầu điều trị. Điều trị kháng sinh dài hạn nên được thực hiện với mức lọc cầu thận ít nhất là 30 ml / phút, hoặc với hàm lượng nitơ dư trong huyết thanh không quá 70 mg. Một chỉ số đánh giá hiệu quả của thuốc sau một tuần điều trị là số lượng vi sinh vật giảm xuống còn 10 trong 000 ml nước tiểu. Có thể làm giảm độc lực của hệ vi sinh và tăng hiệu quả của tác nhân kháng khuẩn bằng cách thay đổi phản ứng của nước tiểu 10-14 ngày một lần. Thực phẩm tạo kiềm, natri citrat (10 g mỗi ngày), nước khoáng kiềm giúp giảm phản ứng pH. Một số hoạt động kháng khuẩn có natri benzoat (4-6 g mỗi ngày), có nhiều trong quả nam việt quất và quả gấu. Liệu pháp di truyền bệnh nên nhằm mục đích tăng phản ứng của cơ thể, cải thiện lượng nước tiểu ra ngoài và bình thường hóa huyết áp. Để kích hoạt phản ứng sinh học miễn dịch, sử dụng α-globulin, tự động hóa trị liệu, truyền máu, liệu pháp vắc xin (điều trị autovaccine được thực hiện trong 30-40 ngày, 0,1 ml tiêm dưới da hoặc 0,2-0,3 ml mỗi 2 ngày), độc tố tụ cầu (0,1-0,3- 0,5-0,7-1,0-1,2-1,7-2,0 ml 3 ngày một lần). Các loại thảo mộc lợi tiểu (bearberry, quả bách xù, cỏ đuôi ngựa, lá orthosiphon - trà thận, lá cây linh chi), thuốc chống co thắt (papaverine, no-shpa, v.v.) giúp bình thường hóa dòng nước tiểu. Nếu có sự cản trở dòng chảy của nước tiểu, điều trị phẫu thuật được chỉ định. Với tăng huyết áp đồng thời, các chế phẩm rauwolfia được chỉ định - isobarine, dopegyt, hemiton, thuốc lợi tiểu, thuốc đối kháng aldosterone. Dự phòng và tiên lượng. Phòng ngừa viêm bể thận bao gồm các biện pháp chính và phụ. Phòng ngừa chính bao gồm, trước hết, điều trị các bệnh có thể dẫn đến sự phát triển của viêm bể thận: nhiễm trùng khu trú, bệnh tiết niệu (như sỏi niệu, u tuyến tiền liệt, cũng như bất kỳ bệnh nào kèm theo vi phạm dòng nước tiểu từ thận), các hoạt động giải trí. Bảng 12 So sánh hiệu quả của các loại thuốc kháng khuẩn trong viêm thận bể thận
Phòng ngừa thứ cấp bao gồm việc phát hiện vi khuẩn niệu khi khám dự phòng (ví dụ, phụ nữ mang thai nên tiến hành phân tích vi khuẩn trong nước tiểu ít nhất một lần một tháng), chỉ định điều trị chống tái phát: tuần đầu tiên của mỗi tháng - tạm dừng điều trị: nước sắc tầm xuân, tuần thứ hai, thứ ba - thuốc lợi tiểu thảo dược và thuốc sát trùng, tuần thứ tư - chất kháng khuẩn (nitrofurans, kháng sinh, thuốc sát trùng, mỗi năm một lần - nevigramon 1 g 1 lần trong tuần và 1,0 g - trong tuần thứ hai, hoặc 4 -NOC 2-5 mg x 100 lần một ngày 150-4 ngày). Điều trị chống tái phát được thực hiện trong 2-3 năm. Việc khám bệnh và điều trị nên được thực hiện 3-4 lần một năm hoặc 4-6 lần. Dự báo. Tiên lượng phụ thuộc vào giai đoạn của bệnh. Trị liệu spa. Điều trị tại khu nghỉ dưỡng điều dưỡng được chỉ định trong thời gian thuyên giảm, đặc biệt đối với những bệnh nhân bị viêm bể thận do sỏi thứ phát sau phẫu thuật tiết niệu (Truskavets, Sairme, Zheleznovodsk, Berezovsky nước khoáng), nơi bệnh nhân uống nước có hàm lượng khoáng chất thấp. Điều trị Sanatorium-and-spa được chống chỉ định trong trường hợp tăng huyết áp cao, thiếu máu nặng và suy thận rõ ràng. Các biến chứng của viêm bể thận rất đa dạng. Trong viêm thận bể thận cấp tính, sự tiến triển của quá trình tạo mủ dẫn đến sự hợp nhất của các ổ áp xe lớn và hình thành một khối thận, sự thông thương của các khoang chứa mủ với khung chậu (thận bể thận), quá trình chuyển đổi thành một nang xơ (viêm quanh thận. ) và mô quanh thận (viêm thận). Viêm thận bể thận cấp có thể biến chứng do hoại tử các nhú của kim tự tháp (u nhú), phát triển do tác dụng gây độc trực tiếp của vi khuẩn trong tình trạng ứ nước tiểu. Biến chứng viêm bể thận này xảy ra với hầu hết các trường hợp bệnh nhân mắc bệnh tiểu đường. Hiếm khi, viêm bể thận trở thành nguồn lây nhiễm trùng huyết. Với sự hạn chế của quá trình tạo mủ trong thời kỳ sẹo, áp xe được bao quanh bởi một màng sinh mủ (áp xe thận mãn tính) có thể hình thành. Trong viêm bể thận mãn tính, đặc biệt là một bên, có thể phát triển chứng tăng huyết áp do thận và xơ vữa động mạch ở thận thứ hai (còn nguyên vẹn). Sự nhăn nheo đài bể thận hai bên của thận dẫn đến suy thận mãn tính. Kết quả của viêm bể thận cấp thường là hồi phục, nhưng do hậu quả của các biến chứng (thận hư, nhiễm trùng huyết, u nhú), có thể tử vong. Viêm thận bể thận mãn tính với nếp nhăn của thận thường kết thúc bằng tăng ure huyết tăng ure huyết. Với sự phát triển của tăng huyết áp động mạch có nguồn gốc từ thận, kết quả gây tử vong trong viêm thận bể thận mãn tính đôi khi kết hợp với các biến chứng xảy ra trong tăng huyết áp (xuất huyết não, nhồi máu cơ tim, v.v.). Tác giả: Mostovaya O.S.
▪ Kinh tế doanh nghiệp. Ghi chú bài giảng
Máy tỉa hoa trong vườn
02.05.2024 Kính hiển vi hồng ngoại tiên tiến
02.05.2024 Bẫy không khí cho côn trùng
01.05.2024
▪ Đồng hồ nguyên tử xác nhận thuyết tương đối ▪ Cảm biến chuyển động Philips Hue điều khiển đèn
▪ phần của trang web Thợ điện trong nhà. Lựa chọn các bài viết ▪ bài báo Sự nhẹ nhàng không thể chịu nổi của bản thể. biểu hiện phổ biến ▪ bài viết Nỗi ám ảnh xã hội là gì? đáp án chi tiết ▪ bài viết Cao nguyên Putorana. thiên nhiên kỳ diệu ▪ bài báo Công cụ tìm dây ẩn trên chip logic. Bách khoa toàn thư về điện tử vô tuyến và kỹ thuật điện ▪ bài viết Intercom với cuộc gọi tự động. Bách khoa toàn thư về điện tử vô tuyến và kỹ thuật điện
Trang chủ | Thư viện | bài viết | Sơ đồ trang web | Đánh giá trang web www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese








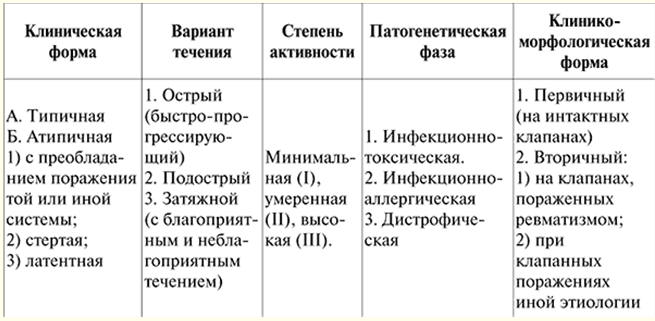








 Xem các bài viết khác razdela
Xem các bài viết khác razdela 